下列推断正确的是 ( )
| A.BF3为三角锥型分子 |
B.NH4+的电子式为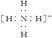 ,离子呈平面正方形结构 ,离子呈平面正方形结构 |
| C.CH4分子中的4个C—H键都是氢原子的1s轨道与碳原子的2p轨道形成的spσ键 |
| D.甲醛分子为平面三角形,有一个π键垂直于三角形平面 |
17-18高二下·宁夏吴忠·单元测试 查看更多[3]
(已下线)专题11.2 分子结构与性质(练)-《2020年高考一轮复习讲练测》贵州省安顺市普定县第一中学2018-2019学年高二上学期12月考试化学试题宁夏吴忠市高二人教版选修3第2章 分子结构与性质综合练习2
更新时间:2018-02-11 22:22:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】观察下列模型并结合有关信息,判断有关说法正确的是
| 硼晶体结构单元 | SF6分子 | S8 | HCN | |
| 结构模型示意图 |
|
|
|
|
| 备注 | 熔点1873K | — | 易溶于CS2 | — |
| A.单质硼属于共价晶体 | B.SF6是由极性键构成的极性分子 |
| C.固态硫S8属于共价晶体 | D.HCN的结构式为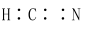 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】NH3、NH4Cl、NO、NO2、HNO3等是氮重要的化合物,NO2与N2O4能相互转化,热化学方程式为N2O4(g) 2NO2(g) △H=+57kJ•mol-1。NO在大气中能转化为NO2、HNO2、HNO3等。机动车尾气中的NO可通过催化还原的方法转化为N2。下列有关NH3、NH
2NO2(g) △H=+57kJ•mol-1。NO在大气中能转化为NO2、HNO2、HNO3等。机动车尾气中的NO可通过催化还原的方法转化为N2。下列有关NH3、NH 、NO
、NO 、HNO3的说法
、HNO3的说法不 正确的是
 2NO2(g) △H=+57kJ•mol-1。NO在大气中能转化为NO2、HNO2、HNO3等。机动车尾气中的NO可通过催化还原的方法转化为N2。下列有关NH3、NH
2NO2(g) △H=+57kJ•mol-1。NO在大气中能转化为NO2、HNO2、HNO3等。机动车尾气中的NO可通过催化还原的方法转化为N2。下列有关NH3、NH 、NO
、NO 、HNO3的说法
、HNO3的说法A.NH3转化为NH ,其键角变小 ,其键角变小 |
| B.NH3沸点较高是因为分子间存在氢键 |
C.NO 空间构型为V形 空间构型为V形 |
| D.浓HNO3保存在玻璃塞的棕色试剂瓶中 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】铁、氮气、丙酮和乙醇可参与制备铁氮化合物(FexNy),以下说法不正确的是
| A.Fe元素位于元素周期表的第VIIIB族 |
| B.丙酮中碳原子采用sp2和sp3杂化 |
| C.1个N2分子中有1个σ键和2个π键 |
| D.乙醇的沸点高于丙烷,是因为乙醇分子间存在氢键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】纯水电离产生 、
、 ,研究发现在某些水溶液中还存在
,研究发现在某些水溶液中还存在 、
、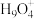 等微粒。下列说法错误的是
等微粒。下列说法错误的是
 、
、 ,研究发现在某些水溶液中还存在
,研究发现在某些水溶液中还存在 、
、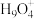 等微粒。下列说法错误的是
等微粒。下列说法错误的是A. 和 和 所含电子数相同 所含电子数相同 | B.键角: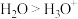 |
C. 中 中 原子是 原子是 杂化 杂化 | D. 、 、 、 、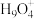 微粒中均含有配位键 微粒中均含有配位键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关含氯的物质或微粒说法不正确 的是
A.随Cl元素化合价升高, 、 、 、 、 、 、 和 和 的氧化性增强 的氧化性增强 |
B. 、 、 和 和 中心原子轨道的杂化类型均为sp3 中心原子轨道的杂化类型均为sp3 |
| C.NaF、NaCl、NaBr的熔点依次降低,原因是晶体的晶格能随离子核间距的增大而减小 |
| D.配合物Pt(NH3)2Cl2存在顺反异构体,分别称为顺铂和反铂。顺铂为极性分子,相同温度时在水中的溶解度大于反铂 |
您最近半年使用:0次

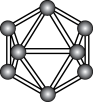
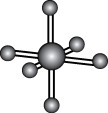
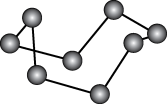
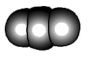
 ②NCl3③H2O④BF3⑤BeCl2
②NCl3③H2O④BF3⑤BeCl2

