碱式氯化镁(MgOHCl)常用作塑料添加剂,我国首创利用氢氧化镁与氯化铵热分解制氨气并得到碱式氯化镁的工艺。某科研小组根据该原理设计了如图实验装置制备碱式氧化镁并探究氨的还原性,反应前,装置C中CuO的质量为14.40g。
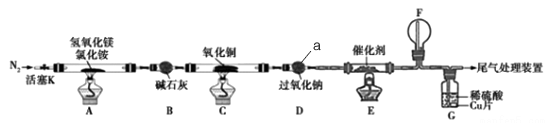
请回答下列问题:
(1)仪器a的名称是_______ .
(2)装置A中发生反应的化学方程式为____________ ,装置B的作用是_________ ,装置D的作用是________
(3)装置G中的现象为____________
(4)反应结束后装置C中的氧化铜完全反应生成红色固体,并测得其质量为12.24g。则红色固体是______ (填化学式),该反应中转移电子的物质的量为_______ mol.
(5)完成下列实验方案,证明装置C中完全反应后得到的红色固体中含有氧化亚铜(供选择的试剂:2mol/L的HNO3溶液、2mol/L的H2SO4溶液、2mol/L的NaOH溶液)。
已知:Cu2O+2H+=Cu2++Cu+H2O.

请回答下列问题:
(1)仪器a的名称是
(2)装置A中发生反应的化学方程式为
(3)装置G中的现象为
(4)反应结束后装置C中的氧化铜完全反应生成红色固体,并测得其质量为12.24g。则红色固体是
(5)完成下列实验方案,证明装置C中完全反应后得到的红色固体中含有氧化亚铜(供选择的试剂:2mol/L的HNO3溶液、2mol/L的H2SO4溶液、2mol/L的NaOH溶液)。
已知:Cu2O+2H+=Cu2++Cu+H2O.
| 实验步骤 | 预期现象和结论 |
| 步骤1取装置C中所得红色固体于大试管中 | ----- |
| 步骤2: |
更新时间:2018-03-08 16:55:18
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为(MgCO3,舍少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
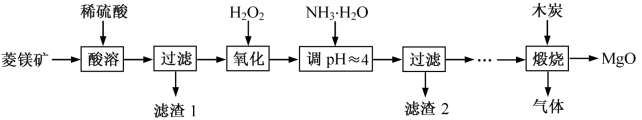
(1)加入H2O2氧化时,发生反应的化学方程式为___________________________ 。
(2)滤渣2的成分是_________ (填化学式)。
煅烧过程存在以下反应:
2MgSO4+C 2MgO+2SO2↑+CO2↑;MgSO4+C
2MgO+2SO2↑+CO2↑;MgSO4+C MgO+SO2↑+CO↑;MgSO4+3C
MgO+SO2↑+CO↑;MgSO4+3C MgO+S↑+3CO↑。
MgO+S↑+3CO↑。
利用下图装置对煅烧产生的气体进行分步吸收或收集。
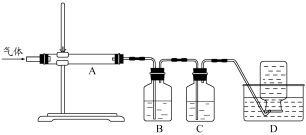
(3)D中收集的气体是__________ (填化学式)。
(4)B中盛放的溶液是_________ (填序号)。
a.NaOH溶液 b.Na2CO3溶液 c.稀硝酸 d..KMnO4溶液
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:_________________________

(1)加入H2O2氧化时,发生反应的化学方程式为
(2)滤渣2的成分是
煅烧过程存在以下反应:
2MgSO4+C
 2MgO+2SO2↑+CO2↑;MgSO4+C
2MgO+2SO2↑+CO2↑;MgSO4+C MgO+SO2↑+CO↑;MgSO4+3C
MgO+SO2↑+CO↑;MgSO4+3C MgO+S↑+3CO↑。
MgO+S↑+3CO↑。利用下图装置对煅烧产生的气体进行分步吸收或收集。

(3)D中收集的气体是
(4)B中盛放的溶液是
a.NaOH溶液 b.Na2CO3溶液 c.稀硝酸 d..KMnO4溶液
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z三种物质有如图所示转化关系,其中X与稀盐酸不反应:
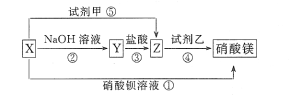
(1)根据上述转化关系,推断下列物质的化学式: X_____ ,Y_____ ,Z____ ,试剂甲____ ,试剂乙____ 。
(2)写出上述①~⑤步反应的离子方程式:
①____________________________________________ 。
②____________________________________________ 。
③____________________________________________ 。
④____________________________________________ 。
⑤____________________________________________ 。

(1)根据上述转化关系,推断下列物质的化学式: X
(2)写出上述①~⑤步反应的离子方程式:
①
②
③
④
⑤
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如下:
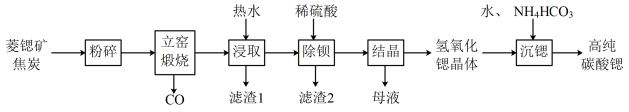
Sr(OH)2在水中的溶解度
(1)元素Sr位于元素周期表第_______ 周期第_______ 族。
(2)菱锶矿、焦炭混合粉碎的目的是_______ 。
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为_______ 。进行煅烧反应的立窑衬里应选择_______ (填“石英砂砖”或“碱性耐火砖”)。
(4)“浸取”中用热水浸取而不用冷水的原因是_______ ;滤渣1含有焦炭、Ca(OH)2和_______ 。
(5)“沉锶”中反应的化学方程式为_______ 。
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则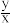 为
为_______ (取整数)。

Sr(OH)2在水中的溶解度
温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
溶解度/(g/100g) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(2)菱锶矿、焦炭混合粉碎的目的是
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为
(4)“浸取”中用热水浸取而不用冷水的原因是
(5)“沉锶”中反应的化学方程式为
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则
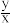 为
为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】硅在生活、生活和科学研究中具有广泛的应用。回答下列问题:
(1)硅在元素周期表的位置是___________ 。
(2)请写出硅的原子结构示意图___________ 。
(3)氮化硅是一种性能优良的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,根据以上描述,推测氮化硅可能有哪些用途:___________ (填字母)。
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作电线
(4)若要下图装置证明酸性: 。
。

从以下所给物质中选出甲同学设计的实验所用到的物质:①稀 ;②稀盐酸;③碳酸钙;④
;②稀盐酸;③碳酸钙;④ 溶液;⑤
溶液;⑤ 。试剂A与C分别为
。试剂A与C分别为___________ 、___________ (填序号);试管中发生反应的离子方程式为___________ 。有同学认为此实验不能说明酸性强弱,你认为原因是___________ 。
(1)硅在元素周期表的位置是
(2)请写出硅的原子结构示意图
(3)氮化硅是一种性能优良的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,根据以上描述,推测氮化硅可能有哪些用途:
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作电线
(4)若要下图装置证明酸性:
 。
。
从以下所给物质中选出甲同学设计的实验所用到的物质:①稀
 ;②稀盐酸;③碳酸钙;④
;②稀盐酸;③碳酸钙;④ 溶液;⑤
溶液;⑤ 。试剂A与C分别为
。试剂A与C分别为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】2020年初,突如其来的新型冠状肺炎在全世界肆虐,依据研究,含氯消毒剂可以有效灭活新冠病毒,为阻断疫情做出了巨大贡献。二氧化氯(ClO2)就是其中一种高效消毒灭菌剂。氯酸钠还原法是目前使用较为广泛的ClO2制备方法,其中一种是用NaClO3与CH3OH在催化剂、60℃时,发生反应得到ClO2,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
已知:①ClO2的浓度较大时易分解爆炸,一般用CO2或空气稀释到10%以下;实验室也常用稳定剂吸收ClO2,生成NaClO2,使用时加酸只释放出ClO2一种气体;
②ClO2与KI反应的离子方程式为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O
③

请回答:
(1)仪器d的名称是___________ ,仪器b在装置中的作用是___________ ;比较仪器c和e,实验中c的优点是___________ 。
(2)根据反应条件判断制备装置甲中需改进的一项措施是___________ 。
(3)反应中甲醇被氧化为甲酸,写出制备ClO2的化学方程式:___________ ;该制备法可选用不同的还原性物质作为还原剂,例如草酸(草酸的氧化产物为CO2),相比甲醇法,草酸法的优点是___________ 。
(4)下列有关说法正确的是___________ 。
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的ClO2
B.装置f主要用于检验是否有Cl2生成
C.在ClO2释放实验中,发生的离子反应方程式是:4H++5 =Cl-+4ClO2↑+2H2O
=Cl-+4ClO2↑+2H2O
D.ClO2和Cl2都为强氧化剂,在相同条件下,等物质的量时,ClO2的氧化能力是Cl2的2倍
已知:①ClO2的浓度较大时易分解爆炸,一般用CO2或空气稀释到10%以下;实验室也常用稳定剂吸收ClO2,生成NaClO2,使用时加酸只释放出ClO2一种气体;
②ClO2与KI反应的离子方程式为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O
③
物质 | CH3OH | HCOOH | ClO2 |
沸点 | 64.7℃ | 100.8℃ | 11℃ |

请回答:
(1)仪器d的名称是
(2)根据反应条件判断制备装置甲中需改进的一项措施是
(3)反应中甲醇被氧化为甲酸,写出制备ClO2的化学方程式:
(4)下列有关说法正确的是
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的ClO2
B.装置f主要用于检验是否有Cl2生成
C.在ClO2释放实验中,发生的离子反应方程式是:4H++5
 =Cl-+4ClO2↑+2H2O
=Cl-+4ClO2↑+2H2OD.ClO2和Cl2都为强氧化剂,在相同条件下,等物质的量时,ClO2的氧化能力是Cl2的2倍
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】一种利用水钴矿[主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等]制取CoCl2·6H2O的工艺流程如下:
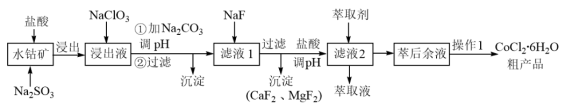
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Al3+、Mn2+、Ca2+、Mg2+等
②部分阳离子开始沉淀和完全沉淀的pH见下表

③CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定,加热至110~120℃时失去结晶水变成无水氯化钴。
(1)写出Co2O3与Na2SO3和盐酸反应的离子方程式______________________ 。
(2)加入NaClO3的目的是______________________ ;加入过量NaClO3可能生成有毒气体,该气体是___________ (填化学式)
(3)为了除去Fe3+、Al3+,需加Na2CO3调pH,则pH应控制的范围为_____________________ .
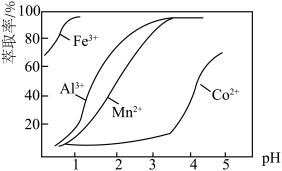
(4)加萃取剂的目的是___________ ;金属离子在萃取剂中的萃取率与pH的关系如图,据此分析pH的最佳范围为___________ (填字母序号)。
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)CoCl2·6H2O常用减压烘干法烘干,原因是___________ 。

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Al3+、Mn2+、Ca2+、Mg2+等
②部分阳离子开始沉淀和完全沉淀的pH见下表

③CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定,加热至110~120℃时失去结晶水变成无水氯化钴。
(1)写出Co2O3与Na2SO3和盐酸反应的离子方程式
(2)加入NaClO3的目的是
(3)为了除去Fe3+、Al3+,需加Na2CO3调pH,则pH应控制的范围为

(4)加萃取剂的目的是
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)CoCl2·6H2O常用减压烘干法烘干,原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】化合物X由两种元素 组成,为探究其组成和性质,设计并完成如下实验:

已知:固体2为一种常见氧化物,呈红棕色。请回答:
(1)固体1的化学式是___________ ,X的化学式是___________ 。
(2)化合物X在空气中高温煅烧的化学方程式为___________ 。
(3)加热条件下氨气被固体2氧化成一种气体单质,同时生成金属单质。写出该反应的化学方程式___________ 。
(4)简述检验磁性氧化物固体1中金属价态的实验方案___________ 。

已知:固体2为一种常见氧化物,呈红棕色。请回答:
(1)固体1的化学式是
(2)化合物X在空气中高温煅烧的化学方程式为
(3)加热条件下氨气被固体2氧化成一种气体单质,同时生成金属单质。写出该反应的化学方程式
(4)简述检验磁性氧化物固体1中金属价态的实验方案
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】我国《食品添加剂使用卫生标准》中规定葡萄酒中SO2最大使用量为0.25g·L-1.某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中的SO2,并对其含量进行测定。
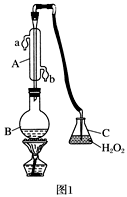

(1)仪器B的名称是___________ ,冷却水的进口为___________ (填“a”或“b” )
(2) B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为___________
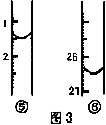
(3)除去C中过量的H2O2,然后用0.0900mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的___________
(4)若选择酚酞作为指示剂,滴定终点的现象是___________ ;滴定前和滴定后,滴定管中的液面如图3中所示,消耗NaOH溶液的体积为___________ mL。
(5)利用上述步骤测定的量,计算该葡萄酒中SO2含量为:___________ g·L-1。
(6)该测定结果总是比实际值偏高,分析可能原因__________



(1)仪器B的名称是
(2) B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为
(3)除去C中过量的H2O2,然后用0.0900mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的
(4)若选择酚酞作为指示剂,滴定终点的现象是
(5)利用上述步骤测定的量,计算该葡萄酒中SO2含量为:
(6)该测定结果总是比实际值偏高,分析可能原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】由于亚硝酸钠和食盐性状相似,曾多次发生过将NaNO2误当食盐食用的事件。欲测定某样品中NaNO2的含量,某同学设计如下实验:
①称取样品ag,加水溶解,配制成100mL溶液。
②取25.00mL溶液于锥形瓶中,用0.0200mol/LKMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液VmL。
(1)上述实验①所需玻璃仪器除烧杯、玻璃棒、胶头滴管之外还有_______ 。
(2)在进行滴定操作时,KMnO4溶液盛装在_______ (填“酸式”或“碱式”)滴定管中。当滴入最后一滴溶液,_______ 时达到滴定终点。
(3)滴定过程中发生反应的离子方程式是_______ ;测得该样品中NaNO2的质量分数为_______ 。
(4)以下操作造成测定结果偏高的是_______。
(5)大量的碘富集在海藻中,用水浸取后浓缩。浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中 =
=_______ 。(结果保留两位有效数字)(已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17)
(6)已知: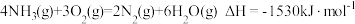 ,
,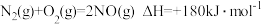 ,写出
,写出 还原
还原 的热化学方程式:
的热化学方程式:_______ 。
①称取样品ag,加水溶解,配制成100mL溶液。
②取25.00mL溶液于锥形瓶中,用0.0200mol/LKMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液VmL。
(1)上述实验①所需玻璃仪器除烧杯、玻璃棒、胶头滴管之外还有
(2)在进行滴定操作时,KMnO4溶液盛装在
(3)滴定过程中发生反应的离子方程式是
(4)以下操作造成测定结果偏高的是_______。
| A.滴定管未用KMnO4标准溶液润洗 |
| B.锥形瓶未用待测液润洗 |
| C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失 |
| D.若滴定过程中刚出现颜色变化就停止滴定 |
 =
=(6)已知:
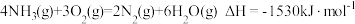 ,
,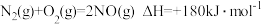 ,写出
,写出 还原
还原 的热化学方程式:
的热化学方程式:
您最近一年使用:0次



