A B C D E是前四周期元素,且原子序数依次增大。A的原子核中只有一个质子;B原子外围电子排布nSn nPn ;D原子核外有2个电子层,S轨道电子总数和P轨道电子总数相等;E2+ 的M能层上各能级的电子数之比为1:3:3 请回答下列问题:
(1)E原子基态电子排布式_______________________
(2)这五种元素中电负性最大的是________________ (填元素符号,下同)第一电离能最小的是__________________
(3)化合物EBC2中阴离子是BC22-,和BC2 2- 互为等电子体的分子有C2D和____________ ,由此可知BC2 2- 的空间构型是___________ 。
(4)由A C两元素形成一种10电子分子X,写出X的电子式_________
X可与多种金属离子形成配合物。钴有两种化学式均为Co(X)5BrSO4的配合物,且配位数均为6,则它们分别溶于水时电离出的阳离子的化学式可能是_______________ 和______________ ;
(5)A C两元素还能形成一种离子化合物,写出该化合物化学式__________ ;你认为该化合物中除了离子键外还存在化学键是__________________ ;该化合物溶于水有气体产生,写出反应化学方程式________________________
(1)E原子基态电子排布式
(2)这五种元素中电负性最大的是
(3)化合物EBC2中阴离子是BC22-,和BC2 2- 互为等电子体的分子有C2D和
(4)由A C两元素形成一种10电子分子X,写出X的电子式
X可与多种金属离子形成配合物。钴有两种化学式均为Co(X)5BrSO4的配合物,且配位数均为6,则它们分别溶于水时电离出的阳离子的化学式可能是
(5)A C两元素还能形成一种离子化合物,写出该化合物化学式
10-11高二下·福建福州·期中 查看更多[1]
(已下线)2010-2011学年福建省福州八县(市)一中高二下学期期中联考化学试卷
更新时间:2016-12-09 01:44:49
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】氮和氧是构建化合物的常见元素。
(1)下列说法正确的是___________。
(2)①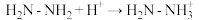 ,其中
,其中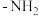 的
的 原子杂化方式为
原子杂化方式为___________ ;比较键角 中的-NH2
中的-NH2_____ H2N-NH 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由___________ 。
②将 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是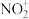 。比较氧化性强弱:NO
。比较氧化性强弱:NO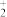
_____ HNO3(填“>”、“<”或“=”);写出A中阴离子的结构式___________ 。
已知: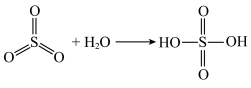
(1)下列说法正确的是___________。
A.电负性: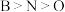 | B.离子半径: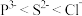 |
C.第一电离能: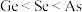 | D.基态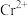 的简化电子排布式: 的简化电子排布式: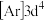 |
(2)①
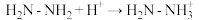 ,其中
,其中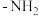 的
的 原子杂化方式为
原子杂化方式为 中的-NH2
中的-NH2 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由②将
 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是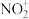 。比较氧化性强弱:NO
。比较氧化性强弱:NO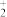
您最近一年使用:0次
【推荐2】大连理工大学彭孝军院士课题组报道了基于氟硼荧类荧光染料(BODIPY)的铜荧光探针的设计与应用,利用Cu2+诱导胺的氧化脱氢反应形成的Cu2+配合物,进行Hela细胞中的Cu2+荧光成像和检测,荧光染料(BODIPY)的结构如图所示。
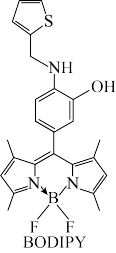
回答下列问题:
(1)写出Cu2+的核外电子排布式:_______ 。
(2)BODIPY荧光探针分子中,硼原子的杂化方式为_______ ,1 mol BODIPY分子中含有_______ mol配位键,其中位于第二周期的元素原子的第一电离能由大到小的顺序为:_______ 。
(3)磷锡青铜是有名的弹性材料,广泛用于仪器仪表中的耐磨零件和抗磁元件等。磷锡青铜的晶胞结构如图所示。NA代表阿伏加德罗常数的值,铜、磷原子间的最短距离为0.5apm。

①磷锡青铜的化学式为_______ 。
②磷锡青铜晶体的密度ρ_______ g/cm3 (用代数式表示)。

回答下列问题:
(1)写出Cu2+的核外电子排布式:
(2)BODIPY荧光探针分子中,硼原子的杂化方式为
(3)磷锡青铜是有名的弹性材料,广泛用于仪器仪表中的耐磨零件和抗磁元件等。磷锡青铜的晶胞结构如图所示。NA代表阿伏加德罗常数的值,铜、磷原子间的最短距离为0.5apm。

①磷锡青铜的化学式为
②磷锡青铜晶体的密度ρ
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】湖南是我国矿产资源大省,磷储量丰富。回答下列问题:
(1)第三周期元素的原子中,第一电离能大于磷原子的有_______ 种
(2)氮族元素氢化物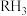 (
( 、
、 、
、 )的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物(
)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物(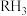 )性质可能为_______(填序号)。
)性质可能为_______(填序号)。

(3)白磷P4分子P-P键之间键角为_______ ,P原子的杂化方式为_______
(4)磷酸为磷的最高价含氧酸,其空间结构如下:

①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是_______ 。
②键能大小比较:磷氧双键_______ (填“大于”“等于”或“小于”)磷氧单键。
③键角大小比较α:_______ β(填“大于”“等于”或“小于”)。
④磷的含氧酸中,酸性:H3PO4_______ (填“ 大于”或“小于”)H3PO3。
⑤次磷酸根( )的球棍模型如图所示,下列说法错误的是
)的球棍模型如图所示,下列说法错误的是_______

A.P的原子结构示意图为:
B.次磷酸根的电子式为:
C.次磷酸根的结构式为:
D.次磷酸钠的化学式为:NaH2PO2,该化合物次磷酸的酸式盐。
(5)磷化硼是一种半导体材料,其晶胞结构如图所示。其化学式为:_______

(1)第三周期元素的原子中,第一电离能大于磷原子的有
(2)氮族元素氢化物
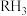 (
( 、
、 、
、 )的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物(
)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物(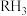 )性质可能为_______(填序号)。
)性质可能为_______(填序号)。
| A.稳定性 | B.沸点 | C.分子间作用力 | D.还原性 |
(4)磷酸为磷的最高价含氧酸,其空间结构如下:

①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是
②键能大小比较:磷氧双键
③键角大小比较α:
④磷的含氧酸中,酸性:H3PO4
⑤次磷酸根(
 )的球棍模型如图所示,下列说法错误的是
)的球棍模型如图所示,下列说法错误的是
A.P的原子结构示意图为:

B.次磷酸根的电子式为:

C.次磷酸根的结构式为:

D.次磷酸钠的化学式为:NaH2PO2,该化合物次磷酸的酸式盐。
(5)磷化硼是一种半导体材料,其晶胞结构如图所示。其化学式为:

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】过氧乙酸又名过醋酸(C2H4O3),是重要化工原料。也是一种绿色生态杀菌剂,其制法为CH3COOH+H2O2=CH3COOOH+H2O。
(1)某同学写出了碳原子的4种不同状态的电子排布图____ 。
A.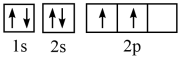 B.
B.
C.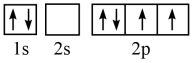 D.
D.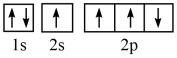
其中能量最低的是____ (填标号),电子由状态C到状态B所得到的光谱为____ 光谱(填“原子发射”或“原子吸收”)。
(2)过氧乙酸分子中C原子的杂化方式有____ 。
(3)乙酸比乙醇易电离出H+的原因____ 。
(4)乙酸和硝酸分子中所包含元素电负性由大到小的顺序是____ (用元素符号表示)。
(5)造纸中,用NaBH4与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化铝被认为是有机化学上的“万能还原剂”。
①两种硼氢化物的熔点如表所示:
解释表中两种物质熔点差异的原因____ 。
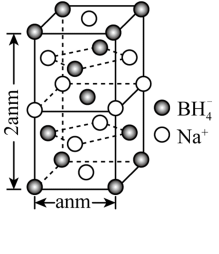
②硼氢化钠晶胞结构如图所示,该晶体中Na+的配位数为____ 。已知:硼氢化钠晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值,则a=___ nm(用含ρ、NA的最简式子表示)
(1)某同学写出了碳原子的4种不同状态的电子排布图
A.
 B.
B.
C.
 D.
D.
其中能量最低的是
(2)过氧乙酸分子中C原子的杂化方式有
(3)乙酸比乙醇易电离出H+的原因
(4)乙酸和硝酸分子中所包含元素电负性由大到小的顺序是
(5)造纸中,用NaBH4与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化铝被认为是有机化学上的“万能还原剂”。
①两种硼氢化物的熔点如表所示:
| 硼氢化物 | NaBH4 | Al(BH4)3 |
| 熔点/℃ | 400 | -64.5 |
②硼氢化钠晶胞结构如图所示,该晶体中Na+的配位数为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】I.表中列出了第三周期的几种元素的部分性质:
请按要求回答下列问题:
(1)写出基态a原子的价层电子排布式:____ 。
(2)表中元素原子半径最大的是(写元素符号)_____ 。
(3)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)_____ 。
(4)d、e最高价氧化物对应水化物相互反应的离子方程式为_____ 。
(5)表中五种元素的第一电离能由大到小的顺序是(写元素符号)____ 。
II.硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(6)Se原子结构示意图可表示为____ 。
(7)下列说法合理的是____ 。
a.SeO2既有氧化性又有还原性 b.沸点:H2O<H2S<H2Se
c.热稳定性:H2Se<HCl<H2S d.酸性:H2SeO4<HBrO4<HClO4
| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(1)写出基态a原子的价层电子排布式:
(2)表中元素原子半径最大的是(写元素符号)
(3)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)
(4)d、e最高价氧化物对应水化物相互反应的离子方程式为
(5)表中五种元素的第一电离能由大到小的顺序是(写元素符号)
II.硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(6)Se原子结构示意图可表示为
(7)下列说法合理的是
a.SeO2既有氧化性又有还原性 b.沸点:H2O<H2S<H2Se
c.热稳定性:H2Se<HCl<H2S d.酸性:H2SeO4<HBrO4<HClO4
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】物质的组成与结构决定了物质的性质与变化。请回答下列问题:
(1)钠元素的焰色反应呈黄色,其中黄色对应的辐射波长为______ nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)C、H、N、O四种元素中电负性最大的是______  填元素符号
填元素符号 ,写出Fe2+的最外层电子排布式
,写出Fe2+的最外层电子排布式______ 。根据等电子原理,写出CN-的电子式______ ,CNO-中心原子的杂化方式为______ 。
(3) 的沸点比
的沸点比
______  填“高”或“低”
填“高”或“低” ;原因是
;原因是______ 。
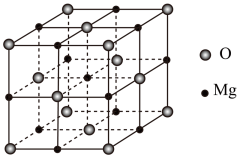
(4)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为______ nm;MnO也属于NaCl型结构,晶胞参数为a’=0.448nm,则r(Mn2+)为______ nm。
(1)钠元素的焰色反应呈黄色,其中黄色对应的辐射波长为
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)C、H、N、O四种元素中电负性最大的是
 填元素符号
填元素符号 ,写出Fe2+的最外层电子排布式
,写出Fe2+的最外层电子排布式(3)
 的沸点比
的沸点比
 填“高”或“低”
填“高”或“低” ;原因是
;原因是(4)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】某些过渡金属(如钛、铜)及其化合物,以其高导电性和丰富的物理化学性质在材料领域大放异彩。
(1)钛比钢轻、比铝硬。基态钛原子的价层电子排布式为_______ :钛原子核外电子占据的轨道数_______ 。
(2)铜的下列状态中,失去最外层一个电子所需能量最小的是_______。
(3)二氧化钛是良好的光催化剂,可催化转化多种有毒物质,如:可将水中的 转化为
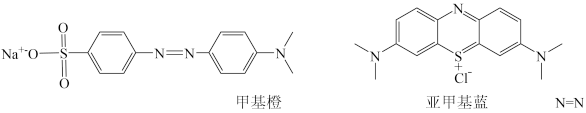
转化为 ,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
① 的空间构型是
的空间构型是_______ 。
②甲基橙、亚甲基蓝中C原子的杂化类型有_______ ,
③常温下,CO2、HCHO在水中溶解度之比大约是1:500,其主要原因是_______ 。
(4)黄铜矿炼铜过程中会产生SO2,与SO2互为等电子体的分子和阴离子分别为_______ (各写一种即可)。
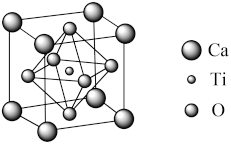
(5)钙钛矿型太阳能电池近年越来越受到科学界的关注,其效率提升速度超越过去任何一类电池。某种钙钛矿晶胞如图所示,则钙原子的配位数是_______ ,若阿伏加德罗常数的值为NA,晶胞中钙原子与氧原子的最近距离为a pm。则该晶胞的密度为_______ g/cm3.(列出计算式)
(1)钛比钢轻、比铝硬。基态钛原子的价层电子排布式为
(2)铜的下列状态中,失去最外层一个电子所需能量最小的是_______。
| A.[Ar]3dl04pl | B.[Ar]3d10 | C.[Ar]3d94s1 | D.[Ar]3d104s1 |
 转化为
转化为 ,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
①
 的空间构型是
的空间构型是②甲基橙、亚甲基蓝中C原子的杂化类型有
③常温下,CO2、HCHO在水中溶解度之比大约是1:500,其主要原因是
(4)黄铜矿炼铜过程中会产生SO2,与SO2互为等电子体的分子和阴离子分别为
(5)钙钛矿型太阳能电池近年越来越受到科学界的关注,其效率提升速度超越过去任何一类电池。某种钙钛矿晶胞如图所示,则钙原子的配位数是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】下图为钠的某种氧化物D的晶胞和H3BO3(层状结构)的结构示意图。请回答下列问题:


(1)基态硼原子的电子排布图为:_______ 其第一电离能小于Be,原因是_______ 。
(2)三价B易形成多种配离子如[B(OH)4]-、BH 离子[B(OH)4]-的空间构型为
离子[B(OH)4]-的空间构型为_______ 。硼酸显弱酸性与该配离子有关写出硼酸的电离方程式_______ 。写出一种与BH 互为等电子体的分子的电子式
互为等电子体的分子的电子式_______ 。
(3)在硼酸的层状结构中B的杂化类型是_______ 层内存在的作用力有_______ 。
(4)D的化学式为_______ ;晶胞中O原子的配位数为_______ ;已知该晶体F的密度为dg·cm-3,晶胞参数a=_______ nm。


(1)基态硼原子的电子排布图为:
(2)三价B易形成多种配离子如[B(OH)4]-、BH
 离子[B(OH)4]-的空间构型为
离子[B(OH)4]-的空间构型为 互为等电子体的分子的电子式
互为等电子体的分子的电子式(3)在硼酸的层状结构中B的杂化类型是
(4)D的化学式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】镍是一种用途广泛的金属,常用于电镀工业和制造电池。镍易形成Ni(CO)4、[Ni(NH3)6]SO4等配合物。
(1)Ni2+的核外电子排布式为_______ 。
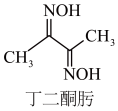
(2)Ni2+可用丁二酮肟检验。丁二酮肟的结构如图所示,其分子中碳原子轨道的杂化类型为_______ 。
(3)与CO互为等电子体的阴离子的化学式为_______ 。
(4)1mol [Ni(NH3)6]SO4中σ键的数目为_______ 。氨的沸点高于膦(PH3),原因是_______ 。
(5)镧镍合金是较好的储氢材料。储氢后所得晶体的化学式为LaNi5H6,晶胞结构如图所示,X、Y、Z表示储氢后的三种微粒,则图中Z表示的微粒为_______ (填化学式)。

(1)Ni2+的核外电子排布式为
(2)Ni2+可用丁二酮肟检验。丁二酮肟的结构如图所示,其分子中碳原子轨道的杂化类型为

(3)与CO互为等电子体的阴离子的化学式为
(4)1mol [Ni(NH3)6]SO4中σ键的数目为
(5)镧镍合金是较好的储氢材料。储氢后所得晶体的化学式为LaNi5H6,晶胞结构如图所示,X、Y、Z表示储氢后的三种微粒,则图中Z表示的微粒为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】第三代太阳能电池是铜铟镓硒CIGS等化合物薄太阳能电池以及薄膜Si系太阳能电池。请回答下列问题:
(1)晶体Si中硅原子的杂化方式是_______ ,基态Ga原子的价电子排布式是_______ 。
(2)H2O沸点_______ (填“高于”或“低于”)H2Se的沸点,其原因是_______ 。
(3)向硫酸铜溶液中逐滴滴加浓氨水,先出现蓝色絮状沉淀,后沉淀逐渐溶解得到[Cu(NH3)4]SO4的深蓝色透明溶液。
①在[Cu(NH3)4]2+中,Cu2+与NH3之间形成的化学键称为_______ ,提供孤电子对的成键原子是_______ 。
②锌与铜位于同一周期。硫化锌的结构如图甲所示,硫离子周围等距离且最近的锌离子个数是_______ ;某含铜化合物的晶胞如图乙所示,晶胞上下底面为正方形,侧面与底面垂直,则该化合物的化学式是_______ ,设NA为阿伏加德罗常数的值,则该晶胞的密度是_______ g/cm3(用含a、b、NA的代数式表示)。

(1)晶体Si中硅原子的杂化方式是
(2)H2O沸点
(3)向硫酸铜溶液中逐滴滴加浓氨水,先出现蓝色絮状沉淀,后沉淀逐渐溶解得到[Cu(NH3)4]SO4的深蓝色透明溶液。
①在[Cu(NH3)4]2+中,Cu2+与NH3之间形成的化学键称为
②锌与铜位于同一周期。硫化锌的结构如图甲所示,硫离子周围等距离且最近的锌离子个数是

您最近一年使用:0次
【推荐2】硼及其化合物应用广泛。回答下列问题:
(1)基态B原子的价电子轨道表达式为____________________________ ,其第一电离能比Be____________ (填“大”或“小”)
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是______________ 。

(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图。
① B原子的杂化方式为_____________ 。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:________________________________________________________ 。
② 路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸的原因是_______________________________ 。
(1)基态B原子的价电子轨道表达式为
(2)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是

(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图。
① B原子的杂化方式为
② 路易斯酸碱理论认为,任何可接受电子对的分子或离子叫路易斯酸,任何可给出电子对的分子或离子叫路易斯碱。从结构角度分析硼酸是路易斯酸的原因是
您最近一年使用:0次
【推荐3】按要求完成下列各题:
(1)基态溴原子的价层电子轨道表达式为________ 。
(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有_______(填标号)。
(3)Al元素可形成[AlF6]3-、[AlCl4]-配离子,而B元素只能形成[BF4]-配离子,由此可知决定配合物中配位数多少的因素是________________ ;
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是________________
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是_________ 。

A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
(1)基态溴原子的价层电子轨道表达式为
(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有_______(填标号)。
| A.都属于p区主族元素 | B.电负性都比镁大 |
| C.第一电离能都比镁大 | D.氯化物的水溶液pH均小于7 |
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是

A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
您最近一年使用:0次



