某些过渡金属(如钛、铜)及其化合物,以其高导电性和丰富的物理化学性质在材料领域大放异彩。
(1)钛比钢轻、比铝硬。基态钛原子的价层电子排布式为_______ :钛原子核外电子占据的轨道数_______ 。
(2)铜的下列状态中,失去最外层一个电子所需能量最小的是_______。
(3)二氧化钛是良好的光催化剂,可催化转化多种有毒物质,如:可将水中的 转化为
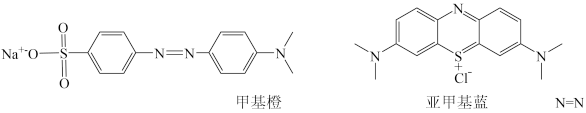
转化为 ,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
① 的空间构型是
的空间构型是_______ 。
②甲基橙、亚甲基蓝中C原子的杂化类型有_______ ,
③常温下,CO2、HCHO在水中溶解度之比大约是1:500,其主要原因是_______ 。
(4)黄铜矿炼铜过程中会产生SO2,与SO2互为等电子体的分子和阴离子分别为_______ (各写一种即可)。
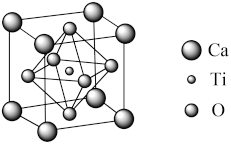
(5)钙钛矿型太阳能电池近年越来越受到科学界的关注,其效率提升速度超越过去任何一类电池。某种钙钛矿晶胞如图所示,则钙原子的配位数是_______ ,若阿伏加德罗常数的值为NA,晶胞中钙原子与氧原子的最近距离为a pm。则该晶胞的密度为_______ g/cm3.(列出计算式)
(1)钛比钢轻、比铝硬。基态钛原子的价层电子排布式为
(2)铜的下列状态中,失去最外层一个电子所需能量最小的是_______。
| A.[Ar]3dl04pl | B.[Ar]3d10 | C.[Ar]3d94s1 | D.[Ar]3d104s1 |
 转化为
转化为 ,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
,将甲基橙、亚甲基蓝、HCHO转化为CO2等。
①
 的空间构型是
的空间构型是②甲基橙、亚甲基蓝中C原子的杂化类型有
③常温下,CO2、HCHO在水中溶解度之比大约是1:500,其主要原因是
(4)黄铜矿炼铜过程中会产生SO2,与SO2互为等电子体的分子和阴离子分别为
(5)钙钛矿型太阳能电池近年越来越受到科学界的关注,其效率提升速度超越过去任何一类电池。某种钙钛矿晶胞如图所示,则钙原子的配位数是

2023·河南·二模 查看更多[4]
内蒙古自治区包头市2024届高三二模理科综合-化学试题陕西省铜川市2023届高三下学期第二次模拟考试理综化学试题(已下线)狂飙卷 04-【热题狂飙】2023年高考化学样卷(全国卷专用)河南省平许济洛四市2023届高三下学期第二次质量检测理科综合化学试题
更新时间:2023-03-16 17:23:59
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硼及其化合物在医疗、航空航天、超导磁体、储能材料、微波通信和动力装置上具有广泛的应用价值。
(1)固体储氢材料NH3BH3中,N原子的核外电子排布式为___________ ,B原子的杂化轨道类型为___________ ,N和B的第一电离能大小:N___________ B(填“大于”“小于”或“等于”)。
(2)氨羧基硼烷能抑制肿瘤和降低血清胆固醇,其结构与甘氨酸(NH2CH2COOH)类似,氨羧基硼烷的结构简式为___________ 。
(3)化学式为B2H6、B5H9、B6H10的硼氢化合物具有巢形结构,该硼氢化合物的通式可表示为___________ 。
(4)硼中子俘获疗法(BNCT)是一种针对脑、头、颈部肿瘤的一种新型放射疗法,该法涉及利用低能中子照射硼化合物,将13B标记的硼化合物注射到患者体内,用中子照射10B发生核裂变产生氦核(α粒子)和7Li核,裂变过程反应式为___________ 。
(5)物质的硬度和晶格焓密度(晶格焓除以物质的摩尔体积)之间的关系如图所示(碳的点代表金刚石)。氮化硼能用作高温动力装置磨料的原因是___________ 。

(6)立方氮化硼是一种用于航空航天的热绝缘体纳米材料,晶胞结构如图,晶胞参数为anm。晶体的密度ρ=___________ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)固体储氢材料NH3BH3中,N原子的核外电子排布式为
(2)氨羧基硼烷能抑制肿瘤和降低血清胆固醇,其结构与甘氨酸(NH2CH2COOH)类似,氨羧基硼烷的结构简式为
(3)化学式为B2H6、B5H9、B6H10的硼氢化合物具有巢形结构,该硼氢化合物的通式可表示为
(4)硼中子俘获疗法(BNCT)是一种针对脑、头、颈部肿瘤的一种新型放射疗法,该法涉及利用低能中子照射硼化合物,将13B标记的硼化合物注射到患者体内,用中子照射10B发生核裂变产生氦核(α粒子)和7Li核,裂变过程反应式为
(5)物质的硬度和晶格焓密度(晶格焓除以物质的摩尔体积)之间的关系如图所示(碳的点代表金刚石)。氮化硼能用作高温动力装置磨料的原因是

(6)立方氮化硼是一种用于航空航天的热绝缘体纳米材料,晶胞结构如图,晶胞参数为anm。晶体的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】氮化镓(GaN)材料是第三代半导体的代表,通常以GaCl3为镓源,NH3为氮源制备,具有出色的抗击穿能力,能耐受更高的电子密度。
(1)基态Ga价电子排布图为___________ 。
(2)Ga、N和O的第一电离能由小到大的顺序为___________ ,NO 的空间构型为
的空间构型为___________ ,与其互为等电子体的微粒有___________ (任写一种)
(3)GaCl3熔点为77.9℃,气体在270℃左右以二聚物存在,GaF3熔点1000℃,GaCl3二聚体的结构式为___________ ,其熔点低于GaF3的原因为___________ 。
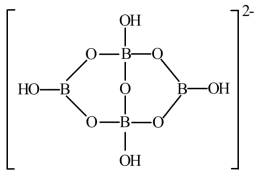
(4)与镓同主族的B具有缺电子性,硼砂(四硼酸钠Na2B4O7·10H2O)中B4O 是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应写成[B4O5(OH)4]2-的形式,结构如图所示,则该离子存在的作用力有
是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应写成[B4O5(OH)4]2-的形式,结构如图所示,则该离子存在的作用力有___________ ,B原子的杂化方式为___________ 。
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键 F.配位键
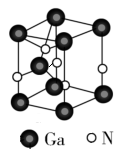
(5)氮化镓的晶胞如图所示,Ga原子与N原子半径分别为a pm和b pm,阿伏加德罗常数的值为NA,晶胞密度为c g/cm3,则该晶胞的空间利用率为___________ (已知空间利用率为晶胞内原子体积占晶胞体积的百分比)。
(1)基态Ga价电子排布图为
(2)Ga、N和O的第一电离能由小到大的顺序为
 的空间构型为
的空间构型为(3)GaCl3熔点为77.9℃,气体在270℃左右以二聚物存在,GaF3熔点1000℃,GaCl3二聚体的结构式为
(4)与镓同主族的B具有缺电子性,硼砂(四硼酸钠Na2B4O7·10H2O)中B4O
 是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应写成[B4O5(OH)4]2-的形式,结构如图所示,则该离子存在的作用力有
是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应写成[B4O5(OH)4]2-的形式,结构如图所示,则该离子存在的作用力有
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键 F.配位键
(5)氮化镓的晶胞如图所示,Ga原子与N原子半径分别为a pm和b pm,阿伏加德罗常数的值为NA,晶胞密度为c g/cm3,则该晶胞的空间利用率为

您最近一年使用:0次
【推荐3】“摩尔盐”是分析化学中的重要试剂,化学式为(NH4)2Fe(SO4)2·6H2O。“摩尔盐”在一定条件下分解的方程式为:4[(NH4)2Fe(SO4)2·6H2O]  2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
(1)铁元素在元素周期表中的位置为_____ ,其价层电子排布图为________ 。
(2)组成“摩尔盐”的非金属元素中第一电离能最大的元素为________ 。“摩尔盐”的分解产物中属于非极性分子的化合物是________ 。
(3)NH3 的沸点比N2O 的沸点_____ (填“高”或“低”),其主要原因是________________ 。
(4)K3[Fe(CN)6]常用于检验Fe2+,K3[Fe(CN)6]中除了离子键以外还存在的化学键为_______ ,与CN- 互为等电子体的单质的分子式为________ 。HCN 分子中σ键和π键的个数之比为________ 。
(5)FeO 晶胞结构如下图所示,FeO 晶体中Fe2+配位数为______ ,若该晶胞边长为acm,则该晶胞密度为________ 。

 2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:(1)铁元素在元素周期表中的位置为
(2)组成“摩尔盐”的非金属元素中第一电离能最大的元素为
(3)NH3 的沸点比N2O 的沸点
(4)K3[Fe(CN)6]常用于检验Fe2+,K3[Fe(CN)6]中除了离子键以外还存在的化学键为
(5)FeO 晶胞结构如下图所示,FeO 晶体中Fe2+配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】铁、钻、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:
(1)基态钴原子的价电子排布式为________ ,铁、钴、镍的基态原子核外未成对电子数最少的是_____________
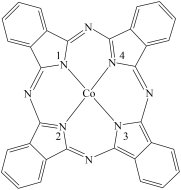
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是__________ (填1、2、3、4),三种非金属原子的电负性由大到小的顺序为____ (用相应的元素符号表示);碳原子的杂化轨道类型为_________
(3)Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO) x晶体属于_______ (填晶体类型),若配合物Fe(CO) x的中心原子价电子数与配体提供电子数之和为18,则x=_________
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO______ FeO(填“>”“<”或“=”),原因是___________________________ 。
(5)NiAs的晶胞结构如图所示:
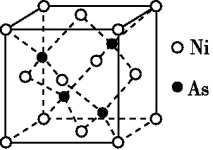
①镍离子的配位数为_________ 。
②若阿伏伽德罗常数的值为NA,晶体密度为pg.cm-1,则该晶胞中最近的离子之间的距离为_____ cm。(写出计算表达式)
(1)基态钴原子的价电子排布式为
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是

(3)Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO) x晶体属于
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO
(5)NiAs的晶胞结构如图所示:

①镍离子的配位数为
②若阿伏伽德罗常数的值为NA,晶体密度为pg.cm-1,则该晶胞中最近的离子之间的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的价电子排布式为____ 。
(2)磷的一种同素异形体是白磷(P4),其分子的空间构型为____ ,键角为____ ,推测其在CS2中的溶解度____ (填“大于”“等于”或“小于”)其在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因__________ 。
(4)常温下PCl5是一种白色晶体,其立方晶系晶胞结构模型如图所示,由A、B两种微粒构成。将其加热至148 ℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为____ ,其中心原子杂化轨道类型为_______ 。

(5)磷化硼(BP)是一种超硬耐磨涂层材料,如图为其立方晶胞,其中每个原子均满足8电子稳定结构,P原子的配位数为______ 。已知B—P键的键长为x cm,则磷化硼晶体的密度为____ g·cm-3(列出计算式即可)。
(1)基态P原子的价电子排布式为
(2)磷的一种同素异形体是白磷(P4),其分子的空间构型为
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因
(4)常温下PCl5是一种白色晶体,其立方晶系晶胞结构模型如图所示,由A、B两种微粒构成。将其加热至148 ℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为

(5)磷化硼(BP)是一种超硬耐磨涂层材料,如图为其立方晶胞,其中每个原子均满足8电子稳定结构,P原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。
(1)写出基态Mn原子的核外电子排布式________________________ 。
(2)CoTiO3晶体结构模型如图1所示。在CoTiO3晶体中1个Ti原子、1个Co原子,周围距离最近的O原子数目分别为_______ 个、_______ 个。
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂, 常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO- 互为等电子体的分子、离子化学式分别为______________ 、_______ (各写一种)。
(4)三聚氰胺是一种含氮化合物,其结构简式如图所示。
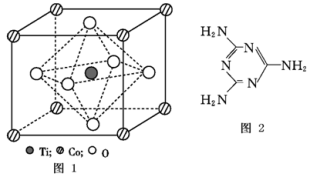
三聚氰胺分子中氮原子轨道杂化类型是______ ,1 mol三聚氰胺分子中σ键的数目为_______ 。
(1)写出基态Mn原子的核外电子排布式
(2)CoTiO3晶体结构模型如图1所示。在CoTiO3晶体中1个Ti原子、1个Co原子,周围距离最近的O原子数目分别为
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂, 常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO- 互为等电子体的分子、离子化学式分别为
(4)三聚氰胺是一种含氮化合物,其结构简式如图所示。

三聚氰胺分子中氮原子轨道杂化类型是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】化合物 是合成抗心律失常药物决泰达隆的一种中间体,可通过以下方法合成:
是合成抗心律失常药物决泰达隆的一种中间体,可通过以下方法合成:

(1)A中的含氧官能团名称为_______ ,_______ 。
(2) 的反应类型为
的反应类型为_______ 。
(3)化合物C分子中发生 杂化的碳原子数目为
杂化的碳原子数目为_______ 。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式_______ 。
①能发生银镜反应;
②能发生水解反应,其水解产物之一能与 溶液发生显色反应;
溶液发生显色反应;
③分子中只有4种不同化学环境的氢。
(5) 经还原得到
经还原得到 ,
, 的分子是为
的分子是为 ,写出
,写出 的结构简式
的结构简式_______ 。
 是合成抗心律失常药物决泰达隆的一种中间体,可通过以下方法合成:
是合成抗心律失常药物决泰达隆的一种中间体,可通过以下方法合成:
(1)A中的含氧官能团名称为
(2)
 的反应类型为
的反应类型为(3)化合物C分子中发生
 杂化的碳原子数目为
杂化的碳原子数目为(4)写出同时满足下列条件的C的一种同分异构体的结构简式
①能发生银镜反应;
②能发生水解反应,其水解产物之一能与
 溶液发生显色反应;
溶液发生显色反应;③分子中只有4种不同化学环境的氢。
(5)
 经还原得到
经还原得到 ,
, 的分子是为
的分子是为 ,写出
,写出 的结构简式
的结构简式
您最近一年使用:0次
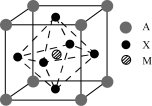
【推荐2】I某钙钛矿型太阳能电池吸光材料的晶胞结构如图所示,其中A通常为CH3NH3+,可由甲胺(CH3NH2)制得;M为Pb2+或Sn2+;X为卤离子,如Cl-、Br-等。___ (用A、X、M表示)。
(2)H、C、Cl三种元素的电负性由小到大的顺序为____ 。
(3)溴原子基态核外价电子排布式为___ 。
(4)甲胺(CH3NH2)极易溶于水,除因为它们都是极性分子外,还因为___ 。
(5)CH3NH2中N原子的轨道杂化类型为__ ;1mol CH3NH3+中含σ键的数目为____ 。
II 镍的单质、合金及其化合物用途非常广泛。
(1)Ni在周期表中的位置为___ 。
(2)[Ni(N2H4)2](N3)2是一种富氮含能材料。配体N2H4的熔沸点比C2H6高的多的原因是____ ;[Ni(N2H4)2]2+中含四个配位键,不考虑空间构型,[Ni(N2H4)2]2+的结构可用示意图表示为_____ 。
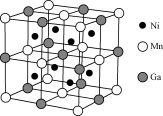
(3)一种新型的功能材料的晶胞结构如图所示,它的化学式可表示为___ 。每个Mn周围最近且等距离的Mn数目为___ ,每个Ga周围最近且等距离的Mn数目为____ 。
(2)H、C、Cl三种元素的电负性由小到大的顺序为
(3)溴原子基态核外价电子排布式为
(4)甲胺(CH3NH2)极易溶于水,除因为它们都是极性分子外,还因为
(5)CH3NH2中N原子的轨道杂化类型为
II 镍的单质、合金及其化合物用途非常广泛。
(1)Ni在周期表中的位置为
(2)[Ni(N2H4)2](N3)2是一种富氮含能材料。配体N2H4的熔沸点比C2H6高的多的原因是
(3)一种新型的功能材料的晶胞结构如图所示,它的化学式可表示为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】有下列8种晶体:A.水晶B.白磷C.冰醋酸D.固态氩E.氯化铵F.铝G.金刚石H.烧碱。用序号回答下列问题:
(1)含有非极性键的原子晶体是_______ ;属于分子晶体的单质是_______ ;含有离子键、共价键、配位键的化合物是_______ ;受热熔化,需克服共价键的是_______ 。
(2)在肺部,血红素中的Fe2+结合的水分子与氧分子交换,形成氧合血红蛋白,经动脉运送到组织释放出O2;然后血红素结合组织代谢所产生的CO2,经静脉送回肺中与水分子交换,最后将CO2排出体外,完成呼吸过程。血红素中Fe2+与CO2中的氧原子以配位键形式结合,这种结合是可逆的,比Fe2+与N的结合弱的原因是_______ 。
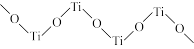
(3)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图,化学式为_______
(4)氨硼烷是一种特殊的化合物,分子式为NH3BH3.氨硼烷在催化剂作用下水解释放出氢气: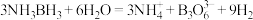 。
。 的结构如图。回答下列问题:
的结构如图。回答下列问题:

①请写出氧原子价电子轨道表达式_______ 。
②NH3BH3晶体中含有的微粒间作用力有_______ (填标号)。
a.非极性共价键 b.配位键 c.氢键 d.范德华力 e.金属键
③已知钛的一种常见化合物是 。1mol该物质中含有σ键的数目为
。1mol该物质中含有σ键的数目为_______
(5)图象是NaCl、CsCl、ZnS等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于NaCl的晶体结构的图是_______
(1)含有非极性键的原子晶体是
(2)在肺部,血红素中的Fe2+结合的水分子与氧分子交换,形成氧合血红蛋白,经动脉运送到组织释放出O2;然后血红素结合组织代谢所产生的CO2,经静脉送回肺中与水分子交换,最后将CO2排出体外,完成呼吸过程。血红素中Fe2+与CO2中的氧原子以配位键形式结合,这种结合是可逆的,比Fe2+与N的结合弱的原因是
(3)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图,化学式为

(4)氨硼烷是一种特殊的化合物,分子式为NH3BH3.氨硼烷在催化剂作用下水解释放出氢气:
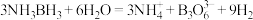 。
。 的结构如图。回答下列问题:
的结构如图。回答下列问题:
①请写出氧原子价电子轨道表达式
②NH3BH3晶体中含有的微粒间作用力有
a.非极性共价键 b.配位键 c.氢键 d.范德华力 e.金属键
③已知钛的一种常见化合物是
 。1mol该物质中含有σ键的数目为
。1mol该物质中含有σ键的数目为(5)图象是NaCl、CsCl、ZnS等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于NaCl的晶体结构的图是_______
A.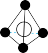 | B.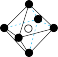 | C.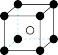 | D.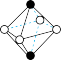 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过___________ 方法区分晶体、准晶体和非晶体。
(2)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是___________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有___________ 个铜原子。
(3)Cu2+能与乙二胺(H2N- CH2- CH2- NH2) 形成配离子如图: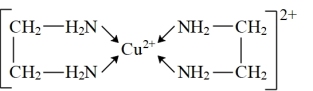 ,该配离子中含有的化学键类型有___________(填字母序号)。
,该配离子中含有的化学键类型有___________(填字母序号)。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗暴剂等。lmolFe(CO)5分子中含___________ molσ键。
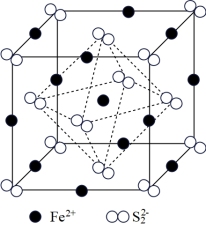
(5)FeS2晶体的晶胞如图所示。晶胞边长为a nm,FeS2的相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________ g·cm-3
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是
(3)Cu2+能与乙二胺(H2N- CH2- CH2- NH2) 形成配离子如图:
 ,该配离子中含有的化学键类型有___________(填字母序号)。
,该配离子中含有的化学键类型有___________(填字母序号)。| A.配位键 | B.极性键 | C.离子键 | D.非极性键 |
(5)FeS2晶体的晶胞如图所示。晶胞边长为a nm,FeS2的相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态镍原子价电子排布式为___________ 。
(2)丁二酮肟( )是检验Ni2+的灵敏试剂,常与Ni2+形成图I所示的配合物,图II是硫代氧的结果:
)是检验Ni2+的灵敏试剂,常与Ni2+形成图I所示的配合物,图II是硫代氧的结果:
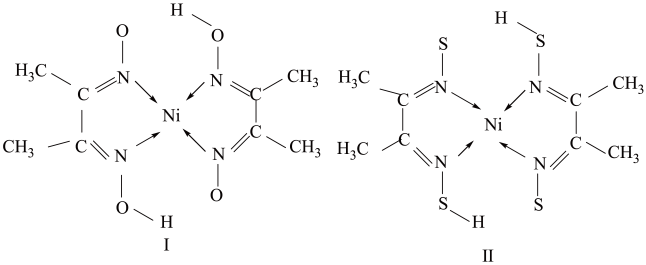
①下列说法正确的有___________ (填字母)。
A.在I中N元素的电负性最大 B.在I中C-C-C键角是180°
C.在II中-SH 上的S原子采取sp3杂化 D.在II中存在σ键、Π键与配位键
②化合物I的熔、沸点高于化合物II的原因是___________ 。
(3)工业上选用硫酸和硝酸的混酸与Ni反应制备NiSO4。写出与SO 互为等电子体的一种分子
互为等电子体的一种分子___________ 。Fe、Co、Ni三种元素二价离子的硫酸盐晶体的晶胞类型相同,其熔点由高到低的顺序为___________ 。
(4)Ni和La的合金是目前使用广泛的储氢材料。该合金的晶胞结构如图所示。
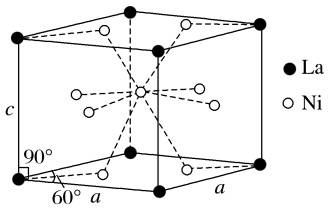
①设该合金的密度为dg/cm3,则该晶胞的体积为___________ cm3(用含 d的代数式表示,NA表示阿伏加德罗常数的值)
②该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子时比较稳定。已知:a=500pm,c=400pm;标准状况下氢气的密度为9.00×10-5g/cm3; 储氢能力= 。若忽略储氢前后晶胞的体积变化,则该合金的储氢能力为
。若忽略储氢前后晶胞的体积变化,则该合金的储氢能力为___________ (列出最简计算式,计算式不使用小数。NA表示阿伏加德罗常数的值)。
(1)基态镍原子价电子排布式为
(2)丁二酮肟(
 )是检验Ni2+的灵敏试剂,常与Ni2+形成图I所示的配合物,图II是硫代氧的结果:
)是检验Ni2+的灵敏试剂,常与Ni2+形成图I所示的配合物,图II是硫代氧的结果:
①下列说法正确的有
A.在I中N元素的电负性最大 B.在I中C-C-C键角是180°
C.在II中-SH 上的S原子采取sp3杂化 D.在II中存在σ键、Π键与配位键
②化合物I的熔、沸点高于化合物II的原因是
(3)工业上选用硫酸和硝酸的混酸与Ni反应制备NiSO4。写出与SO
 互为等电子体的一种分子
互为等电子体的一种分子(4)Ni和La的合金是目前使用广泛的储氢材料。该合金的晶胞结构如图所示。

①设该合金的密度为dg/cm3,则该晶胞的体积为
②该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子时比较稳定。已知:a=500pm,c=400pm;标准状况下氢气的密度为9.00×10-5g/cm3; 储氢能力=
 。若忽略储氢前后晶胞的体积变化,则该合金的储氢能力为
。若忽略储氢前后晶胞的体积变化,则该合金的储氢能力为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】碳材料在生活中占有重要地位。
请回答:
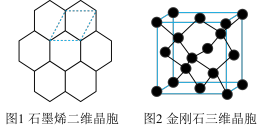
(1)下列说法正确的是 。
(2)图 1 中 C—C 键键长为 apm,则石墨烯的密度ρ=______________ g/cm2 (用含 a 式子表示,阿伏伽德罗常数为 NA)
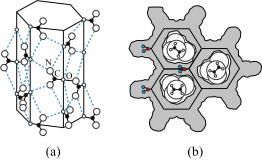
(3)尿素[(NH2)2CO]可以与正烷烃(n~CmH2m+2,m≥8)形成超分子包合物。尿素中各种元素的电负性由大到小的顺序________________ ,尿素分子通过______________________ 氢键(写出具体形式)
有序地组合成具有蜂窝状六角形通道结构的接受体,如(a)所示。正烷烃分子作为底物填入到通道之中,图(b)示出垂直于通道截面的结构。该超分子包合物能稳定存在的原因是_________________________ 。
请回答:

(1)下列说法正确的是 。
| A.石墨烯碳采用 sp2杂化,金刚石 VSPRE 模型为正四面体形 |
| B.多层石墨烯和金刚石均为共价型晶体 |
| C.1mol 石墨烯与金刚石中,σ键键数之比为 3:4 |
| D.石墨烯中 C—C 键键能较金刚石大,故石墨烯的内能更高 |
(3)尿素[(NH2)2CO]可以与正烷烃(n~CmH2m+2,m≥8)形成超分子包合物。尿素中各种元素的电负性由大到小的顺序
有序地组合成具有蜂窝状六角形通道结构的接受体,如(a)所示。正烷烃分子作为底物填入到通道之中,图(b)示出垂直于通道截面的结构。该超分子包合物能稳定存在的原因是

您最近一年使用:0次



