I、完成下列填空。
(1)第三周期中,第一电离能最小的元素是___________ ,第一电离能最大的元素是___________ 。(填元素符号)
(2)分子中σ键数目:C2H4_____ CH4 ;原子轨道能量:3d___________ 4s(用“>”或“<”完成下列填空)
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的___________ 键更稳定(填“σ”或“π”)
II、A、B、C代表3种元素。请填空:
(1)A的原子的3p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:_______________________________ ,核外电子运动状态有_______ 种。
(2)B是原子序数为35的元素,其原子中有___________ 个电子层,有_________ 个能级。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,元C素基态原子的电子排布式为____________________________ ,其单质在一定条件下能与浓硫酸反应,试写出该反应方程式:____________________________ 。
(1)第三周期中,第一电离能最小的元素是
(2)分子中σ键数目:C2H4
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的
II、A、B、C代表3种元素。请填空:
(1)A的原子的3p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:
(2)B是原子序数为35的元素,其原子中有
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,元C素基态原子的电子排布式为
更新时间:2018-04-19 10:26:48
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】新型半导体材料如碳化硅(SiC)、氮化镓(GaN)等在国防技术、航空航天及5G技术等领域扮演着重要的角色。回答下列问题:
(1)基态Si原子中,核外电子占据的最高能层的符号为_____ ,占据最高能级的电子的电子云轮廓图形状为_____ ;基态Ga原子的核外电子排布为[Ar]3d104s2p1,其转化为下列激发态时,吸收能量最少的是_____ (填选项字母)。
A.[Ar]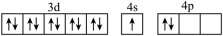 B.[Ar]
B.[Ar]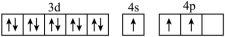
C.[Ar]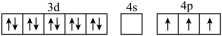 D.[Ar]
D.[Ar]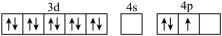
(2)C与Si是同主族元素,C原子之间可以形成双键、叁键,但Si原子之间难以形成双键、叁键。从原子结构分析,其原因为_____ 。
(3)硼(B)与Ga是同主族元素,硼氢化钠(NaBH4)是有机合成中重要的还原剂,其阴离子BH 的立体构型为
的立体构型为_____ ;另一种含硼阴离子的结构如图所示,其中B原子的杂化方式为_____ 。
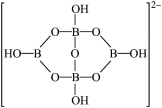
(4)GaCl3的熔点为77.9℃,GaF3的熔点为1000℃,试分析GaCl3熔点低于GaF3的原因为_____ ;气态GaCl3常以二聚体形式存在,二聚体中各原子均满足8e-结构,据此写出二聚体的结构式为_____ 。
(1)基态Si原子中,核外电子占据的最高能层的符号为
A.[Ar]
 B.[Ar]
B.[Ar]
C.[Ar]
 D.[Ar]
D.[Ar]
(2)C与Si是同主族元素,C原子之间可以形成双键、叁键,但Si原子之间难以形成双键、叁键。从原子结构分析,其原因为
(3)硼(B)与Ga是同主族元素,硼氢化钠(NaBH4)是有机合成中重要的还原剂,其阴离子BH
 的立体构型为
的立体构型为
(4)GaCl3的熔点为77.9℃,GaF3的熔点为1000℃,试分析GaCl3熔点低于GaF3的原因为
您最近一年使用:0次
【推荐2】人们常在过渡元素中寻找制造催化剂和耐高温、耐腐蚀合金的元素。
(1)纳米TiO2是种应用广泛的催化剂,在太阳光照射下,可以降解酚、醛等多种有机物。22号元素钛位于元素周期表的_______ 区,基态钛原子的价层电子轨道表示式为_______ 。TiCl4的水解反应可以制得TiO2·xH2O,过滤后再经焙烧可以得到TiO2,写出TiCl4水解反应的化学方程式_______ 。
(2)铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。对于基态 原子,下列叙述不正确的是_______(填标号)。
原子,下列叙述不正确的是_______(填标号)。
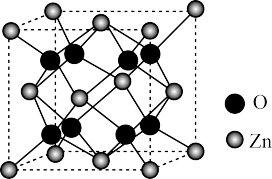
(3)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图所示。Zr4+离子在晶胞中的配位数是_______ ,晶胞参数为a pm、a pm、c pm,该晶体密度为_______  (写出表达式,用a、c和NA表示,
(写出表达式,用a、c和NA表示, )。
)。
(1)纳米TiO2是种应用广泛的催化剂,在太阳光照射下,可以降解酚、醛等多种有机物。22号元素钛位于元素周期表的
(2)铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。对于基态
 原子,下列叙述不正确的是_______(填标号)。
原子,下列叙述不正确的是_______(填标号)。| A.核外电子有24种运动状态,处在7个不同的能级上 |
| B.核外电子排布是[Ar]3d54s1,是第四周期元素中未成对电子数最多的元素 |
| C.4s电子能量较高,总是在比3s电子离核更远的地方运动 |
| D.电负性比钾大,原子对键合电子的吸引力比钾大 |
 (写出表达式,用a、c和NA表示,
(写出表达式,用a、c和NA表示, )。
)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】据媒体报道,法国一家公司 Tiamat 日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠离子电池,预计从 2020 年开始实现工业生产。该电池的负极材料为 Na2Co2TeO6(制备原料为 Na2CO3、Co3O4和TeO2),电解液为 NaClO4 的碳酸丙烯酯溶液。 回答下列问题:
(1)Te 属于元素周期表中______ 区元素,其基态原子的价电子排布式为______ 。
(2)基态 Na 原子中,核外电子占据的原子轨道总数为______ ,最高能层电子云轮廓图形状为______ 。
(3)结合题中信息判断:C、O、Cl 的电负性由大到小的顺序为______ (用元素符号表示)。
(4)CO32-的几何构型为______ ;碳酸丙烯酯的结构简式如图所示,则其中碳原子的杂化轨道类型为______ ,1mol 碳酸丙烯酯中σ键的数目为______ 。

(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是______ ,该配离子包含的作用力为______ (填选项字母)。
A.离子键 B.极性键 C.配位键 D.氢键 E.金属键
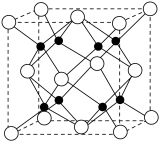
(6)Na 和 O 形成的离子化合物的晶胞结构如图所示,晶胞中 O 的配位数为______ ,该晶胞的密度为ρg/cm3,阿伏加 德罗常数的值为 NA,则Na与O之间的最短距离为______ cm(用 ρ、NA 的代数式表示)。
(1)Te 属于元素周期表中
(2)基态 Na 原子中,核外电子占据的原子轨道总数为
(3)结合题中信息判断:C、O、Cl 的电负性由大到小的顺序为
(4)CO32-的几何构型为

(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是
A.离子键 B.极性键 C.配位键 D.氢键 E.金属键
(6)Na 和 O 形成的离子化合物的晶胞结构如图所示,晶胞中 O 的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铍及其化合物的应用正日益被重视。
(1)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价层电子的轨道表示式为___________ 。
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有___________(填字母)。
(3)氯化铍在气态时存在BeCl2分子(a)和二聚分子(BeCl2)2(b), a的VSEPR模型为___________ ,a属于___________ (填“极性”或“非极性”)分子。
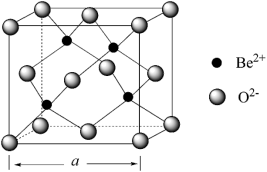
(4)BeO立方晶胞如图所示。若BeO晶体的密度为d g·cm-3, 阿伏加德罗常数为6.02×1023 mol-1,则晶胞棱长a=___________ nm 。
(1)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价层电子的轨道表示式为
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有___________(填字母)。
| A.都属于p区主族元素 | B.电负性都比镁大 |
| C.第一电离能都比镁大 | D.氯化物的水溶液pH均小于7 |
(4)BeO立方晶胞如图所示。若BeO晶体的密度为d g·cm-3, 阿伏加德罗常数为6.02×1023 mol-1,则晶胞棱长a=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵【(NH4)3Fe(C6H5O7)2】。
(1)铁原子在周期表中的位置为_______ ,其外围电子的轨道表达式为_______ ;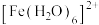 中与Fe2+配位的原子是
中与Fe2+配位的原子是_______ (填元素符号)。
(2)NH3分子中氮原子的轨道杂化类型是_______ ;C、N、O元素的第一电离能由大到小的顺序为_______ 。
(3)与 互为等电子体的一种分子为
互为等电子体的一种分子为_______ (填化学式)。
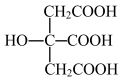
(4)柠檬酸的结构简式如图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为_______ mol。
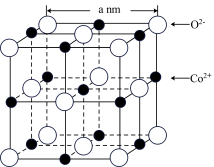
(5)CoO的面心立方晶胞如图所示。设阿伏加德罗常数的值为NA,则CoO晶体的密度为_______ g﹒cm−3。
(1)铁原子在周期表中的位置为
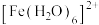 中与Fe2+配位的原子是
中与Fe2+配位的原子是(2)NH3分子中氮原子的轨道杂化类型是
(3)与
 互为等电子体的一种分子为
互为等电子体的一种分子为(4)柠檬酸的结构简式如图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为

(5)CoO的面心立方晶胞如图所示。设阿伏加德罗常数的值为NA,则CoO晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】过渡金属铬、铅、镍、铁及其化合物在工业上有重要用途,回答下列问题:
(1)Cr基态原子价电子的轨道表示式___________ 。
(2)氮化铬(CrN)在超级电容器领域具有良好的应用前景,可由CrCl3·6H2O与尿素[(NH2)2CO]反应先得到配合物{Cr[OC(NH2)2]6}Cl3,然后在通有NH3和N2混合气体的反应炉内热分解制得。
①尿素中C、N、O三种元素的第一电离能由大到小的顺序为___________ 。
②{Cr[OC(NH2)2]6}3+中存在的化学键有___________ (填标号)
A.极性共价键 B.非极性共价键 C.氢键
D.配位键 E.金属键 F.离子键
(3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图所示。
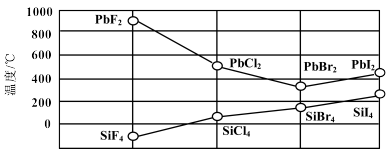
①SiX4的沸点依F、Cl、 Br、I次序升高的原因是_____ 。
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性___________ 、共价性___________ 。(填“增强”、“减弱”或“不变”)。
(4)丁二酮肟常与Ni2+形成图A所示的配合物,图B是硫代氧的结果:
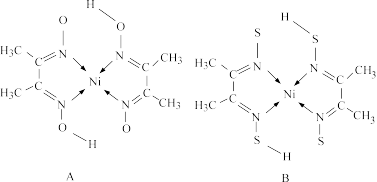
A的熔、沸点高于B的原因为___________ 。
(5)某FexNy的晶胞如图1所示。Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为_____ 。

(1)Cr基态原子价电子的轨道表示式
(2)氮化铬(CrN)在超级电容器领域具有良好的应用前景,可由CrCl3·6H2O与尿素[(NH2)2CO]反应先得到配合物{Cr[OC(NH2)2]6}Cl3,然后在通有NH3和N2混合气体的反应炉内热分解制得。
①尿素中C、N、O三种元素的第一电离能由大到小的顺序为
②{Cr[OC(NH2)2]6}3+中存在的化学键有
A.极性共价键 B.非极性共价键 C.氢键
D.配位键 E.金属键 F.离子键
(3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图所示。

①SiX4的沸点依F、Cl、 Br、I次序升高的原因是
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性
(4)丁二酮肟常与Ni2+形成图A所示的配合物,图B是硫代氧的结果:

A的熔、沸点高于B的原因为
(5)某FexNy的晶胞如图1所示。Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为

您最近一年使用:0次
【推荐1】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能_______ (填“<”“>”或“=”)B元素的第一电离能,A、B、C三种元素的电负性由小到大的顺序为________ (用元素符号表示)。
(2)D元素原子的价电子排布式是________ 。
(3)C元素的电子排布图为_________ ;E3+的离子符号为__________ 。
(4)F元素位于元素周期表的______ 区,其基态原子的电子排布式为_______ 。
(5)G元素可能的性质有________ 。
A.其最高价氧化物是分子晶体 B.其电负性大于磷 C.其原子半径大于锗 D.其第一电离能小于硒
(6)用氢键表示式写出C的氢化物水溶液中存在的所有氢键:_________ 。已知F的最高价氧化物对应水化物能溶于氨水且生成一种配合物阳离子,写出该反应的离子方程式____ 。
(1)A元素的第一电离能
(2)D元素原子的价电子排布式是
(3)C元素的电子排布图为
(4)F元素位于元素周期表的
(5)G元素可能的性质有
A.其最高价氧化物是分子晶体 B.其电负性大于磷 C.其原子半径大于锗 D.其第一电离能小于硒
(6)用氢键表示式写出C的氢化物水溶液中存在的所有氢键:
您最近一年使用:0次
【推荐2】完成下列填空
(1)某元素基态原子电子排布式为[Ar]3d104s24p1,该元素处于周期表第___________ 周期,第___________ 族,位于___________ 区。
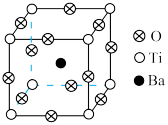
(2)钛酸钡是一种典型钙钛矿型结构晶体,其晶胞如图,写出其化学式:___________ 。
(3)图表法、图像法是常用的科学研究方法。短周期某主族元素M的电离能情况如图A所示。则M元素位于周期表的第___________ 族。图B是研究部分主族元素的氢化物的沸点变化规律的图像,折线c可以表达出第___________ 族元素氢化物的沸点的变化规律。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线,折线a和折线b,你认为正确的是___________ (填“a”或“b”),理由是___________ 。

(1)某元素基态原子电子排布式为[Ar]3d104s24p1,该元素处于周期表第
(2)钛酸钡是一种典型钙钛矿型结构晶体,其晶胞如图,写出其化学式:

(3)图表法、图像法是常用的科学研究方法。短周期某主族元素M的电离能情况如图A所示。则M元素位于周期表的第

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为长式周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)写出元素⑩的一价离子的核外电子排布式:_______ 该元素属于_______ 区元素。
(2)在标号的主族元素中,电负性最大的是_______ (填元素符号,下同),第一电离能最小的是_______ 。
(3)元素④⑥⑦的气态氢化物热稳定性由强到弱的顺序为:_______ (填化学式)。
(4)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式_______ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑨ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑩ |
(1)写出元素⑩的一价离子的核外电子排布式:
(2)在标号的主族元素中,电负性最大的是
(3)元素④⑥⑦的气态氢化物热稳定性由强到弱的顺序为:
(4)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】我国科学家研究的第五代甲醇生产技术被誉为“液态阳光”,该技术中水经过太阳能光解制得氢气,再利用二氧化碳催化加氢合成甲醇。回答下列问题:
(1)硫化氢分子和水分子结构相似,但冰中水分子周围紧邻的分子数(4个)远小于硫化氢的(12个),原因是____ 。
(2)二氧化碳是重要的碳源,1molCO2分子中存在____ 个π键,碳在成键时,能将一个2s电子激发进入2p能级而参与成键,写出该激发态原子的核外电子排布式:____ 。基态氧原子有_____ 种不同形状的电子云。
(3)磷化硼纳米颗粒可以作为CO2合成甲醇时的非金属电催化剂,磷化硼硬度极大,在数千摄氏度高温时也较稳定,其立方晶胞结构如图所示。回答下列问题:

①晶胞中含有的P原子与B原子的个数比为____ ,晶体中与P原子距离最近且相等的P原子数为____ 。
②已知阿伏加德罗常数的值为NA,磷化硼的晶胞参数为apm,磷化硼晶体的密度ρ=____ g·cm-3。
(1)硫化氢分子和水分子结构相似,但冰中水分子周围紧邻的分子数(4个)远小于硫化氢的(12个),原因是
(2)二氧化碳是重要的碳源,1molCO2分子中存在
(3)磷化硼纳米颗粒可以作为CO2合成甲醇时的非金属电催化剂,磷化硼硬度极大,在数千摄氏度高温时也较稳定,其立方晶胞结构如图所示。回答下列问题:

①晶胞中含有的P原子与B原子的个数比为
②已知阿伏加德罗常数的值为NA,磷化硼的晶胞参数为apm,磷化硼晶体的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.下列说法正确的是__________ 。
A.元素的电负性越大,其单质越稳定
B.分子晶体中可能不存在共价键
C.晶格能越大,形成的离子晶体越稳定
D.金属晶体和离子晶体均具有延展性
Ⅱ.钢铁中含有C、N、Mn等元素,实验中常用过硫酸盐氧化法测定钢铁中锰的含量,反应原理为2Mn2++5S2O82-+8H2O 2MnO4-+10SO42-+16H+
2MnO4-+10SO42-+16H+
(1)Mn原子的价层电子的轨道表达式(电子排布图)为____________________ 。
(2)已知H2S2O8的结构简式如图所示。
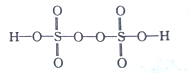
①H2S2O8中S的轨道杂化方式为______________ ,H、O、S三种元素中,电负性最大的元素是___________ (填元素符号)。
②S基态原子中电子的运动状态有_________ 种。
③上述反应中S2O82-断裂的共价键类型为___________ (填“σ键”或“π键”) ,每生成1mol MnO4-,断裂的共价键数目为___________ NA。
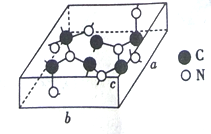
(3)C和N能形成多种结构的晶体。一种新型的超硬材料类似于金刚石的结构,但硬度比金刚石大,其晶胞如图所示(图示原子都包含在晶胞内),其化学式为______________ 。已知晶胞参数a=0.64nm,b=0.55nm,c=0.24nm,则该晶体的密度为_______________ (列出式子即可,但式子中不包含字母)g/cm3。
A.元素的电负性越大,其单质越稳定
B.分子晶体中可能不存在共价键
C.晶格能越大,形成的离子晶体越稳定
D.金属晶体和离子晶体均具有延展性
Ⅱ.钢铁中含有C、N、Mn等元素,实验中常用过硫酸盐氧化法测定钢铁中锰的含量,反应原理为2Mn2++5S2O82-+8H2O
 2MnO4-+10SO42-+16H+
2MnO4-+10SO42-+16H+(1)Mn原子的价层电子的轨道表达式(电子排布图)为
(2)已知H2S2O8的结构简式如图所示。

①H2S2O8中S的轨道杂化方式为
②S基态原子中电子的运动状态有
③上述反应中S2O82-断裂的共价键类型为

(3)C和N能形成多种结构的晶体。一种新型的超硬材料类似于金刚石的结构,但硬度比金刚石大,其晶胞如图所示(图示原子都包含在晶胞内),其化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的阴离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物中Q的杂化类型为___ ,分子中含有____ 个σ键,____ 个π键。
(2)R的氢化物分子的立体构型是____ ,R与X形成的化合物可作为一种重要的陶瓷材料,其化学式是____ 。
(3)X的常见氢化物的立体构型是____ ;键角___ ;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是____ 。
(4)Q分别与Y、Z形成的共价化合物的化学式是____ 和____ ;
(1)Q的最高价氧化物中Q的杂化类型为
(2)R的氢化物分子的立体构型是
(3)X的常见氢化物的立体构型是
(4)Q分别与Y、Z形成的共价化合物的化学式是
您最近一年使用:0次



