现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能_______ (填“<”“>”或“=”)B元素的第一电离能,A、B、C三种元素的电负性由小到大的顺序为________ (用元素符号表示)。
(2)D元素原子的价电子排布式是________ 。
(3)C元素的电子排布图为_________ ;E3+的离子符号为__________ 。
(4)F元素位于元素周期表的______ 区,其基态原子的电子排布式为_______ 。
(5)G元素可能的性质有________ 。
A.其最高价氧化物是分子晶体 B.其电负性大于磷 C.其原子半径大于锗 D.其第一电离能小于硒
(6)用氢键表示式写出C的氢化物水溶液中存在的所有氢键:_________ 。已知F的最高价氧化物对应水化物能溶于氨水且生成一种配合物阳离子,写出该反应的离子方程式____ 。
(1)A元素的第一电离能
(2)D元素原子的价电子排布式是
(3)C元素的电子排布图为
(4)F元素位于元素周期表的
(5)G元素可能的性质有
A.其最高价氧化物是分子晶体 B.其电负性大于磷 C.其原子半径大于锗 D.其第一电离能小于硒
(6)用氢键表示式写出C的氢化物水溶液中存在的所有氢键:
更新时间:2020-10-20 12:57:54
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】二氧化钛是钛的重要化合物,钛白(纯净的二氧化钛)是一种折射率高、着色力和遮盖力强、化学性质稳定的白色颜料。钛精矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有Fe2O3、SiO2等杂质,由钛精矿制取一氧化钛,常用硫酸法,其流程如下:

(1)基态22Ti原子的价电子排布式为___________ 。
(2)钛精矿主要成分与硫酸反应的主要产物是TiOSO4和FeSO4,该反应的化学方程式为___________ 。
(3)矿渣主要成分___________ ,试剂X为___________ (填化学式)。
(4)为了从溶液I中获取纯净的FeSO4·7H2O,应采取的操作是___________ 、___________ 、过滤、洗涤、干燥。
(5)用氧化还原滴定法测定制备得到的中间产品中TiO2的质量分数:在一定条件下,将一定量的产品溶解并将TiO2还原为Ti3+,再以KSCN溶液作为指示剂,用硫酸铁铵 [NH4Fe(SO4)2]标准溶液滴定Ti3+至全部生成Ti4+。
①滴定终点的现象是:加入最后半滴标准液时,___________ 。
②滴定分析时,称取TiO2试样0.2g,消耗0.1mol/L[NH4Fe(SO4)2]标准溶液24.00mL,则TiO2的质量分数为(计算结果保留小数点后一位)___________ 。

(1)基态22Ti原子的价电子排布式为
(2)钛精矿主要成分与硫酸反应的主要产物是TiOSO4和FeSO4,该反应的化学方程式为
(3)矿渣主要成分
(4)为了从溶液I中获取纯净的FeSO4·7H2O,应采取的操作是
(5)用氧化还原滴定法测定制备得到的中间产品中TiO2的质量分数:在一定条件下,将一定量的产品溶解并将TiO2还原为Ti3+,再以KSCN溶液作为指示剂,用硫酸铁铵 [NH4Fe(SO4)2]标准溶液滴定Ti3+至全部生成Ti4+。
①滴定终点的现象是:加入最后半滴标准液时,
②滴定分析时,称取TiO2试样0.2g,消耗0.1mol/L[NH4Fe(SO4)2]标准溶液24.00mL,则TiO2的质量分数为(计算结果保留小数点后一位)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钛酸钡具有优良的介电、压电特性,主要用于电容器、自动温控等领域。
(1)基态钛原子的电子排布式为_______ 。
(2)钡元素在自然界中主要以重晶石形式存在,其成分为 ,
, 的空间构型为
的空间构型为_______ 。
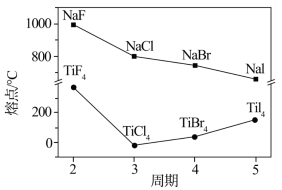
(3)卤化钠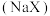 和四卤化钛
和四卤化钛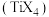 的熔点如图所示,已知
的熔点如图所示,已知 是离子晶体与
是离子晶体与 、
、 、
、 晶体类型不同,下列判断不正确的是_______(选填字母序号)。
晶体类型不同,下列判断不正确的是_______(选填字母序号)。
(4)钛酸钡的晶胞结构如图所示,在该晶胞结构中,钡离子、钛离子、氧离子的个数比为_______ ,该物质的化学式为_______ ;晶体中每个钛离子周围与其距离最近且相等的氧离子的数量是_______ ;其晶胞参数约为 ,钛酸钡晶体的密度
,钛酸钡晶体的密度
_______  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示)。
的代数式表示)。
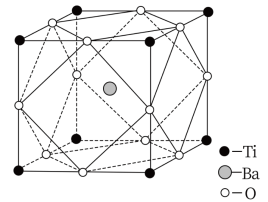
(1)基态钛原子的电子排布式为
(2)钡元素在自然界中主要以重晶石形式存在,其成分为
 ,
, 的空间构型为
的空间构型为(3)卤化钠
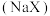 和四卤化钛
和四卤化钛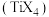 的熔点如图所示,已知
的熔点如图所示,已知 是离子晶体与
是离子晶体与 、
、 、
、 晶体类型不同,下列判断不正确的是_______(选填字母序号)。
晶体类型不同,下列判断不正确的是_______(选填字母序号)。
A. 为离子晶体 为离子晶体 |
B. 的熔点反常升高是因为分子间存在氢键 的熔点反常升高是因为分子间存在氢键 |
C.随X半径的增大, 的离子键减弱,熔点逐渐降低 的离子键减弱,熔点逐渐降低 |
D. 、 、 、 、 的相对分子质量依次增大,分子间作用力增大,熔点逐渐升高 的相对分子质量依次增大,分子间作用力增大,熔点逐渐升高 |
 ,钛酸钡晶体的密度
,钛酸钡晶体的密度
 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】磷酸铁锂( )被认为是最有前途的锂离子电池正极材料。某企业利用富铁浸出液生成磷酸铁锂,开辟了处理硫酸亚铁废液一条新途径。其主要流程如下:
)被认为是最有前途的锂离子电池正极材料。某企业利用富铁浸出液生成磷酸铁锂,开辟了处理硫酸亚铁废液一条新途径。其主要流程如下:

已知: 是种难溶于水的物质。
是种难溶于水的物质。
(1)基态 原子的单电子数目为
原子的单电子数目为___________ 。
(2)钛铁矿用浓硫酸处理之前,需要粉碎,其目的是___________ 。
(3) 水解生成
水解生成 的离子方程式为
的离子方程式为___________ 。
(4)加入 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(5)为测定钛铁矿中铁的含量,某同学取经浓硫酸等处理的溶液(此时钛铁矿中的铁已全部转化为二价铁离子),采取 标准液滴定
标准液滴定 的方法:(不考虑
的方法:(不考虑 与其他物质反应)在滴定过程中,若未用标准液润洗滴定管,则使测定结果
与其他物质反应)在滴定过程中,若未用标准液润洗滴定管,则使测定结果___________ (填“偏高”、“偏低”或“无影响”),滴定终点的现象是___________ 。滴定分析时,称取ag钛铁矿,处理后,用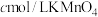 标准液滴定,消耗VmL,则铁元素的质量分数的表达式为
标准液滴定,消耗VmL,则铁元素的质量分数的表达式为___________ 。
 )被认为是最有前途的锂离子电池正极材料。某企业利用富铁浸出液生成磷酸铁锂,开辟了处理硫酸亚铁废液一条新途径。其主要流程如下:
)被认为是最有前途的锂离子电池正极材料。某企业利用富铁浸出液生成磷酸铁锂,开辟了处理硫酸亚铁废液一条新途径。其主要流程如下:
已知:
 是种难溶于水的物质。
是种难溶于水的物质。(1)基态
 原子的单电子数目为
原子的单电子数目为(2)钛铁矿用浓硫酸处理之前,需要粉碎,其目的是
(3)
 水解生成
水解生成 的离子方程式为
的离子方程式为(4)加入
 发生反应的离子方程式为
发生反应的离子方程式为(5)为测定钛铁矿中铁的含量,某同学取经浓硫酸等处理的溶液(此时钛铁矿中的铁已全部转化为二价铁离子),采取
 标准液滴定
标准液滴定 的方法:(不考虑
的方法:(不考虑 与其他物质反应)在滴定过程中,若未用标准液润洗滴定管,则使测定结果
与其他物质反应)在滴定过程中,若未用标准液润洗滴定管,则使测定结果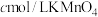 标准液滴定,消耗VmL,则铁元素的质量分数的表达式为
标准液滴定,消耗VmL,则铁元素的质量分数的表达式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为______________ 。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_______ Ⅰ1(Cu)(填“大于”或“小于”)。原因是_____________ 。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是________ ;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是______________ 。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为____ ,C原子的杂化形式为______ 。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______ 。

(1)Zn原子核外电子排布式为
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E是前四周期的元素。A、B、C同周期,C、D同主族且原子半径C>D,A的原子结构示意图为 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
(1)写出下列元素的符号:A___________ ,D___________ 。
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是___________ ,碱性最强的是___________ 。
(3) E原子价电子排布式是___________ ,E元素在___________ 区。
(4)写出D元素原子构成单质的电子式___________ 。
 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3) E原子价电子排布式是
(4)写出D元素原子构成单质的电子式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】太阳能电池可分为:硅太阳能电池,化合物太阳能电池,如砷化镓(GaAs)、铜铟镓硒(CIGS)、硫化镉(CdS),功能高分子太阳能电池等,Al-Ni常作电极。据此回答问题:
(1)镍(Ni)在周期表中的位置为______ ;S原子的价电子排布式为________ ;Ga、As和Se的第一电离能由大到小的顺序是________ 。
(2)Na3As3中As原子的杂化方式为_____ ;AsCl3的空间构型为____ 。
(3)GaAs熔点为1238℃,GaN熔点约为1500°,GaAs熔点低于GaN的原因为__________ 。
(4)写出一种与SO42-互为等电子体的分子_________ 。
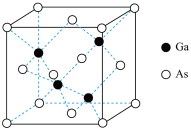
(5)GaAs的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为_____ 。已知GaAs的密度为ρg/cm3,Ga和As的摩尔质量分别为 MGa g/mol和MAsg/mol,则GaAs晶胞中Ga之间的最短距离为________ pm。
(1)镍(Ni)在周期表中的位置为
(2)Na3As3中As原子的杂化方式为
(3)GaAs熔点为1238℃,GaN熔点约为1500°,GaAs熔点低于GaN的原因为
(4)写出一种与SO42-互为等电子体的分子
(5)GaAs的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】近年来中国航天事业快速发展,其中我国自主研制的高性能碳化硅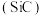 增强铝基复合材料发挥了重要作用。回答下列问题:
增强铝基复合材料发挥了重要作用。回答下列问题:
(1)基态 原子的价电子排布图为
原子的价电子排布图为___________ , 三种元素电负性由大到小的顺序为
三种元素电负性由大到小的顺序为___________ 。
(2)下列状态的铝原子或离子,电离失去最外层一个电子所需能量最大的是___________ 。
a.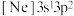 b.
b. c.
c.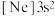 d.
d.
(3)三乙基铝[ ;结构简式:
;结构简式: ;熔点:
;熔点: ]是一种金属有机物,可做火箭燃料。三乙基铝的晶体类型为
]是一种金属有机物,可做火箭燃料。三乙基铝的晶体类型为___________ ,三乙基铝中铝原子的价电子对数为___________ 。
(4)碳化硅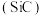 也叫金刚砂,其晶胞结构如图所示,
也叫金刚砂,其晶胞结构如图所示,

①晶体中 原子的杂化方式为
原子的杂化方式为___________ 。
②碳化硅晶体的熔点比金刚石___________ (选填“高”或“低”),原因是___________ 。
③若晶体的晶胞参数为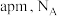 为阿伏加德罗常数的值,则晶体的摩尔体积为
为阿伏加德罗常数的值,则晶体的摩尔体积为___________  (用含
(用含 和
和 的式子表示)。
的式子表示)。
 增强铝基复合材料发挥了重要作用。回答下列问题:
增强铝基复合材料发挥了重要作用。回答下列问题:(1)基态
 原子的价电子排布图为
原子的价电子排布图为 三种元素电负性由大到小的顺序为
三种元素电负性由大到小的顺序为(2)下列状态的铝原子或离子,电离失去最外层一个电子所需能量最大的是
a.
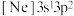 b.
b. c.
c.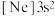 d.
d.
(3)三乙基铝[
 ;结构简式:
;结构简式: ;熔点:
;熔点: ]是一种金属有机物,可做火箭燃料。三乙基铝的晶体类型为
]是一种金属有机物,可做火箭燃料。三乙基铝的晶体类型为(4)碳化硅
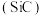 也叫金刚砂,其晶胞结构如图所示,
也叫金刚砂,其晶胞结构如图所示,
①晶体中
 原子的杂化方式为
原子的杂化方式为②碳化硅晶体的熔点比金刚石
③若晶体的晶胞参数为
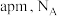 为阿伏加德罗常数的值,则晶体的摩尔体积为
为阿伏加德罗常数的值,则晶体的摩尔体积为 (用含
(用含 和
和 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】2022年北京冬季奥运会场馆使用了大量不锈钢材质,不锈钢属于合金钢,其基体是铁碳合金,常用的不锈钢中含铬(Cr)18%、含镍(Ni)8%。回答下列问题:
(1)石墨烯(即单层石墨)是一种由碳原子构成的单层二维蜂窝状晶格结构的新材料,其中碳原子采取___________ 杂化。
(2) 蒸气状态下以双聚分子形式存在(如图),其中Fe的配位数为
蒸气状态下以双聚分子形式存在(如图),其中Fe的配位数为___________ ,双聚分子中存在配位键,提供空轨道的是___________ (填元素符号)原子。

(3)甘氨酸亚铁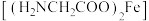 中非金属元素的电负性由大到小的顺序是
中非金属元素的电负性由大到小的顺序是___________ 。甘氨酸(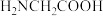 )比其同分异构体硝基乙烷(
)比其同分异构体硝基乙烷(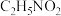 )熔沸点高,其原因是
)熔沸点高,其原因是___________ 。
(4) 的阴离子的空间构型为
的阴离子的空间构型为___________ 。
(5)工业上常用羰基镍 制备高纯镍,其熔点-19℃,沸点43℃,羰基镍属于
制备高纯镍,其熔点-19℃,沸点43℃,羰基镍属于___________ (填晶体类型),该晶体中 键与
键与 键数目之比为
键数目之比为___________ 。
(6)金属铬属于体心立方晶体(如图),已知其密度为 ,则晶体中铬原子的半径为
,则晶体中铬原子的半径为___________ cm(阿伏加德罗常数的值为 ,列出表达式)。
,列出表达式)。

(1)石墨烯(即单层石墨)是一种由碳原子构成的单层二维蜂窝状晶格结构的新材料,其中碳原子采取
(2)
 蒸气状态下以双聚分子形式存在(如图),其中Fe的配位数为
蒸气状态下以双聚分子形式存在(如图),其中Fe的配位数为
(3)甘氨酸亚铁
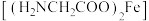 中非金属元素的电负性由大到小的顺序是
中非金属元素的电负性由大到小的顺序是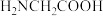 )比其同分异构体硝基乙烷(
)比其同分异构体硝基乙烷(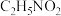 )熔沸点高,其原因是
)熔沸点高,其原因是(4)
 的阴离子的空间构型为
的阴离子的空间构型为(5)工业上常用羰基镍
 制备高纯镍,其熔点-19℃,沸点43℃,羰基镍属于
制备高纯镍,其熔点-19℃,沸点43℃,羰基镍属于 键与
键与 键数目之比为
键数目之比为(6)金属铬属于体心立方晶体(如图),已知其密度为
 ,则晶体中铬原子的半径为
,则晶体中铬原子的半径为 ,列出表达式)。
,列出表达式)。
您最近一年使用:0次
【推荐3】依据原子结构知识回答下列问题。
(1)下列说法错误的是_______ 。
A.电负性:Si<H<C<N
B.离子半径: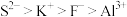
C.原子的未成对电子数: Cr>Mn>Si>Br
D.第二周期中元素原子的第一电离能介于B和N之间的元素有2种
E.前四周期元素中,基态原子中价电子数与其所在周期数相同的元素有4种
(2)基态S原子的价电子轨道表示式为_______ ,其电子占据的最高能层符号为_______ ,其价电子中两种自旋状态的电子数之比为_______ 。
(3)基态F原子核外电子的空间运动状态有_______ 种。下列属于F原子激发态的电子排布式是_______ (填标号,下同),其中能量较高的是_______ 。
A.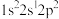 b.
b. c.
c. d.
d.
(4)Cr元素位于元素周期表_______ 区。Cr与Mn相比,第二电离能与第一电离能差值更大的是_______ ,原因是_______ 。
(1)下列说法错误的是
A.电负性:Si<H<C<N
B.离子半径:
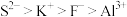
C.原子的未成对电子数: Cr>Mn>Si>Br
D.第二周期中元素原子的第一电离能介于B和N之间的元素有2种
E.前四周期元素中,基态原子中价电子数与其所在周期数相同的元素有4种
(2)基态S原子的价电子轨道表示式为
(3)基态F原子核外电子的空间运动状态有
A.
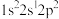 b.
b. c.
c. d.
d.
(4)Cr元素位于元素周期表
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某小组在做铜与浓硫酸(装置如下图)的反应实验时,发现有如下的反应现象:
 呈黄色,
呈黄色, 呈蓝色,两者混合则成绿色,铜的化合物中
呈蓝色,两者混合则成绿色,铜的化合物中 、
、 、
、 都为黑色,其中
都为黑色,其中 溶于盐酸;
溶于盐酸; 、
、 不溶于稀盐酸,但溶于浓盐酸。
不溶于稀盐酸,但溶于浓盐酸。
(1)铜丝与浓硫酸反应的化学方程式为___________ 。
(2)试管中品红溶液褪色,体现 的
的___________ 性,浸 溶液的棉团作用是
溶液的棉团作用是___________ 。
(3)甲组同学对实验中形成的墨绿色溶液进行探究,特进行下列实验:
请解释形成墨绿色的原因:___________ 。
(4)乙组同学对白雾的成分经检验为 ,请设计实验证明该白雾为硫酸:
,请设计实验证明该白雾为硫酸:___________ 。
(5)丙组同学进一步对灰白色沉淀通过加水溶解、过滤,最后沉淀为黑色,取其黑色沉淀,进行成分探究:滴加适量稀盐酸,则发现黑色沉淀几乎不溶解,溶液也不变蓝,则说明黑色沉淀中不含有___________ 。滴加适量浓盐酸,振荡,加热,观察到黑色沉淀几乎完全溶解,生成呈略黄色的 。写出
。写出 与浓盐酸反应的离子方程式:
与浓盐酸反应的离子方程式:___________ 。
(6)某工厂将热空气通入稀硫酸中来溶解废铜屑制备 ,消耗含铜元素80%的废铜屑240kg固体时,得到500kg产品,产率为
,消耗含铜元素80%的废铜屑240kg固体时,得到500kg产品,产率为___________ (结果保留两位小数)。
| 序号 | 操作 | 现象 |
| ① | 加热 | 铜丝表面变黑 |
| ② | 继续加热 | 有大量气泡产生,溶液变为墨绿色浊液,试管底部开始有灰白色沉淀生成。品红溶液褪色。 |
| ③ | 再加热 | 试管中出现“白雾”,浊液逐渐变为澄清,溶液颜色慢慢变为浅蓝色,试管底部灰白色沉淀增多 |
| ④ | 冷却,将灰白色固体倒入水中 | 形成蓝色溶液 |
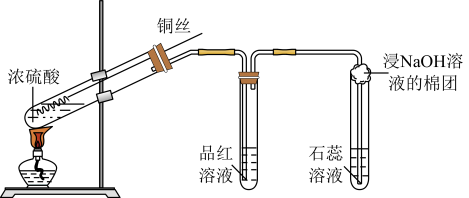
 呈黄色,
呈黄色, 呈蓝色,两者混合则成绿色,铜的化合物中
呈蓝色,两者混合则成绿色,铜的化合物中 、
、 、
、 都为黑色,其中
都为黑色,其中 溶于盐酸;
溶于盐酸; 、
、 不溶于稀盐酸,但溶于浓盐酸。
不溶于稀盐酸,但溶于浓盐酸。(1)铜丝与浓硫酸反应的化学方程式为
(2)试管中品红溶液褪色,体现
 的
的 溶液的棉团作用是
溶液的棉团作用是(3)甲组同学对实验中形成的墨绿色溶液进行探究,特进行下列实验:
| 操作 | 现象 | |
| Ⅰ组 | 直接取其铜丝(表面有聚氯乙烯薄膜)做实验 | 溶液变成墨绿色 |
| Ⅱ组 | 实验前,先将铜丝进行灼烧处理 | 溶液变蓝 |
(4)乙组同学对白雾的成分经检验为
 ,请设计实验证明该白雾为硫酸:
,请设计实验证明该白雾为硫酸:(5)丙组同学进一步对灰白色沉淀通过加水溶解、过滤,最后沉淀为黑色,取其黑色沉淀,进行成分探究:滴加适量稀盐酸,则发现黑色沉淀几乎不溶解,溶液也不变蓝,则说明黑色沉淀中不含有
 。写出
。写出 与浓盐酸反应的离子方程式:
与浓盐酸反应的离子方程式:(6)某工厂将热空气通入稀硫酸中来溶解废铜屑制备
 ,消耗含铜元素80%的废铜屑240kg固体时,得到500kg产品,产率为
,消耗含铜元素80%的废铜屑240kg固体时,得到500kg产品,产率为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
Ⅰ.1—乙基—3—甲基咪唑四氟硼酸盐离子液体稳定性强,可溶于水,可广泛用于有机反应,结构如图。
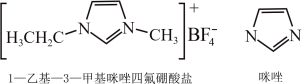
(1)有关1—乙基—3—甲基咪唑四氟硼酸盐说法正确的 。
(2)咪唑具有类似苯的平面结构(如图所示),其大π键应表示为______________ 。
Ⅱ.国际权威学术期刊《自然》最近报道,我国科学家选择碲化锆(ZrTes)和砷化镉(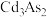 )为材料验证了三维量子霍尔效应。
)为材料验证了三维量子霍尔效应。
(3)Zr是Ti的同族相邻元素,位于周期表的__________ 区。
Ⅲ. 与
与 可形成配离子
可形成配离子 。
。
(4)该离子中不含的化学键类型有__________ (填字母)。
A.离子键 B.配位键 C. 键 D.共价键
键 D.共价键
E. 键 F.氢键
键 F.氢键
(5)已知该离子中2个 被2个
被2个 替代只得到一种结构,则该离子的立体构型为
替代只得到一种结构,则该离子的立体构型为__________ 。
Ⅳ.硫酸氧钛(Ti)是一种优良的催化剂,其阳离子为如图所示链状聚合形式的离子,聚合度为n。
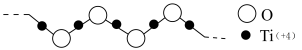
(6)该阳离子的化学式为__________ 。
Ⅰ.1—乙基—3—甲基咪唑四氟硼酸盐离子液体稳定性强,可溶于水,可广泛用于有机反应,结构如图。

(1)有关1—乙基—3—甲基咪唑四氟硼酸盐说法正确的 。
| A.该结构中存在手性碳原子 |
B.该物质相较 摩尔质量更大,具有更高的熔沸点 摩尔质量更大,具有更高的熔沸点 |
C. 中含有配位键,B原子为 中含有配位键,B原子为 杂化 杂化 |
| D.该物质是离子化合物,固态时能导电 |
(2)咪唑具有类似苯的平面结构(如图所示),其大π键应表示为
Ⅱ.国际权威学术期刊《自然》最近报道,我国科学家选择碲化锆(ZrTes)和砷化镉(
 )为材料验证了三维量子霍尔效应。
)为材料验证了三维量子霍尔效应。(3)Zr是Ti的同族相邻元素,位于周期表的
Ⅲ.
 与
与 可形成配离子
可形成配离子 。
。(4)该离子中不含的化学键类型有
A.离子键 B.配位键 C.
 键 D.共价键
键 D.共价键E.
 键 F.氢键
键 F.氢键(5)已知该离子中2个
 被2个
被2个 替代只得到一种结构,则该离子的立体构型为
替代只得到一种结构,则该离子的立体构型为Ⅳ.硫酸氧钛(Ti)是一种优良的催化剂,其阳离子为如图所示链状聚合形式的离子,聚合度为n。

(6)该阳离子的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组探究氨水与硫酸铜反应的实验现象,做了如下实验:操作步骤及实验现象如下表。回答下列相关问题:
经查资料:①深蓝色透明溶液及深蓝色晶体中,深蓝色都是由于存在
② 结构为平面四边形
结构为平面四边形
③深蓝色晶体是
(1)配离子 中中心离子的核外电子占据最高能级为
中中心离子的核外电子占据最高能级为___________ 。
(2)配离子 中
中 采取的杂化类型为
采取的杂化类型为___________ ,配体中N采取的杂化类型为___________ (填标号)。
A. B.
B. C.
C. D.
D.
(3) 中
中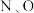 的第一电离能N
的第一电离能N___________ O(填“>”,“<”或“=”),基态 比
比 稳定的原因是
稳定的原因是___________ 。
(4)操作2涉及的离子方程式为___________ 。
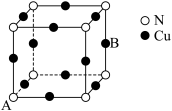
(5)N和Cu形成的化合物的晶胞结构如图所示,若 为阿伏加德罗常数。若该晶胞的边长为apm,则该晶体的密度是
为阿伏加德罗常数。若该晶胞的边长为apm,则该晶体的密度是___________  。
。
| 操作步骤 | 实验现象 |
操作1:向盛有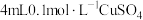 溶液的试管里滴加几滴1mol/L氨水; 溶液的试管里滴加几滴1mol/L氨水; | 形成难溶物; |
| 操作2:继续滴加氨水并振荡试管: | 难溶物溶解,得到深蓝色透明溶液; |
| 操作3:再向试管中加入极性小的溶剂(如8mL95%的乙醇) | 析出深蓝色的晶体。 |

②
 结构为平面四边形
结构为平面四边形③深蓝色晶体是

(1)配离子
 中中心离子的核外电子占据最高能级为
中中心离子的核外电子占据最高能级为(2)配离子
 中
中 采取的杂化类型为
采取的杂化类型为A.
 B.
B. C.
C. D.
D.
(3)
 中
中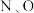 的第一电离能N
的第一电离能N 比
比 稳定的原因是
稳定的原因是(4)操作2涉及的离子方程式为
(5)N和Cu形成的化合物的晶胞结构如图所示,若
 为阿伏加德罗常数。若该晶胞的边长为apm,则该晶体的密度是
为阿伏加德罗常数。若该晶胞的边长为apm,则该晶体的密度是 。
。
您最近一年使用:0次



