张亭栋研究小组受民间中医启发,发现As2O3(俗称砒霜)对白血病有明显的治疗作用。氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)NH3的沸点比PH3_____ (填“高"或“低”),原因是_____________ 。
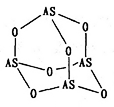
(2)Na3AsO4中含有的化学键类型包括_______ ;AsO43-的空间构型为_______ ,As4O6的分子结构如图所示,则在该化合物中As的杂化方式是_________ 。
(3)自然固氮现象发生的一系列化学变化:N2→NO→NO2→HNO3→NO3-解释了民谚“雷雨发庄稼”的原理。
①NO3-中N原子采取_____ 杂化方式,其空间构型为________ ,写出它的一种等电子体的化学式________ 。
②已知酸性:HNO3>HNO2,下列相关见解合理的是_________ 。
A.含氧酸中氧原子总数越多,酸性越强
B.同种元素化合价越高,对应含氧酸的酸性越强
C.HNO3中氮元素的正电性更高,在水溶液中更易电离出H+,酸性强于HNO2
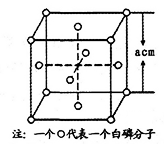
(4)白磷(P4)的晶体属于分子晶体,其晶胞结构如图(小圆圈表示白磷分子)。已知晶胞的边长为acm,阿伏伽德罗常数为NAmol-1,则该晶胞中含有的P原子的个数为______ ,该晶体的密度为______ g·cm-3(用含NA、a的式子表示)。
(1)NH3的沸点比PH3
(2)Na3AsO4中含有的化学键类型包括

(3)自然固氮现象发生的一系列化学变化:N2→NO→NO2→HNO3→NO3-解释了民谚“雷雨发庄稼”的原理。
①NO3-中N原子采取
②已知酸性:HNO3>HNO2,下列相关见解合理的是
A.含氧酸中氧原子总数越多,酸性越强
B.同种元素化合价越高,对应含氧酸的酸性越强
C.HNO3中氮元素的正电性更高,在水溶液中更易电离出H+,酸性强于HNO2
(4)白磷(P4)的晶体属于分子晶体,其晶胞结构如图(小圆圈表示白磷分子)。已知晶胞的边长为acm,阿伏伽德罗常数为NAmol-1,则该晶胞中含有的P原子的个数为

更新时间:2018-05-04 16:13:28
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】Ni、Cu能形成多种化合物,比如Ni能与CO形成正四面体形的配合物Ni(CO)4,CuSO4溶于氨水形成[Cu(NH3)4]SO4深蓝色溶液。
(1)Ni基态原子核外电子排布式为______ ;1 mol Ni(CO)4含σ键数目为______ 。
(2)NiCl2·6H2O在SOCl2气流中加热时,生成NiCl2和两种酸性气体,写出该反应的化学方程式:______
(3)[Cu(NH3)4]SO4中的非金属元素H、N、O的电负性由大到小的顺序为______ (用元素符号回答);[Cu(NH3)4]2+中Cu2+与NH3之间形成的化学键为______ ,提供孤电子对的成键原子是______ 。
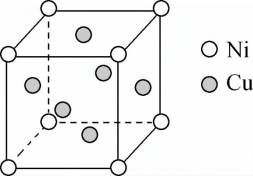
(4)某白铜合金晶胞结构如图所示,晶胞中铜原子与镍原子的个数比为______ 。
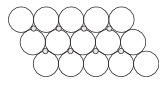
(5)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2−作密置单层排列,Ni2+填充其中。已知O2-的半径为a m,阿伏加德罗常数的值为NA,则每平方米上分散的该晶体的质量为______ g。(写出表达式即可。图中大白球表示O2− ,小黑球表示Ni2+)
(1)Ni基态原子核外电子排布式为
(2)NiCl2·6H2O在SOCl2气流中加热时,生成NiCl2和两种酸性气体,写出该反应的化学方程式:
(3)[Cu(NH3)4]SO4中的非金属元素H、N、O的电负性由大到小的顺序为
(4)某白铜合金晶胞结构如图所示,晶胞中铜原子与镍原子的个数比为

(5)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2−作密置单层排列,Ni2+填充其中。已知O2-的半径为a m,阿伏加德罗常数的值为NA,则每平方米上分散的该晶体的质量为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】镍、铜等金属及其化合物在工农业生产上有重要用途。回答下列问题:
(1)基态Ni的核外电子排布式为___________ ,Ni位于元素周期表中___________ 区(填“s”“p”“d”或“ds”),其核外电子占据的最高能层符号为___________ 。
(2)第二电离能I2(Ni)___________ I2(Cu)(填“<”或“>”),其原因是___________ 。
(3)Ni与CO能形成如图所示的配合物Ni(CO)4,该分子中 键与
键与 键个数比为
键个数比为___________ 。Ni(CO)4易溶于___________ (填标号)。
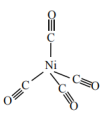
A.水 B.四氯化碳 C.苯 D.稀H2SO4
(4)将Cu粉加入浓氨水中,并通入O2,充分反应后溶液呈深蓝色,该反应的离子方程式为___________ 。
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Ni2+与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有___________ 个,其中提供孤对电子的原子为___________ (写元素符号)。

(1)基态Ni的核外电子排布式为
(2)第二电离能I2(Ni)
(3)Ni与CO能形成如图所示的配合物Ni(CO)4,该分子中
 键与
键与 键个数比为
键个数比为
A.水 B.四氯化碳 C.苯 D.稀H2SO4
(4)将Cu粉加入浓氨水中,并通入O2,充分反应后溶液呈深蓝色,该反应的离子方程式为
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Ni2+与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)基态Li原子的电子排布式为___________ ,其处于元素周期表中的___________ (填“s”、“d”、“ds”或“p”)区。
(2)现有4种元素的基态原子的电子排布式如下:① ;②
;② ;③
;③ ;④
;④ 。则下列比较中,正确的是___________。
。则下列比较中,正确的是___________。
(3)由硅原子核形成的三种微粒,电子排布式分别为:① 、②
、②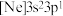 、③
、③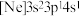 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。
(4)在第四周期元素中,未成对电子数最多的元素是___________ (写元素符号),它的价层电子的轨道表达式___________ 。
(5)Cu与Zn相比,第二电离能与第一电离能差值更大的是___________ (写元素符号),原因是___________ 。
(1)基态Li原子的电子排布式为
(2)现有4种元素的基态原子的电子排布式如下:①
 ;②
;② ;③
;③ ;④
;④ 。则下列比较中,正确的是___________。
。则下列比较中,正确的是___________。| A.第一电离能:④>③>②>① |
| B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① |
| D.最高化合价:④>③=②>① |
 、②
、②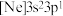 、③
、③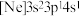 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。| A.微粒半径:③>①>② |
| B.电子排布属于基态原子(或离子)的是:①② |
| C.电离一个电子所需最低能量:①>②>③ |
| D.得电子能力:①>② |
(5)Cu与Zn相比,第二电离能与第一电离能差值更大的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac。请回答下列问题:
(1)C、N、O的电负性由大到小的顺序为________ 。
(2)写出Cu的核外电子排布式________ 。
(3)化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为________ 。
(4)在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为________ ;1mol尿素分子中,σ 键的数目为________ 。
(1)C、N、O的电负性由大到小的顺序为
(2)写出Cu的核外电子排布式
(3)化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为
(4)在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC中化学键为离子键,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且B、C氢化物的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为________________ 。
(2)B的氢化物的分子立体构型是________________ ,中心原子的杂化类型是_______ 。
(3)写出化合物AC2的电子式_______________ 。
(4)E的基态原子核外电子排布式是_________________ ,ECl3形成的配合物的化学式为________ 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是___________________ 。
(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物的分子立体构型是
(3)写出化合物AC2的电子式
(4)E的基态原子核外电子排布式是
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】新版教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素的常见化合价为___________ 。

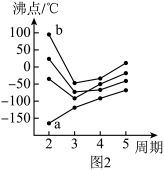
(2)如图2所示,每条折线表示周期表第ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表氢化物的空间结构名称为:___________ 。
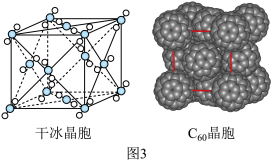
(3) 的晶胞与干冰的晶胞相似(图3),每个
的晶胞与干冰的晶胞相似(图3),每个 分子周围距离最近且相等的
分子周围距离最近且相等的 分子有
分子有___________ 个,构成该晶体微粒间的作用力是___________ 。 晶体的密度为
晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则最近2个
,则最近2个 分子之间的距离d=
分子之间的距离d=___________ pm(用含 、
、 的代数式表示)。
的代数式表示)。
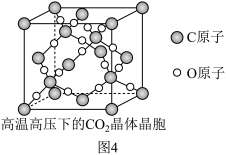
(4) 在高温高压下形成晶体的晶胞(图4)所示,该晶体的类型是
在高温高压下形成晶体的晶胞(图4)所示,该晶体的类型是___________ 。
(5)N元素能形成多种离子,如 、
、 、
、 。
。 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为___________ , 离子空间结构名称为
离子空间结构名称为___________ , 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为___________ 。
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素的常见化合价为

(2)如图2所示,每条折线表示周期表第ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表氢化物的空间结构名称为:

(3)
 的晶胞与干冰的晶胞相似(图3),每个
的晶胞与干冰的晶胞相似(图3),每个 分子周围距离最近且相等的
分子周围距离最近且相等的 分子有
分子有 晶体的密度为
晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则最近2个
,则最近2个 分子之间的距离d=
分子之间的距离d= 、
、 的代数式表示)。
的代数式表示)。
(4)
 在高温高压下形成晶体的晶胞(图4)所示,该晶体的类型是
在高温高压下形成晶体的晶胞(图4)所示,该晶体的类型是
(5)N元素能形成多种离子,如
 、
、 、
、 。
。 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为 离子空间结构名称为
离子空间结构名称为 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】根据晶体的微观结构,试回答有关问题:
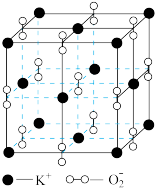
(1)高温下,超氧化钾(KO2)晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。下图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,K+的配位数为_______ ,0价氧原子与-2价氧原子的数目比为_______ 。
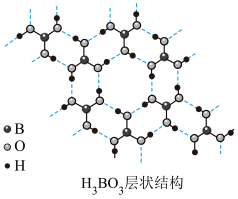
(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的有_______ 。
①硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1 mol H3BO3的晶体中有3 mol氢键
⑤含1 mol H3BO3的晶体中有6 mol极性共价键
(3)确定该合金(如图)的化学式为_____ ,与Fe原子等距离且最短的Fe原子个数为____ ,若晶胞的边长为a nm,此合金的密度为_____ g·cm-3。

(1)高温下,超氧化钾(KO2)晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。下图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,K+的配位数为

(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的有

①硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1 mol H3BO3的晶体中有3 mol氢键
⑤含1 mol H3BO3的晶体中有6 mol极性共价键
(3)确定该合金(如图)的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】铁及其化合物在国民生产、生活中用途广泛。
(1)向FeCl3溶液加入少量的KSCN溶液,生成红色的[Fe(SCN)(H2O)5]2+。N、C、H元素的第一电离能由大到小的顺序为___________ ,O、N、C、H四种元素电负性最大的是___________ (填元素符号) 。
(2)FeCl3 与K4[Fe(CN)6]溶液混合生成Fe4[Fe(CN)6]3沉淀。配体CN-中C原子的杂化方式为___________ ,CH2=CHCH2CN分子中σ键与π键的数目比n(σ)∶n(π)=___________ 。
(3)用邻二氮菲(phen,如图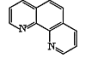 )与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。
)与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。
①[Fe(phen)3]2+中,存在的化学键有___________ (填序号)。
a.配位键 b.离子键 c.π键 d.氢键
②用邻二氮菲测定Fe2+浓度时应控制pH为2~9的适宜范围,请解释原因___________ 。
(4)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。
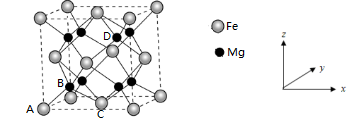
晶体中每个铁原子周围距离最近的镁原子有___________ 个,原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0),B为( ),C为(
),C为(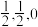 ),则D点坐标参数为
),则D点坐标参数为___________ 。
(1)向FeCl3溶液加入少量的KSCN溶液,生成红色的[Fe(SCN)(H2O)5]2+。N、C、H元素的第一电离能由大到小的顺序为
(2)FeCl3 与K4[Fe(CN)6]溶液混合生成Fe4[Fe(CN)6]3沉淀。配体CN-中C原子的杂化方式为
(3)用邻二氮菲(phen,如图
 )与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。
)与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。①[Fe(phen)3]2+中,存在的化学键有
a.配位键 b.离子键 c.π键 d.氢键
②用邻二氮菲测定Fe2+浓度时应控制pH为2~9的适宜范围,请解释原因
(4)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。

晶体中每个铁原子周围距离最近的镁原子有
 ),C为(
),C为(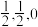 ),则D点坐标参数为
),则D点坐标参数为
您最近一年使用:0次
【推荐3】硼及其化合物在工农业生产、新型材料等方面应用广泛。
(1)区分晶体硼和无定形硼最可靠的科学方法为对固体进行______ ,晶体硼的单质的基本结构单元为正二十面体,能自发呈现多面体外形,这种性质称为晶体的______ 。与硼处于同周期且相邻的两种元素和硼的第一电离能由大到小的顺序为______ 。
(2)硼酸晶体是片层结构,其中一层的结构如图1所示。硼酸在冷水中的溶解度很小,但在热水中较大原因是______ 。

(3)我国著名化学家申泮文教授对硼烷化学的研究开启了无机化学的新篇章。
①最简单的硼烷是B2H6,其分子结构如图2所示,B原子的杂化方式为______ 。

②氨硼烷(NH3BH3)被认为是最具有潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的原子是______ ,写出一种与氨硼烷互为等电子体的分子 ______ (填分子式)。
③硼氢化钠(NaBH4)是一种重要的储氢载体,其阴离子空间构型是______ (填名称)。
(4)砷化硼(BAs)为立方晶系晶体,其结构如图3所示:
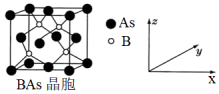
晶胞沿z轴在平面的投影图中,B原子构成的几何形状是______ 。已知:晶体的密度为dg·cm-3, As原子的半径为a pm,假设B、As原子相切,则B原子的半径为______ pm(写出计算表达式即可)。
(1)区分晶体硼和无定形硼最可靠的科学方法为对固体进行
(2)硼酸晶体是片层结构,其中一层的结构如图1所示。硼酸在冷水中的溶解度很小,但在热水中较大原因是

(3)我国著名化学家申泮文教授对硼烷化学的研究开启了无机化学的新篇章。
①最简单的硼烷是B2H6,其分子结构如图2所示,B原子的杂化方式为

②氨硼烷(NH3BH3)被认为是最具有潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的原子是
③硼氢化钠(NaBH4)是一种重要的储氢载体,其阴离子空间构型是
(4)砷化硼(BAs)为立方晶系晶体,其结构如图3所示:

晶胞沿z轴在平面的投影图中,B原子构成的几何形状是
您最近一年使用:0次



