据报道,四川大学某研究所采用近空间升华技术研究碲化镉薄膜太阳能电池,取得了很好的成绩,电池转化效率已经突破13.38%,进入了世界先进行列。回答下列问题:
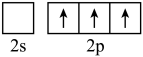
(1)基态碲原子中,价层电子的排布式为______ ;其核外电子占据的最高能级的电子云轮廓图形状为______ .
(2)镉的原子序数为48,它处在元素周期表的______ 区(填s、p、d、ds或f)。
(3)碲和镉中,电负性较大的是______ ;碲酸根离子的空间构型是______ ,其中碲原子的杂化方式为________ .
(4)研制碲化镉太阳能电池的主要工艺流程为:衬底清洗 前电极制备
前电极制备 硫化镉沉积
硫化镉沉积 碲化镉沉积
碲化镉沉积 氯化镉后处理
氯化镉后处理 背电极的制备等。制备过程中涉及的两种物质硫化镉和氯化镉,硫化镉熔点为1750℃,氯化镉熔点为568℃,据此可说明的是
背电极的制备等。制备过程中涉及的两种物质硫化镉和氯化镉,硫化镉熔点为1750℃,氯化镉熔点为568℃,据此可说明的是_______ 。
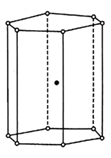
(5)氯化镉晶体的结构如右图所示,图中“。”代表氯原子,“·”代表镉原子,六边形边长为apm,六棱柱高为bpm,则氯化镉晶体的化学式为______ ,晶体密度为______ g/cm3(NA表示阿伏伽德罗常数的值,列出计算式即可)
(1)基态碲原子中,价层电子的排布式为
(2)镉的原子序数为48,它处在元素周期表的
(3)碲和镉中,电负性较大的是
(4)研制碲化镉太阳能电池的主要工艺流程为:衬底清洗
 前电极制备
前电极制备 硫化镉沉积
硫化镉沉积 碲化镉沉积
碲化镉沉积 氯化镉后处理
氯化镉后处理 背电极的制备等。制备过程中涉及的两种物质硫化镉和氯化镉,硫化镉熔点为1750℃,氯化镉熔点为568℃,据此可说明的是
背电极的制备等。制备过程中涉及的两种物质硫化镉和氯化镉,硫化镉熔点为1750℃,氯化镉熔点为568℃,据此可说明的是(5)氯化镉晶体的结构如右图所示,图中“。”代表氯原子,“·”代表镉原子,六边形边长为apm,六棱柱高为bpm,则氯化镉晶体的化学式为

更新时间:2018-05-05 17:37:21
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】能源、材料与生产生活和社会发展密切相关。光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可作太阳能电池材料的有单晶硅、多晶硅、非晶硅、 、
、 、
、 、
、 、
、 等。
等。
(1)写出 原子结构示意图:
原子结构示意图:_______________ 。
(2)P、S、Ga电负性从大到小的顺序为____________________ 。
(3)As元素的第一电离能__________ (填“>”、“<”或“=”)Se元素的第一电离能。
(4)写出原子序数最小的第VIII族元素基态原子的核外电子排布式:_______________ 。
(5)写出3p轨道上只有2个未成对电子的元素的符号:_____________ 、______________ 。
 、
、 、
、 、
、 、
、 等。
等。(1)写出
 原子结构示意图:
原子结构示意图:(2)P、S、Ga电负性从大到小的顺序为
(3)As元素的第一电离能
(4)写出原子序数最小的第VIII族元素基态原子的核外电子排布式:
(5)写出3p轨道上只有2个未成对电子的元素的符号:
您最近一年使用:0次
【推荐2】太阳能的开发利用在新能源研究领域中占据重要地位。单晶硅太阳能电池片在加工时,一般掺杂微量的铜、硼、镓、硒、钛、矾等。回答下列问题:
(1)基态钒原子的电子排布式为___________ ,其中能量最高的电子所占据能级的原子轨道有_________ 个伸展方向。
(2)VO2+与 可形成配合物。
可形成配合物。 中,第二周期元素的第一电离能由大到小的顺序为
中,第二周期元素的第一电离能由大到小的顺序为_________ (用元素符号表示)。
(3)镓与硒相比,电负性更大的是________ (填元素符号)。
(4)已知高温下Cu2O比CuO更稳定,试从铜原子核外电子结构角度解释其原因:________________________________________ 。
(5)与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的有_________ (填元素符号,下同)。
(6)在第二周期元素中,第一电离能介于B和N两元素之间的有_________ 。
(7)硒、硅均能与氢元素形成气态氢化物,若“Si—H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为 Se_________ (填“>”或“<”) Si 。与 Si 同周期的部分元素的电离能如图所示,其中a、b和c分别代表_________ (填字母)。
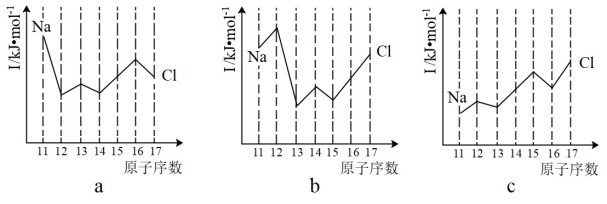
A. a为 ,b为
,b为 ,c为I3 B. a为
,c为I3 B. a为 ,b为
,b为 ,c为
,c为
C. a为 ,b为
,b为 ,c为I1 D. a为
,c为I1 D. a为 ,b为
,b为 ,c为
,c为
(1)基态钒原子的电子排布式为
(2)VO2+与
 可形成配合物。
可形成配合物。 中,第二周期元素的第一电离能由大到小的顺序为
中,第二周期元素的第一电离能由大到小的顺序为(3)镓与硒相比,电负性更大的是
(4)已知高温下Cu2O比CuO更稳定,试从铜原子核外电子结构角度解释其原因:
(5)与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的有
(6)在第二周期元素中,第一电离能介于B和N两元素之间的有
(7)硒、硅均能与氢元素形成气态氢化物,若“Si—H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为 Se

A. a为
 ,b为
,b为 ,c为I3 B. a为
,c为I3 B. a为 ,b为
,b为 ,c为
,c为
C. a为
 ,b为
,b为 ,c为I1 D. a为
,c为I1 D. a为 ,b为
,b为 ,c为
,c为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】磷及其化合物在生产、生活中具有广泛的用途,回答下列问题:
(1)白磷(结构如图1所示)在潮湿的空气中发生缓慢氧化,在40℃左右即可自燃。
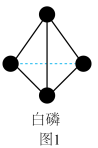
①白磷(P4)的相对分子质量为___________ 。
②基态P原子中成对电子数与未成对电子数之比为___________ 。
③电负性:P___________ (填“>”“<”或“=”)O。
(2)磷,及其部分重要化合物的相互转化如图2所示。
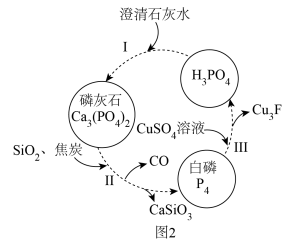
①基态钙原子的简化电子排布式为___________ 。
②第一电离能:Si___________ (填“>”“<”或“=”)C。
③CO2和CO的组成元素相同,但二者的性质不完全相同,其原因为___________ 。
④常温下,H3PO4与少量NaOH溶液反应的化学方程式为___________ 。
(3)反应Ⅲ的离子方程式为___________ (已知:Cu3P不溶于水)。
(1)白磷(结构如图1所示)在潮湿的空气中发生缓慢氧化,在40℃左右即可自燃。

①白磷(P4)的相对分子质量为
②基态P原子中成对电子数与未成对电子数之比为
③电负性:P
(2)磷,及其部分重要化合物的相互转化如图2所示。

①基态钙原子的简化电子排布式为
②第一电离能:Si
③CO2和CO的组成元素相同,但二者的性质不完全相同,其原因为
④常温下,H3PO4与少量NaOH溶液反应的化学方程式为
(3)反应Ⅲ的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)晶体的自范性即__________ ,区分晶体与非晶体最可靠的实验方法是________ ;
(2)原子间通过共用电子对所形成的相互作用叫做共价键。δ键与π键都属于共价键,δ键的特征是__________ ,Π键的特征是__________ 。
(3)Li2O是离子晶体,其晶格能可通过下图的Born−Haber循环计算得到。

可知,Li原子的第一电离能为__________ kJ/mol,O=O键键能为______ kJ/mol,Li2O的晶格能为_________ kJ/mol。
(4)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由_______ 个硼原子组成,共含有__________ 个B−B键。

(2)原子间通过共用电子对所形成的相互作用叫做共价键。δ键与π键都属于共价键,δ键的特征是
(3)Li2O是离子晶体,其晶格能可通过下图的Born−Haber循环计算得到。

可知,Li原子的第一电离能为
(4)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】固体电解质有广泛的用途。研究发现,晶体中有特殊结构为离子 如
如 提供快速迁移的宽敞通道或者有“点缺陷”,都能使其具有导电潜力。比如:图
提供快速迁移的宽敞通道或者有“点缺陷”,都能使其具有导电潜力。比如:图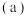 所示的锂超离子导体
所示的锂超离子导体 和图
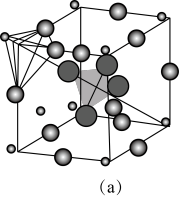
和图 所示的有“点缺陷”的NaCl。
所示的有“点缺陷”的NaCl。
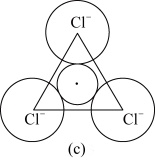
根据所学知识回答下列问题:
(1)在变化“Cl+e-→Cl-”过程中,所得电子填充在基态Cl的________ 能级,此过程会_______  填“吸收”或“释放”
填“吸收”或“释放” 能量。
能量。
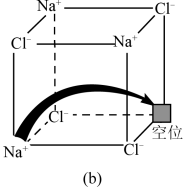
(2) 中B的杂化形式为
中B的杂化形式为__________ ,其等电子体为:___________  任写一种
任写一种 。与其VSEPR模型相同,且有1对孤电子对的相对分子质量最小的分子是
。与其VSEPR模型相同,且有1对孤电子对的相对分子质量最小的分子是____________ 。
(3)图 所示晶胞中
所示晶胞中 位于
位于__________ 位置;若将晶体中形成宽敞通道的 换成
换成 ,导电能力会明显降低,原因是
,导电能力会明显降低,原因是_____________ 。
(4)图 中,若缺陷处填充了
中,若缺陷处填充了 ,则它
,则它____________  填“是”或“不是”
填“是”或“不是” 的晶胞,在NaCl晶体中,
的晶胞,在NaCl晶体中, 填充在
填充在 堆积而成的
堆积而成的___________ 面体空隙中。
 如
如 提供快速迁移的宽敞通道或者有“点缺陷”,都能使其具有导电潜力。比如:图
提供快速迁移的宽敞通道或者有“点缺陷”,都能使其具有导电潜力。比如:图 所示的锂超离子导体
所示的锂超离子导体 和图
和图 所示的有“点缺陷”的NaCl。
所示的有“点缺陷”的NaCl。


根据所学知识回答下列问题:
(1)在变化“Cl+e-→Cl-”过程中,所得电子填充在基态Cl的
 填“吸收”或“释放”
填“吸收”或“释放” 能量。
能量。(2)
 中B的杂化形式为
中B的杂化形式为 任写一种
任写一种 。与其VSEPR模型相同,且有1对孤电子对的相对分子质量最小的分子是
。与其VSEPR模型相同,且有1对孤电子对的相对分子质量最小的分子是(3)图
 所示晶胞中
所示晶胞中 位于
位于 换成
换成 ,导电能力会明显降低,原因是
,导电能力会明显降低,原因是(4)图
 中,若缺陷处填充了
中,若缺陷处填充了 ,则它
,则它 填“是”或“不是”
填“是”或“不是” 的晶胞,在NaCl晶体中,
的晶胞,在NaCl晶体中, 填充在
填充在 堆积而成的
堆积而成的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】硒( )是人体必需微量元素之一,含硒化合物在材料和药物等领域具有重要应用。
)是人体必需微量元素之一,含硒化合物在材料和药物等领域具有重要应用。
(1) 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为_______ 。
(2) 的沸点低于
的沸点低于 ,其原因是
,其原因是_______ 。
(3)硒的两种含氧酸的酸性强弱为
_______  (填“>”或“<”)。
(填“>”或“<”)。 的空间结构为
的空间结构为_______ 。比较键角大小:气态 分子
分子_______  离子(填“>”“<”或“=”)。
离子(填“>”“<”或“=”)。

(4)关于Ⅰ~Ⅲ三种反应物,下列说法正确的有_______ 。
a.Ⅰ中仅有 键 b.Ⅰ中的
键 b.Ⅰ中的 键为非极性共价键 c.Ⅱ易溶于水 d.Ⅱ中原子的杂化轨道类型只有
键为非极性共价键 c.Ⅱ易溶于水 d.Ⅱ中原子的杂化轨道类型只有 与
与 e.Ⅰ~Ⅲ含有的元素中,O电负性最大
e.Ⅰ~Ⅲ含有的元素中,O电负性最大
(5)Ⅳ中具有孤对电子的原子有_______ 。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为_______ 。
②设X的化学式的式量为 ,晶胞边长为
,晶胞边长为 ,则晶体的密度为
,则晶体的密度为_______  (列出计算式)。
(列出计算式)。
 )是人体必需微量元素之一,含硒化合物在材料和药物等领域具有重要应用。
)是人体必需微量元素之一,含硒化合物在材料和药物等领域具有重要应用。(1)
 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为(2)
 的沸点低于
的沸点低于 ,其原因是
,其原因是(3)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。
(填“>”或“<”)。 的空间结构为
的空间结构为 分子
分子 离子(填“>”“<”或“=”)。
离子(填“>”“<”或“=”)。
(4)关于Ⅰ~Ⅲ三种反应物,下列说法正确的有
a.Ⅰ中仅有
 键 b.Ⅰ中的
键 b.Ⅰ中的 键为非极性共价键 c.Ⅱ易溶于水 d.Ⅱ中原子的杂化轨道类型只有
键为非极性共价键 c.Ⅱ易溶于水 d.Ⅱ中原子的杂化轨道类型只有 与
与 e.Ⅰ~Ⅲ含有的元素中,O电负性最大
e.Ⅰ~Ⅲ含有的元素中,O电负性最大(5)Ⅳ中具有孤对电子的原子有
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为
②设X的化学式的式量为
 ,晶胞边长为
,晶胞边长为 ,则晶体的密度为
,则晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】镍(28Ni)及其化合物在工业生产领域有广泛的应用。
(1)Ni在元素周期表中的位置是_______ ,前四周期元素中,基态原子含有未成对电子最多的元素的价层电子排布式为_______ 。
(2)如图所示为NaCl的晶胞结构,NiO(氧化镍)的晶胞结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,阿伏加德罗常数的值为NA,NiO晶体的密度是_______ 。(已知NiO的摩尔质量为74.7g/mol)

(3)天然的晶体和绝大部分人工制备的晶体都存在各种缺陷。例如,在某种氧化镍晶体中就存在如图所示的缺陷,一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其晶体仍呈电中性,但化合物中Ni和O的个数比却发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的个数之比为_______ 。

(1)Ni在元素周期表中的位置是
(2)如图所示为NaCl的晶胞结构,NiO(氧化镍)的晶胞结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,阿伏加德罗常数的值为NA,NiO晶体的密度是

(3)天然的晶体和绝大部分人工制备的晶体都存在各种缺陷。例如,在某种氧化镍晶体中就存在如图所示的缺陷,一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其晶体仍呈电中性,但化合物中Ni和O的个数比却发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的个数之比为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】中国古代四大发明之一——黑火药,它在爆炸时发生的化学反应为2KNO3+3C+S=A+N2↑+3CO2↑(已配平)
(1)①除S外,上列元素的电负性从大到小依次为__________ 。
②在生成物中,A的晶体类型为_______ ,含极性共价键的分子的中心原子轨道杂化类型为_____ 。
③已知CN-与N2互为等电子体,推算HCN分子中σ键与π键数目之比为_____ 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为______ ,Q2+的未成对电子数是_______ 。
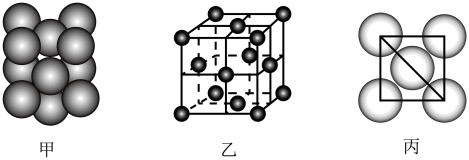
(3)若某金属单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。则晶胞中该原子的配位数为________ ,该单质晶体中原子的堆积方式为四种基本堆积方式中的________ 。
(1)①除S外,上列元素的电负性从大到小依次为
②在生成物中,A的晶体类型为
③已知CN-与N2互为等电子体,推算HCN分子中σ键与π键数目之比为
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为
(3)若某金属单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。则晶胞中该原子的配位数为

您最近一年使用:0次

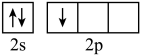 B.
B.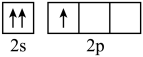 C.
C. D.
D.