已知:pOH=-lgc(OH-),在常温下溶液中的pH+pOH=14,又已知正常人(人的体温高于室温)的血液pH=7.3,则正常人血液的pOH是( )
| A.大于6.7 | B.小于6.7 |
| C.等于6.7 | D.无法判断 |
更新时间:2018-05-25 21:22:00
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】据文献报道: 催化某反应的一种反应机理如下图所示。下列叙述错误的是
催化某反应的一种反应机理如下图所示。下列叙述错误的是

 催化某反应的一种反应机理如下图所示。下列叙述错误的是
催化某反应的一种反应机理如下图所示。下列叙述错误的是
A.该催化循环中 的成键数目没有发生变化 的成键数目没有发生变化 |
B.每生成 转移 转移 电子 电子 |
C. 参与了该催化循环 参与了该催化循环 |
D.总反应方程式为: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列对一些实验事实的理论解释不正确 的是
| 选项 | 客观事实 | 理 论 解 释 |
| A. | 2Na(s)+2H2O (l) ===2NaOH(aq)+H2 (g) ΔH1=-368 kJ·mol-1在常温下能自发进行 | 该反应为放热且熵增的化学反应 |
| B. | 酸性:HClO<H2CO3 | 非金属:C>Cl |
| C. | 原子半径:Cl<S | Cl、S原子电子层数相同,但氯原子核电荷数较硫多,对核外电子吸引能力比硫强 |
| D. | 水分子比H2S分子稳定 | H-O键比H-S键稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】处理含 CO、SO2 烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。已知:
2CO(g)+O2(g)=2 CO2(g) △H1=-566.0kJ/mol
S(g)+O2(g)=SO2(g) △H2=-296.0kJ/mol
S(s)+O2(g)=SO2(g) △H3=?
下列说法不正确的是
2CO(g)+O2(g)=2 CO2(g) △H1=-566.0kJ/mol
S(g)+O2(g)=SO2(g) △H2=-296.0kJ/mol
S(s)+O2(g)=SO2(g) △H3=?
下列说法不正确的是
| A.△H3<△H2 |
| B.将少量 CO 2、SO2分别通入澄清石灰水,都能产生浑浊现象 |
| C.CO2分子中各原子最外层均为8电子稳定结构 |
| D.相同条件下:2CO(g)+SO2(g)=S(g)+2CO2(g) △H=-270kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,甲、乙两烧杯均盛有5mL pH=2的某一元酸溶液,现向乙烧杯中加水稀释至pH=3。此时关于甲、乙两烧杯中溶液的描述正确的是
| A.溶液的体积:10V甲=V乙 | B.溶液的体积:V乙≥10V甲 |
| C.溶液的体积:10V甲≥V乙 | D.水电离出的C(OH—):10C(OH-)甲≤C(OH-)乙 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25 ℃时,向盛有50 mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。下列叙述正确的是( )


| A.HA溶液的物质的量浓度为0.01 mol·L-1 |
| B.b→c的过程中,温度降低的原因是溶液中发生了吸热反应 |
| C.25 ℃时,HA的电离平衡常数K约为1.43×10-2 |
| D.b点处,酸碱恰好中和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
【推荐1】在浓度为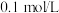 的
的 溶液中,如下说法正确的是
溶液中,如下说法正确的是
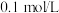 的
的 溶液中,如下说法正确的是
溶液中,如下说法正确的是A.溶液中浓度最大的离子是 |
B.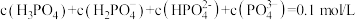 |
C.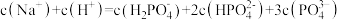 |
D.磷酸第二步电离平衡的平衡常数表达式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,一定浓度的某酸HA溶液的pH=5,下列有关说法正确的是
| A.取该溶液1.00 mL,加水稀释至1 000 mL,所得溶液pH=8 |
| B.向溶液中加入适量NaA固体,若溶液pH不变,则HA为强酸 |
| C.加入等体积pH=9的NaOH溶液,若所得溶液pH>7,则HA为弱酸 |
| D.若该溶液导电能力弱于等体积pH=5的HCl溶液,则HA为弱酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法正确的是
①常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4
②为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
③相同温度下,将足量氯化银固体分别放入相同体积的a.蒸馏水b.0.1mol·L-1盐酸、c.0.1mol·L-1氯化镁溶液d.0.1mol·L-1硝酸银溶液中,Ag+浓度:a>d=b>c
④用0.2000mol·L-1NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1mol·L-1),至中性时,溶液中的酸未被完全中和
⑤将水加热到100℃,pH=6:c(OH)< c(H+)
⑥醋酸与醋酸钠的pH=7的混合溶液中:c(CH3COO-)> c(Na+)
⑦0.lmol·L-1的硫酸铵溶液中:c( )> c(
)> c( )> c(H+)
)> c(H+)
⑧pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)= c(H+)
①常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4
②为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
③相同温度下,将足量氯化银固体分别放入相同体积的a.蒸馏水b.0.1mol·L-1盐酸、c.0.1mol·L-1氯化镁溶液d.0.1mol·L-1硝酸银溶液中,Ag+浓度:a>d=b>c
④用0.2000mol·L-1NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1mol·L-1),至中性时,溶液中的酸未被完全中和
⑤将水加热到100℃,pH=6:c(OH)< c(H+)
⑥醋酸与醋酸钠的pH=7的混合溶液中:c(CH3COO-)> c(Na+)
⑦0.lmol·L-1的硫酸铵溶液中:c(
 )> c(
)> c( )> c(H+)
)> c(H+)⑧pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)= c(H+)
| A.③⑤ | B.①⑧ | C.④⑦ | D.②⑥ |
您最近一年使用:0次

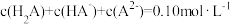 的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法不正确的是
的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法不正确的是
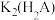 的数量级为
的数量级为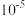
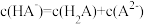

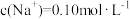 的溶液中,
的溶液中,