第23号元素钒在地壳中的含量大约为0.009%,在过渡元素中仅次于Fe、Ti、Mn、Zn,排第五位。我国四川攀枝花地区蕴藏着极其丰富的钒钛磁铁矿。
(1)钒在周期表中的位置为__________ ,电子占据的最高能层的轨道形状为__________ 。
(2)在地壳中含量最高的五种过渡金属元素Fe、Ti、Mn、Zn、V中,基态原子核外单电子数最多的是__________ 。
(3)过渡金属可形成许多羰基配合物,即CO作为配体形成的配合物。
①CO的等电子体有N2、CN-、__________ (任写一个)等。
②CO作配体时,配位原子是C而不是O,其原因是__________ 。
(4)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如[Fe(CO)5]、[Mn(CO)5]-等都满足这个规则。
①下列钒配合物中,钒原子满足18电子规则的是__________ 。
A.[V(H2O)6]2+ B.[V(CN)6]4- C.[V(CO)6]- D.[V(O2)4]3-
②化合物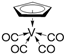 的熔点为138 ℃,其晶体类型为
的熔点为138 ℃,其晶体类型为__________ ;已知该化合物满足18电子规则,其配体“ ”中的大π键可表示为
”中的大π键可表示为__________ 。
(5)VCl2(熔点1027 ℃)和VBr2(熔点827 ℃)均为六方晶胞,结构如图所示。
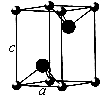
①VCl2和VBr2两者熔点差异的原因是__________ 。
②设晶体中阴、阳离子半径分别为r-和r+,该晶体的空间利用率为__________ (用含a、c、r+和r-的式子表示)。
(1)钒在周期表中的位置为
(2)在地壳中含量最高的五种过渡金属元素Fe、Ti、Mn、Zn、V中,基态原子核外单电子数最多的是
(3)过渡金属可形成许多羰基配合物,即CO作为配体形成的配合物。
①CO的等电子体有N2、CN-、
②CO作配体时,配位原子是C而不是O,其原因是
(4)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如[Fe(CO)5]、[Mn(CO)5]-等都满足这个规则。
①下列钒配合物中,钒原子满足18电子规则的是
A.[V(H2O)6]2+ B.[V(CN)6]4- C.[V(CO)6]- D.[V(O2)4]3-
②化合物
 的熔点为138 ℃,其晶体类型为
的熔点为138 ℃,其晶体类型为 ”中的大π键可表示为
”中的大π键可表示为(5)VCl2(熔点1027 ℃)和VBr2(熔点827 ℃)均为六方晶胞,结构如图所示。

①VCl2和VBr2两者熔点差异的原因是
②设晶体中阴、阳离子半径分别为r-和r+,该晶体的空间利用率为
2018·四川绵阳·一模 查看更多[5]
【全国百强校】四川省绵阳中学2018届高三考前适应性考试(三)理科综合化学试题【全国百强校】江西省新余市第四中学2020届高三第七次训练理科综合化学试题四川省绵阳南山中学2020届高三下学期3月网络考试化学试题(已下线)考点14 物质结构与性质(选考)-2020年高考化学命题预测与模拟试题分类精编解题达人.化学选择题(2021全国卷)精编特训10
更新时间:2018-05-29 08:09:40
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】锂一磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备: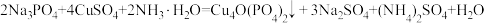 。回答下列问题:
。回答下列问题:
(1)铜位于周期表中_____ 区,与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有_____ (填元素符号)。
(2)上述方程式中涉及的N、O、P、S元素第一电离能由小到大的顺序为________ ,电负性由小到大的顺序为______ 。
(3)常见含硫的微粒有SO2、SO3、 等,
等, 的空间构型为
的空间构型为________ ;SO2、SO3杂化轨道类型相同,但键角SO3大于SO2,原因是_______ 。
(4)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则[Cu(CN)4]2-中σ键与π键的数目之比为_______ 。
(5)铜的晶胞结构如图所示。
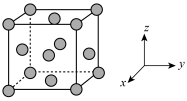
①铜晶胞在x轴方向的投影图是_____ (填标号)。
A.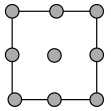 B.
B. 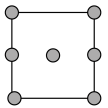
C.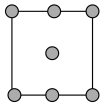 D.
D. 
②假设铜晶胞参数为anm,铜晶体的密度为bg·cm-3,则铜的相对原子质量为_____ (设NA为阿伏加德罗常数的值,用含a、b、NA的代数式表示)。
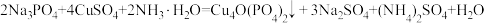 。回答下列问题:
。回答下列问题:(1)铜位于周期表中
(2)上述方程式中涉及的N、O、P、S元素第一电离能由小到大的顺序为
(3)常见含硫的微粒有SO2、SO3、
 等,
等, 的空间构型为
的空间构型为(4)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则[Cu(CN)4]2-中σ键与π键的数目之比为
(5)铜的晶胞结构如图所示。

①铜晶胞在x轴方向的投影图是
A.
 B.
B. 
C.
 D.
D. 
②假设铜晶胞参数为anm,铜晶体的密度为bg·cm-3,则铜的相对原子质量为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】M、R、X、Y、Z为原子序数依次增大的短周期主族元素,M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,Y和M形成的一种化合物是引起酸雨的主要大气污染物,X的原子核外有3个单电子。请回答下列问题:
(1)R基态原子的电子排布式是______________ ,X、Y、Z电负性由小到大的顺序是_______ (填元素符号)
(2)Y的氢化物在乙醇中的溶解度小于M的氢化物,其原因是______________
(3)在 H2O分子中,H﹣O﹣H的键角是_________ ,H3O+中H﹣O﹣H键角比H2O中H﹣O﹣H键角________ 填“大、小、相等”),原因为________________________________
(4)Y与M形成的YM3分子的空间构型是____________________ .
(1)R基态原子的电子排布式是
(2)Y的氢化物在乙醇中的溶解度小于M的氢化物,其原因是
(3)在 H2O分子中,H﹣O﹣H的键角是
(4)Y与M形成的YM3分子的空间构型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】离子晶体是常见的晶体类型。请回答以下问题:
(1)离子晶体中阴阳离子半径之比是决定晶体构型的重要因素之一,配位数与离子半径之比存在如下关系:

已知在某AB型离子化合物中,A+离子的半径为84 pm,B-离子的半径为140 pm。分析以上信息,与A+离子配位的所有B-离子,在空间构成的立体形状为_______ 。
(2)硫化亚铜和氧化亚铜均为离子晶体,其中熔点较高的为________ (填化学式),原因是________ 。
(3)向硫酸铜溶液中加入乙二胺(H2N-CH2-CH2-NH2)溶液后,每个Cu2+可与两个乙二胺分子形成四配位离子,导致溶液由蓝色变为紫色。该四配位离子的结构式为_______ 。
(4)K3C60是由足球烯(C60)与金属钾反应生成的盐。在K3C60晶胞中,C603-堆积方式为面心立方结构,每个晶胞中形成4个八面体空隙和8个四面体空隙,K+填充在空隙中。晶胞中被K+占据的空隙百分比为__________ 。
(5)H和Mg能形成一种离子型储氢材料,晶体结构如右图所示:

则该晶体中Mg的配位数是______ ,其化学式为________ 。已知该晶体的密度为ρg·cm-3,晶胞的体积为__________ (用ρ、NA表示,其中NA表示阿伏伽德罗常数的值)。
(1)离子晶体中阴阳离子半径之比是决定晶体构型的重要因素之一,配位数与离子半径之比存在如下关系:

已知在某AB型离子化合物中,A+离子的半径为84 pm,B-离子的半径为140 pm。分析以上信息,与A+离子配位的所有B-离子,在空间构成的立体形状为
(2)硫化亚铜和氧化亚铜均为离子晶体,其中熔点较高的为
(3)向硫酸铜溶液中加入乙二胺(H2N-CH2-CH2-NH2)溶液后,每个Cu2+可与两个乙二胺分子形成四配位离子,导致溶液由蓝色变为紫色。该四配位离子的结构式为
(4)K3C60是由足球烯(C60)与金属钾反应生成的盐。在K3C60晶胞中,C603-堆积方式为面心立方结构,每个晶胞中形成4个八面体空隙和8个四面体空隙,K+填充在空隙中。晶胞中被K+占据的空隙百分比为
(5)H和Mg能形成一种离子型储氢材料,晶体结构如右图所示:

则该晶体中Mg的配位数是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】根据物质结构相关知识,回答下列问题:
(1)在第三周期的元素中,第一电离能介于Mg与Cl之间的有__________ 种。
(2)碳元素与氮元素形成的某种晶体的晶胞如图所示,其中8个C原子位于立方体的顶点,4个C原子位于立方体的面心,4个N原子在立方体内。
①已知该晶体硬度超过金刚石,其原因是_________________ 。
②晶胞中C原子的杂化方式为___________ 。
③知该晶胞参数为a nm,阿伏伽德罗常数用NA表示,则该晶体的密度为________ g·cm-3
(3)大π键可表示为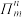 ,其中m代表参与形成的大π键原子数,n表示大π键的电子数,如
,其中m代表参与形成的大π键原子数,n表示大π键的电子数,如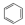 的大π键可表示为
的大π键可表示为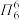 ,则CO32-中的大π键可表示为
,则CO32-中的大π键可表示为_________________ 。
(4)金属铬是一种极硬、耐腐蚀的银白色金属,其化合物种类繁多,如:Cr2(SO4)3、K2Cr2O7以及配离子[Cr(H2O)3(NH3)3]3+等。
①基态铬原子的价电子排布式为________________ 。
②配离子[Cr(H2O)3(NH3)3]3+的结构可能有_________ 种。
(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AIP的熔点为2000℃,其晶胞结构如下图所示。
①C点的原子坐标为_______________ 。
②AlP的晶胞中,Al原子位于P原子形成的正四面体空隙中,此空隙的填充率为_____ 。
(1)在第三周期的元素中,第一电离能介于Mg与Cl之间的有
(2)碳元素与氮元素形成的某种晶体的晶胞如图所示,其中8个C原子位于立方体的顶点,4个C原子位于立方体的面心,4个N原子在立方体内。
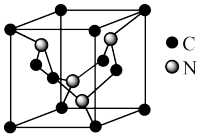
①已知该晶体硬度超过金刚石,其原因是
②晶胞中C原子的杂化方式为
③知该晶胞参数为a nm,阿伏伽德罗常数用NA表示,则该晶体的密度为
(3)大π键可表示为
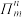 ,其中m代表参与形成的大π键原子数,n表示大π键的电子数,如
,其中m代表参与形成的大π键原子数,n表示大π键的电子数,如 的大π键可表示为
的大π键可表示为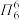 ,则CO32-中的大π键可表示为
,则CO32-中的大π键可表示为(4)金属铬是一种极硬、耐腐蚀的银白色金属,其化合物种类繁多,如:Cr2(SO4)3、K2Cr2O7以及配离子[Cr(H2O)3(NH3)3]3+等。
①基态铬原子的价电子排布式为
②配离子[Cr(H2O)3(NH3)3]3+的结构可能有
(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AIP的熔点为2000℃,其晶胞结构如下图所示。
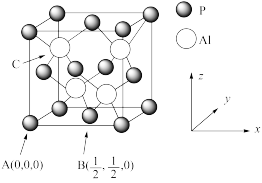
①C点的原子坐标为
②AlP的晶胞中,Al原子位于P原子形成的正四面体空隙中,此空隙的填充率为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】锌及其化合物在生产生活中应用广泛。回答下列问题:
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
(2)一种香豆素衍生物( )可作为测定
)可作为测定 的荧光探针,其原理如下图所示。已知
的荧光探针,其原理如下图所示。已知 中
中 结构的异构化和旋转会导致荧光减弱。
结构的异构化和旋转会导致荧光减弱。

① 所含元素(C、H、O、N)电负性从大到小的顺序为
所含元素(C、H、O、N)电负性从大到小的顺序为_______ ;
② 中N原子的杂化类型为
中N原子的杂化类型为_______ ;
③加入 后,体系荧光增强的原因是
后,体系荧光增强的原因是_______ 。
(3) 可用于配制炉甘石洗剂,具有收敛和保护皮肤的作用。
可用于配制炉甘石洗剂,具有收敛和保护皮肤的作用。 中阴离子
中阴离子 的空间构型为
的空间构型为_______ ,与 互为等电子体的分子有
互为等电子体的分子有_______ (任写一种)。
(4) 水溶液可作为工业零件淬火的冷却介质。已知
水溶液可作为工业零件淬火的冷却介质。已知 的熔点为275℃,而
的熔点为275℃,而 的熔点为782℃,两者熔点相差较大,其原因是
的熔点为782℃,两者熔点相差较大,其原因是_______ 。
(5) 是一种性能优异的荧光材料,在自然界中有立方
是一种性能优异的荧光材料,在自然界中有立方 和六方
和六方 两种晶型,其晶胞结构如下图所示:
两种晶型,其晶胞结构如下图所示:

①立方 中,
中, 填充在
填充在 形成的
形成的_______ 空隙中;
②六方 的晶体密度为
的晶体密度为_______  (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为(2)一种香豆素衍生物(
 )可作为测定
)可作为测定 的荧光探针,其原理如下图所示。已知
的荧光探针,其原理如下图所示。已知 中
中 结构的异构化和旋转会导致荧光减弱。
结构的异构化和旋转会导致荧光减弱。
①
 所含元素(C、H、O、N)电负性从大到小的顺序为
所含元素(C、H、O、N)电负性从大到小的顺序为②
 中N原子的杂化类型为
中N原子的杂化类型为③加入
 后,体系荧光增强的原因是
后,体系荧光增强的原因是(3)
 可用于配制炉甘石洗剂,具有收敛和保护皮肤的作用。
可用于配制炉甘石洗剂,具有收敛和保护皮肤的作用。 中阴离子
中阴离子 的空间构型为
的空间构型为 互为等电子体的分子有
互为等电子体的分子有(4)
 水溶液可作为工业零件淬火的冷却介质。已知
水溶液可作为工业零件淬火的冷却介质。已知 的熔点为275℃,而
的熔点为275℃,而 的熔点为782℃,两者熔点相差较大,其原因是
的熔点为782℃,两者熔点相差较大,其原因是(5)
 是一种性能优异的荧光材料,在自然界中有立方
是一种性能优异的荧光材料,在自然界中有立方 和六方
和六方 两种晶型,其晶胞结构如下图所示:
两种晶型,其晶胞结构如下图所示:
①立方
 中,
中, 填充在
填充在 形成的
形成的②六方
 的晶体密度为
的晶体密度为 (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵[(NH4)3Fe(C6H5O7)2]。
(1)Fe基态核外电子排布式为_________ ;
(2)[Fe(H2O)6]2+与NO反应生成的[Fe(NO)(H2O)5]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)(H2O)5]2+结构示意图的相应位置补填缺少的配体_________ 。

(3)C、N、O元素的第一电离能由大到小的顺序为_______ 。
(4)乙醇的沸点高于丙酮,这是因为_________ 。
(5)与NH 互为等电子体的一种分子为
互为等电子体的一种分子为____ (填化学式)。
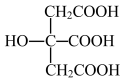
(6)柠檬酸的结构简式见下图。1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为_____ mol。
(1)Fe基态核外电子排布式为
(2)[Fe(H2O)6]2+与NO反应生成的[Fe(NO)(H2O)5]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)(H2O)5]2+结构示意图的相应位置补填缺少的配体

(3)C、N、O元素的第一电离能由大到小的顺序为
(4)乙醇的沸点高于丙酮,这是因为
(5)与NH
 互为等电子体的一种分子为
互为等电子体的一种分子为(6)柠檬酸的结构简式见下图。1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】金属及其化合物具有非常广泛的性质及用途,回答下列问题
(1)碳酸钠和碳酸氢钠是用途广泛的化合物,写出碳酸钠的一种用途___________ 。在实验室中,充分加热碳酸钠和碳酸氢钠的混合物4.80g,完全反应后称得剩余固体质量为3.87g,则混合物中碳酸氢钠的质量分数为___________ 。
(2)某久置的 溶液略显黄色,某同学认为已有部分
溶液略显黄色,某同学认为已有部分 被空气中的氧气氧化为
被空气中的氧气氧化为 。
。
①写出 被空气中的氧气氧化的离子方程式
被空气中的氧气氧化的离子方程式___________ 。
②实验室用邻二氮菲(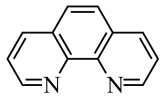 )与
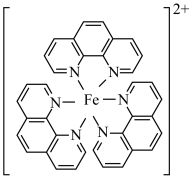
)与 形成的红色配合离子(如图)测定
形成的红色配合离子(如图)测定 的浓度。该配合物中心离子的配位数为
的浓度。该配合物中心离子的配位数为___________ 。该配合离子所含元素的电负性最大的是___________ ,C原子的杂化方式为___________ 。从结构角度分析, 易被氧化成
易被氧化成 的原因是
的原因是___________ 。
③请设计实验验证溶液中是否存在 :
:___________ 。
(3)聚合硫酸铁可用于水的净化,其化学式可表示为 ,取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的
,取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的 溶液,得到白色沉淀1.7475g。另一份溶液,先将
溶液,得到白色沉淀1.7475g。另一份溶液,先将 还原为
还原为 ,再用0.02000mol/L
,再用0.02000mol/L  标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液50.00mL。重铬酸钾与亚铁离子反应的离子方程式为
标准溶液50.00mL。重铬酸钾与亚铁离子反应的离子方程式为___________ ,该聚合硫酸铁样品中a∶b的比值为___________ 。
(1)碳酸钠和碳酸氢钠是用途广泛的化合物,写出碳酸钠的一种用途
(2)某久置的
 溶液略显黄色,某同学认为已有部分
溶液略显黄色,某同学认为已有部分 被空气中的氧气氧化为
被空气中的氧气氧化为 。
。①写出
 被空气中的氧气氧化的离子方程式
被空气中的氧气氧化的离子方程式②实验室用邻二氮菲(
 )与
)与 形成的红色配合离子(如图)测定
形成的红色配合离子(如图)测定 的浓度。该配合物中心离子的配位数为
的浓度。该配合物中心离子的配位数为 易被氧化成
易被氧化成 的原因是
的原因是
③请设计实验验证溶液中是否存在
 :
:(3)聚合硫酸铁可用于水的净化,其化学式可表示为
 ,取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的
,取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的 溶液,得到白色沉淀1.7475g。另一份溶液,先将
溶液,得到白色沉淀1.7475g。另一份溶液,先将 还原为
还原为 ,再用0.02000mol/L
,再用0.02000mol/L  标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液50.00mL。重铬酸钾与亚铁离子反应的离子方程式为
标准溶液50.00mL。重铬酸钾与亚铁离子反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】镍及其化合物是重要的合金材料和催化剂。请回答下列问题:

(1)基态镍原子的价电子排布式为___________ ,排布时最高电子层的电子所占的原子轨道有___________ 个伸展方向。
(2)镍能形成多种配合物如正四面体形的 、正方形的
、正方形的 和正八面体形的
和正八面体形的 等。下列说法不正确的有
等。下列说法不正确的有___________ 。
A. 与
与 互为等电子体,其中
互为等电子体,其中 分子内
分子内 键和
键和 键个数之比为
键个数之比为
B. 的空间结构为平面三角形
的空间结构为平面三角形
C. 在形成配合物时,其配位数可能为4或6
在形成配合物时,其配位数可能为4或6
D. 中,镍元素是
中,镍元素是 杂化
杂化
(3)丁二酮肟常用于检验 :在稀氨水中,丁二酮肟与
:在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用“…”表示出氢键
反应生成鲜红色沉淀,其结构如图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用“…”表示出氢键___________ 。
(4) 的晶体结构类型与氯化钠的相同,相关离子半径如下表:
的晶体结构类型与氯化钠的相同,相关离子半径如下表:
 熔点比
熔点比 高的原因是
高的原因是___________ 。

(1)基态镍原子的价电子排布式为
(2)镍能形成多种配合物如正四面体形的
 、正方形的
、正方形的 和正八面体形的
和正八面体形的 等。下列说法不正确的有
等。下列说法不正确的有A.
 与
与 互为等电子体,其中
互为等电子体,其中 分子内
分子内 键和
键和 键个数之比为
键个数之比为
B.
 的空间结构为平面三角形
的空间结构为平面三角形C.
 在形成配合物时,其配位数可能为4或6
在形成配合物时,其配位数可能为4或6D.
 中,镍元素是
中,镍元素是 杂化
杂化(3)丁二酮肟常用于检验
 :在稀氨水中,丁二酮肟与
:在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用“…”表示出氢键
反应生成鲜红色沉淀,其结构如图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用“…”表示出氢键(4)
 的晶体结构类型与氯化钠的相同,相关离子半径如下表:
的晶体结构类型与氯化钠的相同,相关离子半径如下表: |  |  |  |
 |  |  |  |
 熔点比
熔点比 高的原因是
高的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】钛被誉为“21世纪的金属”,可呈现多种化合价,其中以+4价的Ti最为稳定。回答下列问题:
(1)基态Ti原子的价电子轨道表示式为___ 。
(2)已知电离能:I2(Ti)=1 310 kJ/mol,I2(K)=3051 kJ/mol,I2(Ti)<I2(K),其原因为_____________
(3)钛某配合物可用于催化环烯烃聚合,其结构如下图所示:

①钛的配位数为___ ,碳原子的杂化类型____ 。
②该配合物中存在的化学键有____ (填字母代号)。
A.离子键 B.配位键 C.金属键 D.共价键 e.氢键
(4)钛与卤素形成的化合物熔沸点如下表所示:
分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是_________________
(5)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为____ ,阴离子的空间构型为__________ .


(6)已知TiN晶体的晶胞结构如图所示,若该晶胞的密度为ρg/cm3,阿伏加 德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为____ pm(用含p、NA的代数式表示)。
(1)基态Ti原子的价电子轨道表示式为
(2)已知电离能:I2(Ti)=1 310 kJ/mol,I2(K)=3051 kJ/mol,I2(Ti)<I2(K),其原因为
(3)钛某配合物可用于催化环烯烃聚合,其结构如下图所示:

①钛的配位数为
②该配合物中存在的化学键有
A.离子键 B.配位键 C.金属键 D.共价键 e.氢键
(4)钛与卤素形成的化合物熔沸点如下表所示:
| TiCl4 | TiBr4 | TiI4 | |
| 熔点/℃ | -24.1 | 38.3 | 155 |
| 沸点/℃ | 136.5 | 233.5 | 377 |
分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是
(5)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为


(6)已知TiN晶体的晶胞结构如图所示,若该晶胞的密度为ρg/cm3,阿伏加 德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)基态镍原子的核外电子排布式为___________ 。
(2)很多不饱和有机物在Ni催化下可与H2发生加成反应,如:① ②
② ③
③ ④HCHO,其中碳原子的杂化轨道类型为sp2杂化的分子有
④HCHO,其中碳原子的杂化轨道类型为sp2杂化的分子有___________ (填物质序号)。
(3) 中阴离子的立体构型是
中阴离子的立体构型是___________ 。比较氨气(NH3)的沸点与膦(PH3),理由是___________ 。
(4)某镍白铜合金的立方晶胞结构如图所示,请回答:

①晶胞中镍原子的堆积模型名称是___________ 。
②元素铜与镍的第二电离能分别为 ,
,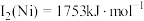 ,
, 的原因是
的原因是___________ 。
③若合金的密度为 ,晶胞参数(即棱长)a=
,晶胞参数(即棱长)a=___________ nm。(用NA表示阿伏加德罗常数的值)
(1)基态镍原子的核外电子排布式为
(2)很多不饱和有机物在Ni催化下可与H2发生加成反应,如:①
 ②
② ③
③ ④HCHO,其中碳原子的杂化轨道类型为sp2杂化的分子有
④HCHO,其中碳原子的杂化轨道类型为sp2杂化的分子有(3)
 中阴离子的立体构型是
中阴离子的立体构型是(4)某镍白铜合金的立方晶胞结构如图所示,请回答:

①晶胞中镍原子的堆积模型名称是
②元素铜与镍的第二电离能分别为
 ,
,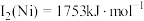 ,
, 的原因是
的原因是③若合金的密度为
 ,晶胞参数(即棱长)a=
,晶胞参数(即棱长)a=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Co、Ni 元素及其化合物有着很多优良的性能和特性,回答下列问题:
(1)基态 Ni 原子的价电子排布图为_______ ;金属镍的原子堆积方式如图所示,则金属镍的晶胞俯视图为_______ (填字母)。

a. b.
b. c.
c. d.
d.
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4 蓝色溶液,N 原子的杂化方式是_______ ,[Ni(NH3)6]SO4晶体中不存在的化学键类型包括_______ (填序号)。
A.极性共价键 B.离子键 C.配位键 D.金属键 E.非极性共价键 F.氢键
(3)Co3+通常易形成六配位的配合物,已知 CoCl3·6H2O 有多种结构,若取 1mol CoCl3·6H2O溶解于水后滴加足量的硝酸银溶液,能够形成 2mol 沉淀,则 CoCl3·6H2O 中配离子的结构示意图为(不考虑空间结构)_______ 。
(4)Co3O4 晶体中 O 作面心立方最密堆积(如图),Co 随机填充在晶胞中 O 构成的 8 个四面体空隙和 4 个八面体空隙中,则 Co 的配位数分别为_______ 、_______ ,如果晶胞边长为a nm,Co3O4的摩尔质量为 M g/mol,NA为阿伏加德罗常数的值,则Co3O4 的晶体密度为_______ g/cm3(列出计算式)。

(1)基态 Ni 原子的价电子排布图为

a.
 b.
b. c.
c. d.
d.
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4 蓝色溶液,N 原子的杂化方式是
A.极性共价键 B.离子键 C.配位键 D.金属键 E.非极性共价键 F.氢键
(3)Co3+通常易形成六配位的配合物,已知 CoCl3·6H2O 有多种结构,若取 1mol CoCl3·6H2O溶解于水后滴加足量的硝酸银溶液,能够形成 2mol 沉淀,则 CoCl3·6H2O 中配离子的结构示意图为(不考虑空间结构)
(4)Co3O4 晶体中 O 作面心立方最密堆积(如图),Co 随机填充在晶胞中 O 构成的 8 个四面体空隙和 4 个八面体空隙中,则 Co 的配位数分别为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】吴梦昊研究团队设计了一系列稳定的由超碱 和超卤素
和超卤素 组成的
组成的 (
( ;
; ;
; )超盐晶体。
)超盐晶体。
(1)基态铁原子价电子排布中未成对电子数与成对电子对数之比为________ 。
(2)第二周期元素中,第一电离能介于元素B和N之间的元素有________ 种。
(3)键角:
________  (填“大于”或“小于”),请分析原因:
(填“大于”或“小于”),请分析原因:________________________ 。
(4)六方相氮化硼晶体结构与石墨相似(如图1),晶体中氮原子的杂化方式为________ 。氮化硼晶体不导电的原因是________________________ 。

(5)磷化硼晶胞结构如图2所示,晶胞中P原子空间堆积方式为________ ;已知晶体中硼和磷原子半径分别为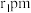 和
和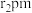 ,距离最近的硼和磷原子核间距为二者原子半径之和。则磷化硼晶胞中原子的体积占晶胞体积的百分率为
,距离最近的硼和磷原子核间距为二者原子半径之和。则磷化硼晶胞中原子的体积占晶胞体积的百分率为________________ (写出计算式)。

 和超卤素
和超卤素 组成的
组成的 (
( ;
; ;
; )超盐晶体。
)超盐晶体。(1)基态铁原子价电子排布中未成对电子数与成对电子对数之比为
(2)第二周期元素中,第一电离能介于元素B和N之间的元素有
(3)键角:

 (填“大于”或“小于”),请分析原因:
(填“大于”或“小于”),请分析原因:(4)六方相氮化硼晶体结构与石墨相似(如图1),晶体中氮原子的杂化方式为

(5)磷化硼晶胞结构如图2所示,晶胞中P原子空间堆积方式为
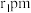 和
和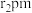 ,距离最近的硼和磷原子核间距为二者原子半径之和。则磷化硼晶胞中原子的体积占晶胞体积的百分率为
,距离最近的硼和磷原子核间距为二者原子半径之和。则磷化硼晶胞中原子的体积占晶胞体积的百分率为
您最近一年使用:0次



