亚氯酸钠(NaClO2)是一种高效漂白剂,工业设计生产NaClO2的主要流程如下:
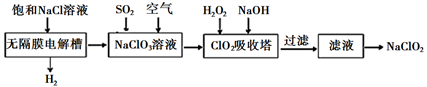
已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用,ClO2气体在中性和碱性溶液中不能稳定存在。
②NaClO2饱和溶液在温度低于38℃时析出晶体NaClO2·3H2O,温度高于38℃时析出晶体NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl。
(1)写出无隔膜电解槽中阳极的电极反应方程式:____________________________ 。
(2)生成ClO2的反应中需用酸进行酸化,你认为最宜选用的酸为______________ (写酸的名称)。
(3)ClO2吸收塔中发生反应的离子方程式为______________ ,H2O2的电子式为______________ 。
(4)请补充从滤液获得NaClO2的操作步骤:①减压,55℃蒸发结晶;②__________________ ;③__________________ ;④__________________ ,得到成品。
(5)NaClO2溶液浓度含量可用碘量法测定,其原理为在稀硫酸介质中,NaClO2能定量地将碘离子氧化成碘,以淀粉为指示剂,用0.1000 mol·L−1的硫代硫酸钠标准溶液滴定碘而确定NaClO2。
已知:2I2 + 2Na2S2O3 2NaI + Na2S4O6。取NaClO2溶液体积V1 mL加入到适量的稀硫酸和KI溶液中,反应完毕用Na2S2O3滴定反应后的溶液,消耗V2 mL Na2S2O3溶液,则NaClO2的浓度为
2NaI + Na2S4O6。取NaClO2溶液体积V1 mL加入到适量的稀硫酸和KI溶液中,反应完毕用Na2S2O3滴定反应后的溶液,消耗V2 mL Na2S2O3溶液,则NaClO2的浓度为_____________ g·L−1(杂质不参与反应,NaClO2中的氯元素被还原为Cl−)。

已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用,ClO2气体在中性和碱性溶液中不能稳定存在。
②NaClO2饱和溶液在温度低于38℃时析出晶体NaClO2·3H2O,温度高于38℃时析出晶体NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl。
(1)写出无隔膜电解槽中阳极的电极反应方程式:
(2)生成ClO2的反应中需用酸进行酸化,你认为最宜选用的酸为
(3)ClO2吸收塔中发生反应的离子方程式为
(4)请补充从滤液获得NaClO2的操作步骤:①减压,55℃蒸发结晶;②
(5)NaClO2溶液浓度含量可用碘量法测定,其原理为在稀硫酸介质中,NaClO2能定量地将碘离子氧化成碘,以淀粉为指示剂,用0.1000 mol·L−1的硫代硫酸钠标准溶液滴定碘而确定NaClO2。
已知:2I2 + 2Na2S2O3
 2NaI + Na2S4O6。取NaClO2溶液体积V1 mL加入到适量的稀硫酸和KI溶液中,反应完毕用Na2S2O3滴定反应后的溶液,消耗V2 mL Na2S2O3溶液,则NaClO2的浓度为
2NaI + Na2S4O6。取NaClO2溶液体积V1 mL加入到适量的稀硫酸和KI溶液中,反应完毕用Na2S2O3滴定反应后的溶液,消耗V2 mL Na2S2O3溶液,则NaClO2的浓度为
2018高三·全国·专题练习 查看更多[1]
(已下线)《2018,我的高考我的教师君》- 名师团队考前模拟练
更新时间:2018-06-08 11:11:10
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氯氧化铋(BiOCl)常用于电子设备等领域,BiOCl难溶于水,它是BiCl3的水解产物。以铋的废料(主要含铋的化合物,含少量铜、铅、锌的硫酸盐及Cu2S和Fe2O3等)为原料生产高纯度BiOCl的工艺流程如下:
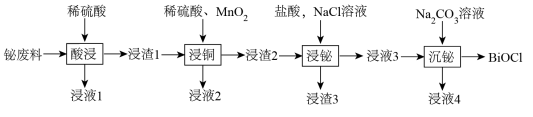
请回答下列问题:
(1)在浸液1中加入过量的锌,过滤,将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥得结晶水合物M,M的摩尔质量为287 g·mol-1,M为___ (填化学式)。
(2)已知:浸液2呈蓝色,浸渣2含有少量硫单质。“浸铜”中MnO2的作用是____ (用离子方程式表示)。
(3)“浸铋”中,铋的浸出率与温度关系如图所示:
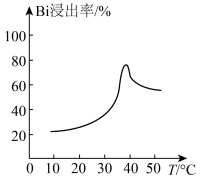
在高于40℃左右时“铋浸出率”开始下降,其主要因素可能是____ (从两个角度分析)。
(4)在室温和液固比固定的条件下,c(HCl)=1.0mol·L-1时,铋的浸出率与溶液中c(Cl-)的关系如图所示。“浸铋”操作中,加入NaCl的目的是____ 。

(5)浸液3中主要溶质是BiCl3,“沉铋”过程中,有气体放出。“沉铋”的主要化学反应的方程式为____ 。从绿色化学角度看,浸液4可以用于____ (填“酸浸”、“浸铜”或“浸铋”)。
(6)测定产品的纯度:取mg充分洗涤并干燥后的产品,溶于稍过量的浓硝酸中,加水稀释到100.0mL,取20.0mL于烧杯中,用cmol·L-1的AgNO3标准溶液滴定至终点(用Na2CrO4,作指示剂),消耗AgNO3标准溶液VmL,则产品中BiOCl的质量分数为____ %(用含m、c、V的代数式表示)。

请回答下列问题:
(1)在浸液1中加入过量的锌,过滤,将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥得结晶水合物M,M的摩尔质量为287 g·mol-1,M为
(2)已知:浸液2呈蓝色,浸渣2含有少量硫单质。“浸铜”中MnO2的作用是
(3)“浸铋”中,铋的浸出率与温度关系如图所示:

在高于40℃左右时“铋浸出率”开始下降,其主要因素可能是
(4)在室温和液固比固定的条件下,c(HCl)=1.0mol·L-1时,铋的浸出率与溶液中c(Cl-)的关系如图所示。“浸铋”操作中,加入NaCl的目的是

(5)浸液3中主要溶质是BiCl3,“沉铋”过程中,有气体放出。“沉铋”的主要化学反应的方程式为
(6)测定产品的纯度:取mg充分洗涤并干燥后的产品,溶于稍过量的浓硝酸中,加水稀释到100.0mL,取20.0mL于烧杯中,用cmol·L-1的AgNO3标准溶液滴定至终点(用Na2CrO4,作指示剂),消耗AgNO3标准溶液VmL,则产品中BiOCl的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某活动小组利用废铁屑(含少量S等元素)为原料制备硫酸亚铁铵晶体[(NH4)2SO4·FeSO4 ·6H2O](M=392g/mol),设计如图所示装置(夹持仪器略去)。
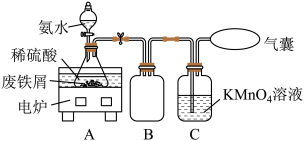
称取一定量的废铁屑于锥形瓶中,加入适量的稀硫酸,在通风橱中置于50 ~60°C热水浴中加热充分反应。待锥形瓶中溶液冷却至室温后加入氨水,使其反应完全,制得浅绿色悬浊液。
(1)在实验中选择50~60℃热水浴的原因是___________________ 。
(2)装置B的作用是_______________________________ 。
(3)检验制得的(NH4)2SO4·FeSO4·6H2O中是否含有Fe3+的方法:将硫酸亚铁铵晶体用加热煮沸过的蒸馏水溶解,然后滴加________________ (填化学式)。
(4)产品中杂质Fe3+的定量分析:
①配制Fe3+浓度为0.1 mg/mL的标准溶液100mL。称取________ (精确到0.1)mg高纯度的硫酸铁铵[(NH4)Fe(SO4)2·12H2O],加入20.00 mL经处理的去离子水。振荡溶解后,加入2 mol·L-1HBr溶液1mL和1mol·L-1KSCN溶液0.5mL,加水配成100mL溶液。
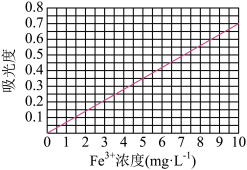
②将上述溶液稀释成浓度分别为0.2、1.0、 3.0、5.0、 7.0、 10.0(单位: mg·L-1)的溶液。分别测定不同浓度溶液对光的吸收程度(吸光度),并将测定结果绘制成如图所示曲线。取硫酸亚铁铵产品,按步骤①配得产品硫酸亚铁铵溶液10mL,稀释至100mL,然后测定稀释后溶液的吸光度,两次测得的吸光度分别为0.590、0.610,则该兴趣小组所配产品硫酸亚铁铵溶液中所含Fe3+浓度为_______ mg·L-1。
(5)称取mg产品,将产品用加热煮沸的蒸馏水溶解,配成250mL溶液,取出100mL放入锥形瓶中,用c mol·L-1KMnO4溶液滴定,消耗KMnO4溶液VmL,则硫酸亚铁铵晶体的纯度为___________ (用含c、V、m的代数式表示,化简)。滴定时,下列滴定方式中,最合理的是___________ (填字母)。
A.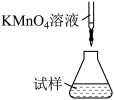 B.
B.  C.
C. 
若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,实验结果将会_________ (填“偏大”“偏小”或“无影响”。)

称取一定量的废铁屑于锥形瓶中,加入适量的稀硫酸,在通风橱中置于50 ~60°C热水浴中加热充分反应。待锥形瓶中溶液冷却至室温后加入氨水,使其反应完全,制得浅绿色悬浊液。
(1)在实验中选择50~60℃热水浴的原因是
(2)装置B的作用是
(3)检验制得的(NH4)2SO4·FeSO4·6H2O中是否含有Fe3+的方法:将硫酸亚铁铵晶体用加热煮沸过的蒸馏水溶解,然后滴加
(4)产品中杂质Fe3+的定量分析:
①配制Fe3+浓度为0.1 mg/mL的标准溶液100mL。称取
②将上述溶液稀释成浓度分别为0.2、1.0、 3.0、5.0、 7.0、 10.0(单位: mg·L-1)的溶液。分别测定不同浓度溶液对光的吸收程度(吸光度),并将测定结果绘制成如图所示曲线。取硫酸亚铁铵产品,按步骤①配得产品硫酸亚铁铵溶液10mL,稀释至100mL,然后测定稀释后溶液的吸光度,两次测得的吸光度分别为0.590、0.610,则该兴趣小组所配产品硫酸亚铁铵溶液中所含Fe3+浓度为

(5)称取mg产品,将产品用加热煮沸的蒸馏水溶解,配成250mL溶液,取出100mL放入锥形瓶中,用c mol·L-1KMnO4溶液滴定,消耗KMnO4溶液VmL,则硫酸亚铁铵晶体的纯度为
A.
 B.
B.  C.
C. 
若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,实验结果将会
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】化工试剂草酸钠常用于制革、烟火、整理织物等。纯 为白色晶体,溶于水,不溶于乙醇,有还原性,
为白色晶体,溶于水,不溶于乙醇,有还原性,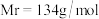 。实验室可用标准
。实验室可用标准 溶液测定市售草酸钠中
溶液测定市售草酸钠中 的质量分数(假设杂质不与
的质量分数(假设杂质不与 反应)。
反应)。
准确称取2.680g草酸钠样品溶于水后,将溶液转移至100mL容量瓶中,加水稀释至刻度制成100mL溶液,每次取20.00mL溶液于锥形瓶中,加足量稀硫酸酸化,作被测试样。然后用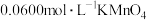 标准溶液进行滴定。
标准溶液进行滴定。
(1)用高锰酸钾标准溶液滴定被测试样,写出滴定过程中的离子反应方程式_______ 。
(2)滴定终点的实验现象为_______ 。
(3)滴定管使用前需进行润洗,润洗操作为_______ 。
(4)重复滴定4次,并记录 溶液的终了读数。实验数据如下表所示(假设每次实验滴定管中的初始读数均相同)。
溶液的终了读数。实验数据如下表所示(假设每次实验滴定管中的初始读数均相同)。
据此计算出草酸钠样品中 的质量分数为
的质量分数为_______ 。
(5)以下操作会造成测定结果偏高的是_______ (填字母编号)。
A.读取标准液读数时,滴定前仰视,滴定到终点后俯视
B.滴定管用蒸馏水洗涤后,未润洗立即装入标准 溶液
溶液
C.锥形瓶用蒸馏水洗净后又用待测草酸钠溶液润洗
D.滴定前滴定管尖嘴中有气泡,滴定后气泡消失
(6)实验过程中需要进行多次滴定,滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):检漏→蒸馏水洗涤→_______ →开始滴定。
A.烘干
B.装入滴定液至零刻度以上
C.右手拿住滴定管使其倾斜30°,左手迅速打开活塞
D.调整滴定液液面至零刻度或零刻度以下
E.用洗耳球吹出润洗液
F.用滴定液润洗2至3次
G.静置1分钟左右,记录起始读数
 为白色晶体,溶于水,不溶于乙醇,有还原性,
为白色晶体,溶于水,不溶于乙醇,有还原性,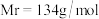 。实验室可用标准
。实验室可用标准 溶液测定市售草酸钠中
溶液测定市售草酸钠中 的质量分数(假设杂质不与
的质量分数(假设杂质不与 反应)。
反应)。准确称取2.680g草酸钠样品溶于水后,将溶液转移至100mL容量瓶中,加水稀释至刻度制成100mL溶液,每次取20.00mL溶液于锥形瓶中,加足量稀硫酸酸化,作被测试样。然后用
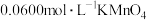 标准溶液进行滴定。
标准溶液进行滴定。(1)用高锰酸钾标准溶液滴定被测试样,写出滴定过程中的离子反应方程式
(2)滴定终点的实验现象为
(3)滴定管使用前需进行润洗,润洗操作为
(4)重复滴定4次,并记录
 溶液的终了读数。实验数据如下表所示(假设每次实验滴定管中的初始读数均相同)。
溶液的终了读数。实验数据如下表所示(假设每次实验滴定管中的初始读数均相同)。实验 | 稀释后样品体积/mL | 滴定消耗 |
1 | 20.00 | 20.02mL |
2 | 20.00 | 21.30mL |
3 | 20.00 | 19.98mL |
4 | 20.00 | 20.00mL |
 的质量分数为
的质量分数为(5)以下操作会造成测定结果偏高的是
A.读取标准液读数时,滴定前仰视,滴定到终点后俯视
B.滴定管用蒸馏水洗涤后,未润洗立即装入标准
 溶液
溶液C.锥形瓶用蒸馏水洗净后又用待测草酸钠溶液润洗
D.滴定前滴定管尖嘴中有气泡,滴定后气泡消失
(6)实验过程中需要进行多次滴定,滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):检漏→蒸馏水洗涤→
A.烘干
B.装入滴定液至零刻度以上
C.右手拿住滴定管使其倾斜30°,左手迅速打开活塞
D.调整滴定液液面至零刻度或零刻度以下
E.用洗耳球吹出润洗液
F.用滴定液润洗2至3次
G.静置1分钟左右,记录起始读数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】金属镓(Ga)的合金可用作半导体材料,以下是工业上从湿法提锌浸渣中提取金属镓和铅,回收锌的工艺:
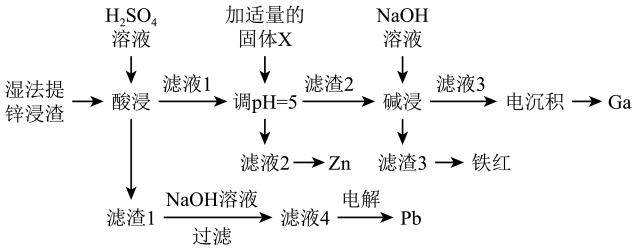
已知:①湿法提锌浸渣中含有Pb(Ⅱ)、Zn(Ⅱ)、Fe(Ⅲ)、Ga(Ⅲ)等;
②已知Ga(OH)3、Zn(OH)2、Pb(OH)2和Al(OH)3具有类似的化学性质;
③25℃时,Fe(OH)3、Ga(OH)3、Zn(OH)2的溶度积依次是2.8×10-39、1.4×10-34、3×10-17。
回答下列问题:
(1)滤渣1的成分是___ (写化学式),固体X为____ 。
(2)NaOH溶液“碱浸”的离子方程式为___ ,检验滤渣3是否洗涤干净的方法是___ 。
(3)“电沉积”时Ga在___ 沉积(填“阴极”或“阳极”),该电极反应式为___ 。
(4)滤渣1中提取Pb的方法是:用NaOH溶液浸取滤渣1生成HPbO ,然后再电解得到Pb。写出生成HPbO
,然后再电解得到Pb。写出生成HPbO 的离子方程式
的离子方程式___ 。
(5)研究人员用络合滴定法测定滤液2中Zn2+含量的方法是:取100mL滤液2,加水稀释至1L,用滴定管量取25.00mL于锥形瓶中,以二甲酚橙为指示剂,加入试剂使pH稳定在5—6之间,用0.0100mol/L的EDTA标准溶液(用Na2H2Y·2H2O配制)滴定,已知滴定反应为Zn2++H2Y2-=ZnY2-+2H+,当溶液由紫红色变为黄色时即为终点。重复上述操作2次,记录实验数据如下表,则滤液2中Zn2+的浓度为____ g/L。用滴定管量取25.00mL溶液时,滴定管用蒸馏水洗过后没有润洗,则测得滤液2中Zn2+的浓度___ (填“偏大”“偏小”或“无影响”)。

已知:①湿法提锌浸渣中含有Pb(Ⅱ)、Zn(Ⅱ)、Fe(Ⅲ)、Ga(Ⅲ)等;
②已知Ga(OH)3、Zn(OH)2、Pb(OH)2和Al(OH)3具有类似的化学性质;
③25℃时,Fe(OH)3、Ga(OH)3、Zn(OH)2的溶度积依次是2.8×10-39、1.4×10-34、3×10-17。
回答下列问题:
(1)滤渣1的成分是
(2)NaOH溶液“碱浸”的离子方程式为
(3)“电沉积”时Ga在
(4)滤渣1中提取Pb的方法是:用NaOH溶液浸取滤渣1生成HPbO
 ,然后再电解得到Pb。写出生成HPbO
,然后再电解得到Pb。写出生成HPbO 的离子方程式
的离子方程式(5)研究人员用络合滴定法测定滤液2中Zn2+含量的方法是:取100mL滤液2,加水稀释至1L,用滴定管量取25.00mL于锥形瓶中,以二甲酚橙为指示剂,加入试剂使pH稳定在5—6之间,用0.0100mol/L的EDTA标准溶液(用Na2H2Y·2H2O配制)滴定,已知滴定反应为Zn2++H2Y2-=ZnY2-+2H+,当溶液由紫红色变为黄色时即为终点。重复上述操作2次,记录实验数据如下表,则滤液2中Zn2+的浓度为
| 序号 | 滴定前读数 | 滴定后读数 |
| 1 | 0.00 | 20.01 |
| 2 | 1.00 | 20.99 |
| 3 | 0.00 | 21.10 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】锰及其化合物在现代工业和国防建设中具有十分重要的地位。金属锰的提炼方式主要有热还原法和电解法两种,热还原法得到的锰纯度在95-98%之间,电解法得到的锰(简称电解锰),其纯度可达99.7~99.9%以上。
(1)锰锌铁氧体是当前广泛使用的一种隐形涂料,其化学组成为MnxZn1-xFe2O4(铁为+3价),其中当锰锌铁氧体中n(Zn):n(Fe)=2:5时,它对雷达波的吸收能力最强。
① 锰锌铁氧体中锰元素的化合价为_______ 。
② 当雷达波吸收能力最强时,该物质的化学式为________ (改写成氧化物的形式)。
(2)写出以MnO2和Al粉为原料,利用热还原法制备Mn的化学方程式:________ 。
(3)工业上以菱锰矿(主要成分是MnCO3,含有Fe2+、Co2+、Ni2+等杂质金属离子)为原料制备电解锰的流程图如下所示。
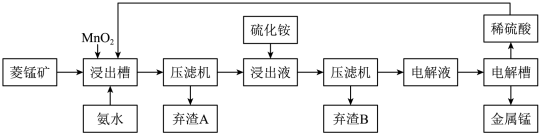
生成氢氧化物的pH如下表:
① 浸出槽中发生多个反应:如主要成分与硫酸的反应、MnO2与Fe2+间的氧化还原反应等,写出这两个反应的离子方程式:___________________ 、____________________ 。
② 加入氨水的目的是为除去杂质,根据流程图及表中数据,pH 应调控在_____ 范围内。常温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=4时溶液中c(Fe3+)=__________ 。
③ 加入硫化铵是为除去剩余的Ni2+,反应的离子方程式为____________________ 。
④ 写出电解硫酸锰溶液制取金属锰的化学方程式:________________________ 。
(1)锰锌铁氧体是当前广泛使用的一种隐形涂料,其化学组成为MnxZn1-xFe2O4(铁为+3价),其中当锰锌铁氧体中n(Zn):n(Fe)=2:5时,它对雷达波的吸收能力最强。
① 锰锌铁氧体中锰元素的化合价为
② 当雷达波吸收能力最强时,该物质的化学式为
(2)写出以MnO2和Al粉为原料,利用热还原法制备Mn的化学方程式:
(3)工业上以菱锰矿(主要成分是MnCO3,含有Fe2+、Co2+、Ni2+等杂质金属离子)为原料制备电解锰的流程图如下所示。

生成氢氧化物的pH如下表:
物质 | Fe(OH)2 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
| 开始沉淀时pH | 7.5 | 2.l | 7.7 | 7.6 | 8.3 |
| 完全沉淀时pH | 9.7 | 3.7 | 8.5 | 8.2 | 9.8 |
② 加入氨水的目的是为除去杂质,根据流程图及表中数据,pH 应调控在
③ 加入硫化铵是为除去剩余的Ni2+,反应的离子方程式为
④ 写出电解硫酸锰溶液制取金属锰的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

相关反应的热化学方程式为:
反应Ⅰ: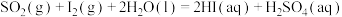 ,
,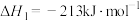
反应Ⅱ: ,
,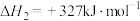
反应Ⅲ: ,
,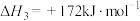
①总反应的热化学方程式为: ,
,
___________ 。
②在该过程中 和
和___________ 对总反应起到催化剂作用;使用了催化剂,总反应的
___________ (填“增大”“减小”或“不变”)。
(2)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
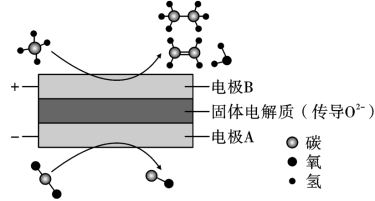
①阴极上的反应式:___________ 。
②若生成的乙烯和乙烷的体积比为2:1,则消耗的CH4和CO2体积比为___________ 。
(3)EF-H2O2-FeOx法可用于水体中有机污染物降解,其反应机理如图所示。X微粒的化学式为___________ ,阴极附近 参与反应的离子方程式为
参与反应的离子方程式为___________ 。

(1)以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

相关反应的热化学方程式为:
反应Ⅰ:
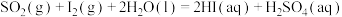 ,
,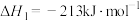
反应Ⅱ:
 ,
,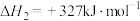
反应Ⅲ:
 ,
,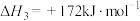
①总反应的热化学方程式为:
 ,
,
②在该过程中
 和
和
(2)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:

①阴极上的反应式:
②若生成的乙烯和乙烷的体积比为2:1,则消耗的CH4和CO2体积比为
(3)EF-H2O2-FeOx法可用于水体中有机污染物降解,其反应机理如图所示。X微粒的化学式为
 参与反应的离子方程式为
参与反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】亚硫酸钠用途广泛,可作漂白剂、显影剂、防护剂等。近年来,以SO2、NH3和NaCl为原料生产无水亚硫酸钠的新方法得到发展。生产流程如图所示:

完成下列填空:
(1)中学化学实验室实现上述流程中“分离器”作用的操作名称是:_________ ;所需玻璃仪器有___________________________ 。
(2)“反应液1”是由SO2通入14.8%氨水形成的亚硫酸铵溶液,在60℃~80℃时,不断搅拌,加入NaCl细晶体,就有无水亚硫酸钠析出,析出无水亚硫酸钠的离子反应方程式为____________________________ 。
(3)在“反应液2”通入足量SO2后,溶液中的阴离子除OH-外还有:_______________ ;在“反应液3”中通入足量NH3的目的是:__________________________________________ 。
(4)该生产方法的原料利用率(每制100g无水亚硫酸钠,各物质的消耗量及副产品物量)如表:
副产品NH4Cl的理论值a为:_________ ;它与NH4Cl实际值有差别的可能原因是:_________________ 。
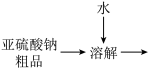
(5)无水亚硫酸钠粗品常用重结晶的方法进行精制,请完善以下能实现物料循环的精制亚硫酸钠操作的流程图。______________

完成下列填空:
(1)中学化学实验室实现上述流程中“分离器”作用的操作名称是:
(2)“反应液1”是由SO2通入14.8%氨水形成的亚硫酸铵溶液,在60℃~80℃时,不断搅拌,加入NaCl细晶体,就有无水亚硫酸钠析出,析出无水亚硫酸钠的离子反应方程式为
(3)在“反应液2”通入足量SO2后,溶液中的阴离子除OH-外还有:
(4)该生产方法的原料利用率(每制100g无水亚硫酸钠,各物质的消耗量及副产品物量)如表:
| 原料 | 理论值 | 实际值 | 利用率 |
| SO2 | 80.79 | 54.4 | 93.36% |
| NaCl | 92.86 | 101.0 | 91.94% |
| NH3 | 26.98 | 30.5 | 88.46% |
| 副产品NH4Cl | a | 87.1 | …… |
副产品NH4Cl的理论值a为:
(5)无水亚硫酸钠粗品常用重结晶的方法进行精制,请完善以下能实现物料循环的精制亚硫酸钠操作的流程图。

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
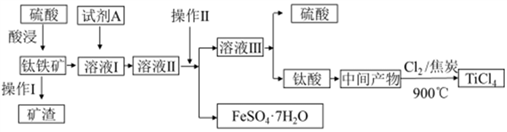
【推荐2】金属钛被称为“21世纪金属”。工业上由钛铁矿(主要成分FeTiO3)制备TiCl4的主要工艺流程如下:
回答下列问题:
(1)已知酸浸反应FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+TiOSO4(aq)+2H2O,则FeTiO3中铁元素的化合价为_____ 。加热TiOSO4溶液可制备TiO2·nH2O 胶体,其反应的化学方程式为__________ 。为提高钛铁矿的酸浸出率,可采取的办法除粉碎矿石外,还可以采取的办法有__________ 、_______ (写出两种方法)。
(2)加入A的目的是____ (填字母)。
A.防止Fe2+被氧化 B.与Fe3+反应 C.防Fe2+水解
溶液II经操作II可得副产品FeSO4·7H2O,则操作II包括浓缩、冷却、_____ 、_____ 。
(3)常温下,若溶液II中Fe2+的浓度为0.49mol/L,为防止生成Fe(OH)2沉淀,溶液的pH不超过_____ 。(已知Ksp[Fe(OH)2]=4.9×10-17)
(4)钛酸煅烧得中间产物的化学方程式为H2TiO3(s) TiO2(s)+H2O(g),上述工艺流程中,氯气与焦炭均足量时生成TiCl4的化学方程式为
TiO2(s)+H2O(g),上述工艺流程中,氯气与焦炭均足量时生成TiCl4的化学方程式为__________________________ 。
(5)可利用TiO2通过下述两种方法制备金属钛:
方法一: 通过以下反应制备金属钛
①TiO2 (s)+2Cl2(g) TiCl4(g)+O2(g) △ H=+ 151kJ/mol
TiCl4(g)+O2(g) △ H=+ 151kJ/mol
②TiCl4+2Mg 2MgCl2+Ti
2MgCl2+Ti
方法二: 将TiO2作阴极,石墨作阳极,熔融CaO为电解液,碳块作电解槽池,电解TiO2制得钛,阳极上一定生成的气体是___________ ,可能生成的气体是______________ 。
从绿色化学角度,你认为上述两种方法中那种更好,并说明理由___________________________

回答下列问题:
(1)已知酸浸反应FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+TiOSO4(aq)+2H2O,则FeTiO3中铁元素的化合价为
(2)加入A的目的是
A.防止Fe2+被氧化 B.与Fe3+反应 C.防Fe2+水解
溶液II经操作II可得副产品FeSO4·7H2O,则操作II包括浓缩、冷却、
(3)常温下,若溶液II中Fe2+的浓度为0.49mol/L,为防止生成Fe(OH)2沉淀,溶液的pH不超过
(4)钛酸煅烧得中间产物的化学方程式为H2TiO3(s)
 TiO2(s)+H2O(g),上述工艺流程中,氯气与焦炭均足量时生成TiCl4的化学方程式为
TiO2(s)+H2O(g),上述工艺流程中,氯气与焦炭均足量时生成TiCl4的化学方程式为(5)可利用TiO2通过下述两种方法制备金属钛:
方法一: 通过以下反应制备金属钛
①TiO2 (s)+2Cl2(g)
 TiCl4(g)+O2(g) △ H=+ 151kJ/mol
TiCl4(g)+O2(g) △ H=+ 151kJ/mol②TiCl4+2Mg
 2MgCl2+Ti
2MgCl2+Ti方法二: 将TiO2作阴极,石墨作阳极,熔融CaO为电解液,碳块作电解槽池,电解TiO2制得钛,阳极上一定生成的气体是
从绿色化学角度,你认为上述两种方法中那种更好,并说明理由
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】由碳酸锰矿(主要成分 ,还含有
,还含有 、
、 、
、 、
、 等)中提取金属锰的一种流程如图:
等)中提取金属锰的一种流程如图:
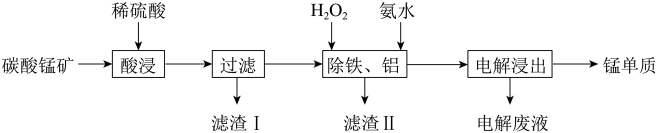
(1)“酸浸”过程中,提高锰元素浸出率的措施有:适当提高酸的浓度、_______ (填一种)。
(2)滤渣Ⅰ的主要成分是_______ 。(填化学式)
(3)保持其他条件不变,在不同温度下对碳酸锰矿进行酸浸,锰元素的浸出率随时间变化如图所示,则酸浸的最佳温度和时间分别是_______ 。

(4)已知“酸浸”后溶液中锰元素只以 形式存在,则“酸浸”中发生氧化还原反应的离子方程式为
形式存在,则“酸浸”中发生氧化还原反应的离子方程式为_______ 。
(5)结合图表,“除铁、铝”时加入氨水控制反应液pH的范围为_______ 。写出除铝的离子方程式:_______ 。
提取过程中相关金属离子生成氢氧化物沉淀的pH
 ,还含有
,还含有 、
、 、
、 、
、 等)中提取金属锰的一种流程如图:
等)中提取金属锰的一种流程如图:
(1)“酸浸”过程中,提高锰元素浸出率的措施有:适当提高酸的浓度、
(2)滤渣Ⅰ的主要成分是
(3)保持其他条件不变,在不同温度下对碳酸锰矿进行酸浸,锰元素的浸出率随时间变化如图所示,则酸浸的最佳温度和时间分别是

(4)已知“酸浸”后溶液中锰元素只以
 形式存在,则“酸浸”中发生氧化还原反应的离子方程式为
形式存在,则“酸浸”中发生氧化还原反应的离子方程式为(5)结合图表,“除铁、铝”时加入氨水控制反应液pH的范围为
提取过程中相关金属离子生成氢氧化物沉淀的pH
| 金属离子 |  |  |  |  |
| 开始沉淀的pH | 1.8 | 5.8 | 3.0 | 7.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.8 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】Al与NaOH的水溶液能反应,而镁不反应。然而一位同学将镁条放入饱和碳酸氢钠溶液时,却观察到反应迅速发生,且有大量气体放出。查阅资料显示:①镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物;②Mg与沸水能明显发生反应。为探究反应原理,同学们设计了如下实验方案并验证产物。
【实验I】:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
(1)提出假设
该同学对反应中产生的白色不溶物作出如下猜测:
猜测1:可能是_______ 。
猜测2:可能是 。
。
猜测3:可能是碱式碳酸镁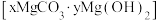 。
。
(2)设计定性实验确定产物并验证猜测:
(3)设计定量实验确定实验I的产物:称取实验I中所得干燥、纯净的白色不溶物31.0g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验前后装置A增重1.8g,装置B增重13.2g,试确定白色不溶物的化学式_______ 。
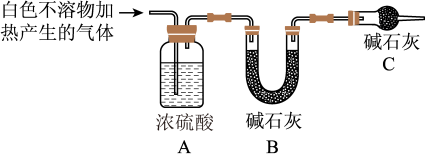
(4)根据资料显示以及实验现象,有同学认为,上述反应可能就是镁分别与水、与碳酸氢钠两个直接反应的共同结果。请你分别写出这两个可能发生的化学反应的化学方程式:_______ ,_______ 。
【实验I】:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
(1)提出假设
该同学对反应中产生的白色不溶物作出如下猜测:
猜测1:可能是
猜测2:可能是
 。
。猜测3:可能是碱式碳酸镁
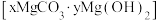 。
。(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 预期现象和结论 |
| 【实验II】 | 将实验I中收集的气体点燃 | 现象及结论 |
| 【实验III】 | 取实验I中的白色不溶物,洗涤,加入足量 |  |
| 【实验IV】 | 取实验I中的滤液,向其中加入BaCl2稀溶液 | 产生白色沉淀;溶液中存在 |

(4)根据资料显示以及实验现象,有同学认为,上述反应可能就是镁分别与水、与碳酸氢钠两个直接反应的共同结果。请你分别写出这两个可能发生的化学反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以废旧锂离子电池正极材料(主要成分为镍钴锰酸锂,还有少量铝箔和含铁化合物)为原料,回收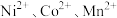 的过程可表示为:
的过程可表示为:

(1)“酸浸”时,三价镍、三价钴、四价锰转化为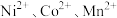 进入溶液。该过程中
进入溶液。该过程中 的作用是
的作用是___________ 。
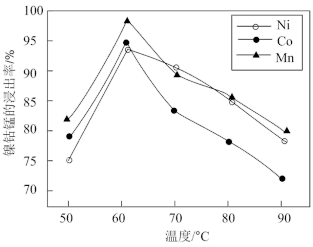
(2)“酸浸”时,保持其他条件相同,搅拌相同时间,测得不同温度下镍、钴、锰的浸出率如图所示。 时浸出率达到最大,可能的原因是
时浸出率达到最大,可能的原因是___________ 。
(3)物质X可调节溶液的 ,X为
,X为___________ (填序号)。
A. B.
B. C.
C.
(4)回收液可用于合成锂离子电池正极材料,合成前需测定其中 等离子的浓度。
等离子的浓度。
测定原理:用过量标准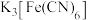 溶液氧化经预处理的吸收液样品中的
溶液氧化经预处理的吸收液样品中的 ,再用标准
,再用标准 溶液滴定过量的
溶液滴定过量的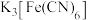 。
。
反应方程式为: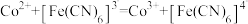 。
。
测定过程:取预处理后的回收液样品 ,向其中加入
,向其中加入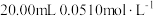
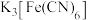 溶液,充分反应;再用
溶液,充分反应;再用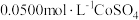 溶液滴定反应后的溶液,消耗
溶液滴定反应后的溶液,消耗 溶液
溶液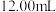 。
。
数据分析:计算预处理后的回收液样品中 的物质的量浓度
的物质的量浓度___________ 。(写出计算过程)
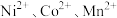 的过程可表示为:
的过程可表示为:
(1)“酸浸”时,三价镍、三价钴、四价锰转化为
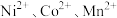 进入溶液。该过程中
进入溶液。该过程中 的作用是
的作用是(2)“酸浸”时,保持其他条件相同,搅拌相同时间,测得不同温度下镍、钴、锰的浸出率如图所示。
 时浸出率达到最大,可能的原因是
时浸出率达到最大,可能的原因是
(3)物质X可调节溶液的
 ,X为
,X为A.
 B.
B. C.
C.
(4)回收液可用于合成锂离子电池正极材料,合成前需测定其中
 等离子的浓度。
等离子的浓度。测定原理:用过量标准
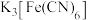 溶液氧化经预处理的吸收液样品中的
溶液氧化经预处理的吸收液样品中的 ,再用标准
,再用标准 溶液滴定过量的
溶液滴定过量的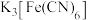 。
。反应方程式为:
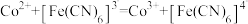 。
。测定过程:取预处理后的回收液样品
 ,向其中加入
,向其中加入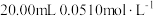
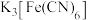 溶液,充分反应;再用
溶液,充分反应;再用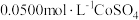 溶液滴定反应后的溶液,消耗
溶液滴定反应后的溶液,消耗 溶液
溶液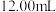 。
。数据分析:计算预处理后的回收液样品中
 的物质的量浓度
的物质的量浓度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】化学实验小组的同学在实验室里发现桌上有瓶敞口放置已久的NaOH溶液,他们对溶质的成分产生了探究的欲望。
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】猜想一:NaOH溶液部分变质
猜想二:NaOH溶液完全变质
【实验探究】
(1)氢氧化钠溶液变质的原因为_____ (用化学方程式表示)。
(2)小组的同学设计了如下实验进行探究,请根据表中内容填写:
上述步骤一中,滴加过量CaCl2溶液的目的是_____ 。
【实验反思】
(3)下列物质中①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代步骤一中CaCl2溶液的是__ (填序号)。
(4)步骤二中用另外一种试剂代替酚酞试液也能得出同样的结论,发生反应的化学方程式为________ 。
(5)通过探究,实验室中的氢氧化钠应密封保存。
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】猜想一:NaOH溶液部分变质
猜想二:NaOH溶液完全变质
【实验探究】
(1)氢氧化钠溶液变质的原因为
(2)小组的同学设计了如下实验进行探究,请根据表中内容填写:
| 实验步骤 | 现象 | 结论 | |
| 步骤一 | 取少量NaOH溶液样品于试管中,向其中滴加过量的CaCl2溶液 | 产生白色沉淀 | 猜想 |
| 步骤二 | 过滤,向滤液中滴加酚酞试液 | 溶液变红色 | |
上述步骤一中,滴加过量CaCl2溶液的目的是
【实验反思】
(3)下列物质中①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代步骤一中CaCl2溶液的是
(4)步骤二中用另外一种试剂代替酚酞试液也能得出同样的结论,发生反应的化学方程式为
(5)通过探究,实验室中的氢氧化钠应密封保存。
您最近一年使用:0次



