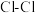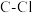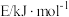反应2A(g)+B(g) 3C(g)+D(g),△H=akJ/mol。反应过程中的能量变化如图所示。回答下列问题:
3C(g)+D(g),△H=akJ/mol。反应过程中的能量变化如图所示。回答下列问题:
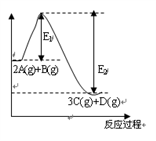
⑴a_____ 0 (填“<”“>”“=”)。
⑵该反应的熵变 △s_______ 0 (填“<”“>”“=”),在_________ (填“高”、“低”、“任何”)温度能正向自发进行。
⑶若反应在恒容恒温条件下进行,且A、B的起始浓度分别为 5mol/L、2mol/L,10min后平衡时D的浓度为1mol/L,C物质的量为3mol,则容器的容积为_________ L,B的转化率为________ ,A的反应速率为______________ ,化学平衡常数为___________ 。
 3C(g)+D(g),△H=akJ/mol。反应过程中的能量变化如图所示。回答下列问题:
3C(g)+D(g),△H=akJ/mol。反应过程中的能量变化如图所示。回答下列问题:
⑴a
⑵该反应的熵变 △s
⑶若反应在恒容恒温条件下进行,且A、B的起始浓度分别为 5mol/L、2mol/L,10min后平衡时D的浓度为1mol/L,C物质的量为3mol,则容器的容积为
更新时间:2018-06-25 19:46:39
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】断开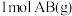 分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为
分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为 键的键能。下表列出了一些化学键的键能E:
键的键能。下表列出了一些化学键的键能E:
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应为_____________ (填“吸热”或“放热”)反应,其中
_____________ (用含有a、b的关系式表示)。
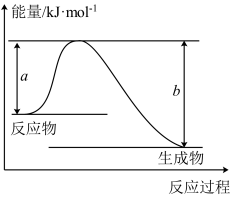
(2)若图示中表示反应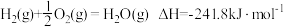 ,
,
①则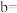
_____________  ,x=
,x=_____________ .
②此热化学方程式的意义是__________________________ 。
③画出此热化学方程式对应的焓变示意图______________ 。

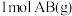 分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为
分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为 键的键能。下表列出了一些化学键的键能E:
键的键能。下表列出了一些化学键的键能E:化学键 |
|
|
|
|
|
|
|
| 436 | 247 | x | 330 | 413 | 463 | 431 |
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应为


(2)若图示中表示反应
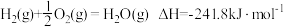 ,
,①则
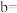
 ,x=
,x=②此热化学方程式的意义是
③画出此热化学方程式对应的焓变示意图

您最近一年使用:0次
【推荐2】2SO2(g)+O2(g)=2SO3(g)反应过程中的能量变化如图所示。已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH1=-99 kJ/mol。请回答下列问题:

(1) 图中A、C分别表示________ 、________ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________ ;
(2) 图中ΔH=__________ kJ/mol;
(3) 已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH_______ 。

(1) 图中A、C分别表示
(2) 图中ΔH=
(3) 已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+260 kJ·mol-1 ①
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1 ②
则CH4与O2反应生成CO和H2的热化学方程式为______
(2)0.3 mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5 kJ热量,其表示乙硼烷(B2H6)燃烧热的热化学方程式为:__________
(3)含Ba(OH)2 1 mol的稀溶液与足量稀盐酸反应,放出114.6 kJ的热量,表示该反应中和热的热化学方程式为:__________
(4)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。

图中A、C分别表示_______ 、_______ ,E的大小对该反应的反应热有无影响?______ 。图中ΔH=________ kJ·mol-1。
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+260 kJ·mol-1 ①
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1 ②
则CH4与O2反应生成CO和H2的热化学方程式为
(2)0.3 mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5 kJ热量,其表示乙硼烷(B2H6)燃烧热的热化学方程式为:
(3)含Ba(OH)2 1 mol的稀溶液与足量稀盐酸反应,放出114.6 kJ的热量,表示该反应中和热的热化学方程式为:
(4)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。

图中A、C分别表示
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】二氧化碳的排放越来越受到能源和环境领域的关注,其综合利用是目前研究的重要课题之一。一定温度下,在2L密闭容器中充入3molCO2和6molH2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测定H2的转化率[α(H2)]随时间的变化如图所示:
CH3OH(g)+H2O(g),测定H2的转化率[α(H2)]随时间的变化如图所示:

0~20min内,用CH3OH的浓度变化表示的平均反应速率:v(CH3OH)=____ mol•L-1•min-1。
 CH3OH(g)+H2O(g),测定H2的转化率[α(H2)]随时间的变化如图所示:
CH3OH(g)+H2O(g),测定H2的转化率[α(H2)]随时间的变化如图所示:
0~20min内,用CH3OH的浓度变化表示的平均反应速率:v(CH3OH)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知可逆反应aA2 +bB2 xX(反应物、生成物都是气体)。回答下列问题:
xX(反应物、生成物都是气体)。回答下列问题:
I.将一定量的两种反应物置于恒容绝热反应器中(与外部环境无热量交换的反应器),反应器内的温度与时间的关系如图:

(1)该反应是___ (填“吸”或“ 放”)热反应。
(2)下列关于该反应的叙述正确的是____ (填字母)。
a A点反应停止 b A点速率不为零
c 反应物的总能量大于生成物的 d B点正反应速率大于逆反应速率
II.将一定量的上述反应的反应物与生成物置于容积为2L的恒温恒容反应器中,反应器中各物质的物质的量与时间的关系如图:

(3)①反应前4 min物质x的物质的量的变化为_____ mol. .
②反应前4 min物质A2反应速率为_______
③该可逆反应的化学方程式为______ (物质X用A、B表示)。
④如果在4 min时升高反应体系的温度.则反应速率___ ( 填“增大“减小”或“不变")。
⑤如果在4min时加入2.4 mol Ne(Ne不参与该反应),则反应速率___ (填“增大”“减小”或“不变”)。
 xX(反应物、生成物都是气体)。回答下列问题:
xX(反应物、生成物都是气体)。回答下列问题:I.将一定量的两种反应物置于恒容绝热反应器中(与外部环境无热量交换的反应器),反应器内的温度与时间的关系如图:

(1)该反应是
(2)下列关于该反应的叙述正确的是
a A点反应停止 b A点速率不为零
c 反应物的总能量大于生成物的 d B点正反应速率大于逆反应速率
II.将一定量的上述反应的反应物与生成物置于容积为2L的恒温恒容反应器中,反应器中各物质的物质的量与时间的关系如图:

(3)①反应前4 min物质x的物质的量的变化为
②反应前4 min物质A2反应速率为
③该可逆反应的化学方程式为
④如果在4 min时升高反应体系的温度.则反应速率
⑤如果在4min时加入2.4 mol Ne(Ne不参与该反应),则反应速率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为__________________________ ,表中b_________ c(填“<”、“=”、“>”)。
(2)20s时,N2O4的的浓度为__________________ mol·L-1,0~20s内N2O4的平均反应速率为________________ ;
(3)该反应的平衡常数表达式K=___________________
在80℃时该反应的平衡常数K值为:______________ (保留到小数点后2位)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时____________ 。
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
| 时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0. 20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为
(2)20s时,N2O4的的浓度为
(3)该反应的平衡常数表达式K=
在80℃时该反应的平衡常数K值为:
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在10L 容器中,加入2mol SO2(g)和2mol NO2(g),保持温度恒定,发生反应:SO2(g)+ NO2(g)  SO3(g)+ NO(g),当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则
SO3(g)+ NO(g),当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则
(1)若在该容器中再继续加入1 mol SO2(g),则化学平衡将向_____________ 方向移动(选填“正反应”、“逆反应”、“不”),NO2(g)的转化率将_______________ (填“增大”、“减小”或“不变”),达到新的平衡状态时,容器中的SO2(g)的浓度是_________________ 。
(2)在其他条件不变的情况下,扩大容器的体积,平衡_____________ 移动(选填“向正反应方向”、“向逆反应方向”、“不”)。
 SO3(g)+ NO(g),当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则
SO3(g)+ NO(g),当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则(1)若在该容器中再继续加入1 mol SO2(g),则化学平衡将向
(2)在其他条件不变的情况下,扩大容器的体积,平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在常温下对反应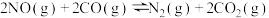 进行研究。
进行研究。
(1)若将3molNO和2molCO通入10L的恒容密闭容器中,在一定条件下发生上述反应,各组分的物质的量浓度随时间的变化情况如图所示。
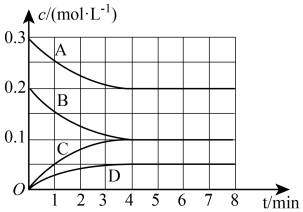
①图中曲线A表示___________ (填“NO”“CO”“ ”或“
”或“ ”,下同)的浓度变化,曲线C表示的是
”,下同)的浓度变化,曲线C表示的是___________ 的浓度变化。
②在0~4min内NO的平均反应速率,
___________ ,4min末 的浓度为
的浓度为___________ 。
③4min末,采用下列措施一定能加快上述反应速率的是___________ (填标号)。
A.升高体系的温度 B.充入一定量的O2
C.将容器体积变为5L D.充入一定量氦气
(2)下列叙述能说明上述反应已达到平衡状态的是___________ (填标号)。
a.容器内压强保持不变 b. 与
与 的物质的量之比为1:1
的物质的量之比为1:1
c.气体的密度保持不变 d.气体的平均相对分子质量保持不变
(3)根据图1数据计算该反应的平衡常数数值
___________ 。
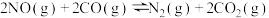 进行研究。
进行研究。(1)若将3molNO和2molCO通入10L的恒容密闭容器中,在一定条件下发生上述反应,各组分的物质的量浓度随时间的变化情况如图所示。

①图中曲线A表示
 ”或“
”或“ ”,下同)的浓度变化,曲线C表示的是
”,下同)的浓度变化,曲线C表示的是②在0~4min内NO的平均反应速率,

 的浓度为
的浓度为③4min末,采用下列措施一定能加快上述反应速率的是
A.升高体系的温度 B.充入一定量的O2
C.将容器体积变为5L D.充入一定量氦气
(2)下列叙述能说明上述反应已达到平衡状态的是
a.容器内压强保持不变 b.
 与
与 的物质的量之比为1:1
的物质的量之比为1:1c.气体的密度保持不变 d.气体的平均相对分子质量保持不变
(3)根据图1数据计算该反应的平衡常数数值

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某温度时,将2molCO与5molH2的混合气体充入容积为2L的密闭容器中,在催化剂的作用下发生反应:CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
(1)经过5min后,反应达到平衡,此时转移电子6mol。该反应的平衡常数为_______ 。V(H2)=_____ mol/(L·min)。若保持体积不变,再充入2mulCO和1.5mol CH3OH,此时v(正)___ v(逆)(填“>”“<”或“=”)。
(2)在其他条件不变的情况下,再增加2molCO与5molH2,达到新平衡时,CO的转化率____ (填“增大”“减小”或“不变”)。
(3)下列不能说明该反应已达到平衡状态的是__________
a.CH3OH 的质量不变 b.混合气体的平均相对分子质量不再改变
c.V逆(CO)=2V正(H2) d.混合气体的密度不再发生改变
(4)在一定压强下,容积为VL的容器充入a molCO与2amolH2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。

则p1_____ p2(填“大于”“小于” 或“等于”,下同),△H_____ 0。该反应在_______ ( 填“高温” 或“低温” )下能自发进行。
(5)能使该反应的反应速率增大,且平衡向正反应方向移动的是_____ 。
a.及时分离除CH3OH气体 b.适当升高温度
c.增大H2的浓度 d.选择高效催化剂
(6)下面四个选项是四位学生在学习化学反应速率与化学反应限度以后,联系化工生产实际所发表的看法,你认为不正确的是_______ 。
a.化学反应速率理论可指导怎样在一定时间内快出产品
b.有效碰撞理论可指导怎样提高原料的转化率
c.勒夏特列原理可指导怎样使用有限原料多出产品
d.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
 CH3OH(g)。
CH3OH(g)。(1)经过5min后,反应达到平衡,此时转移电子6mol。该反应的平衡常数为
(2)在其他条件不变的情况下,再增加2molCO与5molH2,达到新平衡时,CO的转化率
(3)下列不能说明该反应已达到平衡状态的是
a.CH3OH 的质量不变 b.混合气体的平均相对分子质量不再改变
c.V逆(CO)=2V正(H2) d.混合气体的密度不再发生改变
(4)在一定压强下,容积为VL的容器充入a molCO与2amolH2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。

则p1
(5)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离除CH3OH气体 b.适当升高温度
c.增大H2的浓度 d.选择高效催化剂
(6)下面四个选项是四位学生在学习化学反应速率与化学反应限度以后,联系化工生产实际所发表的看法,你认为不正确的是
a.化学反应速率理论可指导怎样在一定时间内快出产品
b.有效碰撞理论可指导怎样提高原料的转化率
c.勒夏特列原理可指导怎样使用有限原料多出产品
d.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】向平底烧瓶中放入氢氧化钡晶体[Ba(OH)2·8H2O]和氯化铵晶体,塞紧瓶塞。在瓶底和木板间滴少量水(如图所示)。一段时间后,发现瓶内固态物质变稀,有液体生成,瓶壁变冷,小木板黏结在烧瓶底部。这时打开瓶塞,烧瓶中散发出刺鼻的气味。
(1)下列有关该实验的结论正确的是___ (填字母)。
A.自发反应一定是放热反应
B.自发反应一定是吸热反应
C.有的吸热反应也能自发进行
D.吸热反应不能自发进行
(2)发生反应的化学方程式为_______________________________________ 。
(3)从化学反应进行方向的角度解释上述现象:________________ 。

(1)下列有关该实验的结论正确的是
A.自发反应一定是放热反应
B.自发反应一定是吸热反应
C.有的吸热反应也能自发进行
D.吸热反应不能自发进行
(2)发生反应的化学方程式为
(3)从化学反应进行方向的角度解释上述现象:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】合成氨工艺是人工固氮最重要的途径。回答下列问题:
(1)工业合成氨的反应为 。在容积为2L的密闭容器中,通入amolN2和bmolH2,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN2.
。在容积为2L的密闭容器中,通入amolN2和bmolH2,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN2.
①该反应的平衡常数表达式
_____ 。
②达到平衡时,H2的转化率为_____ 。
③在tmin内以NH3的浓度变化表示的化学反应速率为_____ 。
④若把容器的容积缩小一半,则正反应速率_____ (填“增大”、“减小”或“不变”,下同),N2的转化率_____ 。
(2)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。铜氨液吸收CO适宜的生产条件是
。铜氨液吸收CO适宜的生产条件是_____ 。
(3)合成氨工业中采用循环操作,主要是为了_____ (填序号)。
a.增大化学反应速率b.提高平衡混合物中氨的含量
c.降低氨的沸点d.提高氮气和氢气的利用率
(4)合成氨气的氢气可由天然气制备。
①其反应为
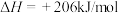 ,该反应自发的条件是
,该反应自发的条件是_____ (填“低温自发”、“高温自发”或“任意温度自发”)。
②为提高CH4的平衡转化率,可采用的措施是_____ (填序号)。
a.使用合适的催化剂b.采用较高的温度
c.采用较高的压强d.延长反应时间
(1)工业合成氨的反应为
 。在容积为2L的密闭容器中,通入amolN2和bmolH2,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN2.
。在容积为2L的密闭容器中,通入amolN2和bmolH2,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN2.①该反应的平衡常数表达式

②达到平衡时,H2的转化率为
③在tmin内以NH3的浓度变化表示的化学反应速率为
④若把容器的容积缩小一半,则正反应速率
(2)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:

 。铜氨液吸收CO适宜的生产条件是
。铜氨液吸收CO适宜的生产条件是(3)合成氨工业中采用循环操作,主要是为了
a.增大化学反应速率b.提高平衡混合物中氨的含量
c.降低氨的沸点d.提高氮气和氢气的利用率
(4)合成氨气的氢气可由天然气制备。
①其反应为

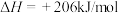 ,该反应自发的条件是
,该反应自发的条件是②为提高CH4的平衡转化率,可采用的措施是
a.使用合适的催化剂b.采用较高的温度
c.采用较高的压强d.延长反应时间
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】NO是一种性质活泼的大气污染物,它能与很多物质发生反应。
Ⅰ、在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2 (g)体系中,n(NO)随时间的变化如表:
2NO2 (g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=_____ 。已知: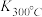 >
>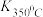 ,则该反应是
,则该反应是___ 热反应。
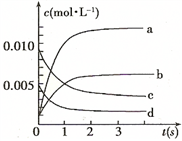
(2)下图中表示NO2的变化的曲线是___________ 。用O2表示从0-2 s内该反应的平均速率
v =___________ 。
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________ 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
Ⅱ、超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO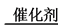 2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)上述条件下反应能够自发进行,则该反应的△H_____ 0(填写“>”、“<”、“=”)。
(2)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是________ 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(3)某同学设计了三组实验,实验条件已经填在下面实验设计表中,分析表格我们可以看出该同学的实验目的主要是研究_______________ 和_____________________ 对化学反应速率的影响。
Ⅰ、在2L密闭容器内,800℃时反应:2NO(g)+O2(g)
 2NO2 (g)体系中,n(NO)随时间的变化如表:
2NO2 (g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=
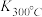 >
>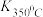 ,则该反应是
,则该反应是(2)下图中表示NO2的变化的曲线是
v =

(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
Ⅱ、超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO
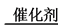 2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(mol/L) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)(mol/L) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)上述条件下反应能够自发进行,则该反应的△H
(2)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(3)某同学设计了三组实验,实验条件已经填在下面实验设计表中,分析表格我们可以看出该同学的实验目的主要是研究
| 实验编号 | T(℃) | NO初始浓(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
| Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | 124 |
您最近一年使用:0次