在10L 容器中,加入2mol SO2(g)和2mol NO2(g),保持温度恒定,发生反应:SO2(g)+ NO2(g)  SO3(g)+ NO(g),当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则
SO3(g)+ NO(g),当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则
(1)若在该容器中再继续加入1 mol SO2(g),则化学平衡将向_____________ 方向移动(选填“正反应”、“逆反应”、“不”),NO2(g)的转化率将_______________ (填“增大”、“减小”或“不变”),达到新的平衡状态时,容器中的SO2(g)的浓度是_________________ 。
(2)在其他条件不变的情况下,扩大容器的体积,平衡_____________ 移动(选填“向正反应方向”、“向逆反应方向”、“不”)。
 SO3(g)+ NO(g),当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则
SO3(g)+ NO(g),当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则(1)若在该容器中再继续加入1 mol SO2(g),则化学平衡将向
(2)在其他条件不变的情况下,扩大容器的体积,平衡
更新时间:2020-10-29 06:33:26
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】向一容积不变的密闭容器中充入一定量A和B,发生如下反应: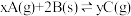 ;
; 。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
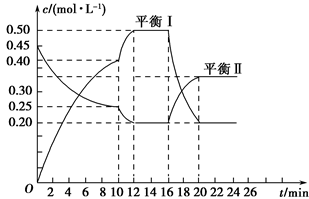
(1)用A的浓度变化表示该反应0~10 min内的平均反应速率v(A)=_____ ;达到平衡状态Ⅰ时A的转化率为_______ ;
(2)根据图示可确定x:y=___________ ;
(3)0~10 min容器内压强___________ (填“变大”,“不变”或“变小”)
(4)推测第10 min引起曲线变化的反应条件可能是_______ (填序号);第16 min引起曲线变化的反应条件可能是_____ (填序号);
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
(5)能说明该反应达到化学平衡状态的是___________(填序号)
(6)能使该反应的反应速率增大,且平衡向正反应方向移动的是___________。
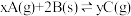 ;
; 。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
(1)用A的浓度变化表示该反应0~10 min内的平均反应速率v(A)=
(2)根据图示可确定x:y=
(3)0~10 min容器内压强
(4)推测第10 min引起曲线变化的反应条件可能是
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
(5)能说明该反应达到化学平衡状态的是___________(填序号)
| A.容器内压强不再改变 | B.c(A):c(C)=1:2 |
| C.气体密度不再改变 | D.v正(A)=2v逆(C) |
| A.及时分离出C气体 | B.适当升高温度 |
| C.增大A的浓度 | D.选择高效催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将二氧化碳转化为高附加值化学品是目前研究的热点之一,甲醇是重要的化工原料和优良的替代燃料,因此加氢制甲醇被广泛关注。在催化剂作用下主要发生以下反应。
I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol−1
Ⅱ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=+41kJ·mol−1
Ⅲ.CO(g)+2H2(g)⇌CH3OH(g) ΔH3
在 ,
, ,CO2(g)、H2(g)以物质的量浓度1:3投料,以一定流速通过不同Cu-ZnO与Cu-ZnO@SiO2催化剂,图a和b为催化反应CO2转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、
,CO2(g)、H2(g)以物质的量浓度1:3投料,以一定流速通过不同Cu-ZnO与Cu-ZnO@SiO2催化剂,图a和b为催化反应CO2转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、 和H2O。
和H2O。

(1)分析在该压强下的最适合反应条件为_______ 。
(2)推测在一定温度范围内,随着反应温度的升高,CO2转化率增大,但甲醇选择性降低的原因是_______ 。
I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol−1
Ⅱ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=+41kJ·mol−1
Ⅲ.CO(g)+2H2(g)⇌CH3OH(g) ΔH3
在
 ,
, ,CO2(g)、H2(g)以物质的量浓度1:3投料,以一定流速通过不同Cu-ZnO与Cu-ZnO@SiO2催化剂,图a和b为催化反应CO2转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、
,CO2(g)、H2(g)以物质的量浓度1:3投料,以一定流速通过不同Cu-ZnO与Cu-ZnO@SiO2催化剂,图a和b为催化反应CO2转化率、甲醇选择性、甲醇收率随温度的变化,反应的产物只有甲醇、 和H2O。
和H2O。
(1)分析在该压强下的最适合反应条件为
(2)推测在一定温度范围内,随着反应温度的升高,CO2转化率增大,但甲醇选择性降低的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在2020年中央经济工作会议上,我国明确提出“碳达峰”与“碳中和”目标。使利用CO2合成高价值化学品更突显其重要性。
Ⅰ.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应起始物质的量如表:
(1)达到平衡时,CO2的体积分数φ①_____ φ②(填“>”“<”或“=”)。
(2)当_____ = v逆(H2)时,说明反应在条件②达到平衡状态。
v逆(H2)时,说明反应在条件②达到平衡状态。
Ⅱ.利用CH4超干重整CO2的催化转化如图所示:
(3)CH4与CO2超干重整反应的方程式为_____ 。
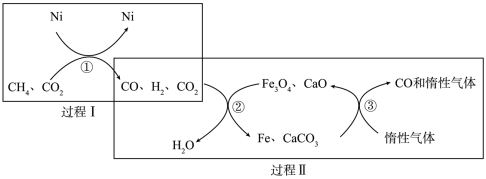
(4)有关转化过程,下列说法正确的是_____ (填序号)。
a.过程Ⅰ中CO2未参与反应
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO2,有利于反应正向进行
d.转化③中Fe与CaCO3反应的物质的量之比为4∶3
Ⅲ.通过下列反应可实现CO2的再转化,合成CO、CH4:
①CO2(g)+4H2(g)=CH4(g)+2H2O(g)ΔH<0
②CO2(g)+H2(g)=CO(g)+H2O(g)ΔH>0
在密闭容器中通入3mol的H2和1mol的CO2,分别在压强为1MPa和10MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。
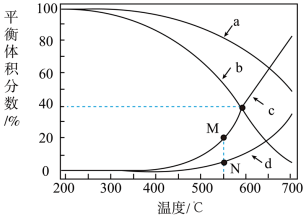
(5)1MPa时,表示CH4和CO平衡体积分数随温度变化关系的曲线分别是_____ 和_____ 。M点平衡体积分数高于N点的原因是_____ 。
(6)图中当CH4和CO平衡体积分数均为40%时,若容器的体积为1L,该温度下反应①的平衡常数K的值为_____ 。
Ⅰ.工业上可以利用CO2和H2合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH<0。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应起始物质的量如表:
| 反应条件 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| ①恒温恒容 | 1 | 3 | 0 | 0 |
| ②绝热恒容 | 0 | 0 | 1 | 1 |
(1)达到平衡时,CO2的体积分数φ①
(2)当
 v逆(H2)时,说明反应在条件②达到平衡状态。
v逆(H2)时,说明反应在条件②达到平衡状态。Ⅱ.利用CH4超干重整CO2的催化转化如图所示:
(3)CH4与CO2超干重整反应的方程式为

(4)有关转化过程,下列说法正确的是
a.过程Ⅰ中CO2未参与反应
b.过程Ⅱ实现了含碳物质与含氢物质的分离
c.转化②中CaO消耗过程中的CO2,有利于反应正向进行
d.转化③中Fe与CaCO3反应的物质的量之比为4∶3
Ⅲ.通过下列反应可实现CO2的再转化,合成CO、CH4:
①CO2(g)+4H2(g)=CH4(g)+2H2O(g)ΔH<0
②CO2(g)+H2(g)=CO(g)+H2O(g)ΔH>0
在密闭容器中通入3mol的H2和1mol的CO2,分别在压强为1MPa和10MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。

(5)1MPa时,表示CH4和CO平衡体积分数随温度变化关系的曲线分别是
(6)图中当CH4和CO平衡体积分数均为40%时,若容器的体积为1L,该温度下反应①的平衡常数K的值为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.在水溶液中橙红色的Cr2O72—与黄色的CrO42—有下列平衡关系:Cr2O72—+H2O 2CrO42—+2H+,把重铬酸钾(K2Cr2O7)溶于水配成稀溶液是橙色。
2CrO42—+2H+,把重铬酸钾(K2Cr2O7)溶于水配成稀溶液是橙色。
(1)向上述溶液中加入NaOH溶液,溶液呈___________ 色,因为___________ 。
(2)向已加入NaOH溶液的(1)溶液中再加入过量稀H2SO4,则溶液呈___________ 色,因为_______________ 。
Ⅱ.将CoCl2溶于浓盐酸中能形成CoCl42—。溶液中存在如下平衡:CoCl42-(蓝色) + 6H2O Co(H2O)62+(粉红色)+ 4Cl-
Co(H2O)62+(粉红色)+ 4Cl-
(3)一般情况下,CoCl2溶液呈紫色,将盛有CoCl2溶液的试管放在热水中溶液逐渐变成蓝色,则正反应方向为___________ 反应(填“吸热”或“放热”)。
(4)该反应平衡常数表达式为______________________ ,加水稀释平衡向____________ 方向(填“正”或“逆”)移动。
(5)向溶液中加入少量AgNO3固体,溶液颜色变为_______ 色。
 2CrO42—+2H+,把重铬酸钾(K2Cr2O7)溶于水配成稀溶液是橙色。
2CrO42—+2H+,把重铬酸钾(K2Cr2O7)溶于水配成稀溶液是橙色。(1)向上述溶液中加入NaOH溶液,溶液呈
(2)向已加入NaOH溶液的(1)溶液中再加入过量稀H2SO4,则溶液呈
Ⅱ.将CoCl2溶于浓盐酸中能形成CoCl42—。溶液中存在如下平衡:CoCl42-(蓝色) + 6H2O
 Co(H2O)62+(粉红色)+ 4Cl-
Co(H2O)62+(粉红色)+ 4Cl-(3)一般情况下,CoCl2溶液呈紫色,将盛有CoCl2溶液的试管放在热水中溶液逐渐变成蓝色,则正反应方向为
(4)该反应平衡常数表达式为
(5)向溶液中加入少量AgNO3固体,溶液颜色变为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】煤气中主要的含硫杂质有H2S以及COS(有机硫),煤气燃烧后含硫杂质会转化成SO2从而引起大气污染。煤气中H2S的脱除程度已成为其洁净度的一个重要指标。回答下列问题:
(1)将H2S通入FeCl3溶液中,该反应的还原产物为___________ 。
(2)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法以及水解法等。
①COS的分子结构与CO2相似,COS的电子式为_____________ 。
②Br2的KOH溶液将COS氧化为硫酸盐和碳酸盐的离子方程式为_____________ 。
③已知断裂1mol化学键所需的能量如下:
H2还原COS发生的反应为H2(g)+COS(g) ═H2S(g)+CO(g),该反应的ΔH=________ kJ·mol-1。
④用活性α—Al2O3催化COS水解的反应为COS(g)+ H2 O(g) CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与
CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与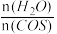 的关系如图2所示。
的关系如图2所示。
由图1可知,催化剂活性最大时对应的温度约为____________ ;由图2可知,P点时平衡常数K=_____
(保留2位有效数字)。
(3)常温下可发生反应:ZnS(s)+2H+(aq) Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=
Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=_______ [已知:Ksp(ZnS)=2.93×10-25;H2S电离常数;Ka1=9.5×10-8,Ka2=1.3×10-14]。
(1)将H2S通入FeCl3溶液中,该反应的还原产物为
(2)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法以及水解法等。
①COS的分子结构与CO2相似,COS的电子式为
②Br2的KOH溶液将COS氧化为硫酸盐和碳酸盐的离子方程式为
③已知断裂1mol化学键所需的能量如下:
| 化学键 | H—H | C═O | C═S | H—S | C≡O |
| E/kJ•mol-1 | 436 | 745 | 577 | 339 | 1072 |
H2还原COS发生的反应为H2(g)+COS(g) ═H2S(g)+CO(g),该反应的ΔH=
④用活性α—Al2O3催化COS水解的反应为COS(g)+ H2 O(g)
 CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与
CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与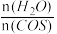 的关系如图2所示。
的关系如图2所示。

由图1可知,催化剂活性最大时对应的温度约为
(保留2位有效数字)。
(3)常温下可发生反应:ZnS(s)+2H+(aq)
 Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=
Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将4 mol N2O4放入2 L馆容密闭容器中发生反应N2O4(g) 2NO2(g),平衡体系中N2O4的体积分数(φ) 随温度的变化如图所示:
2NO2(g),平衡体系中N2O4的体积分数(φ) 随温度的变化如图所示:
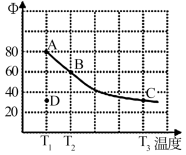
(1) D点v(正)___________ v(逆) (填“>、<或=")。
(2) A、B、C三点中平衡常数K的值最大的是___________ 点。T2时N2O4的平衡转化率为___________ 。
(3)若其条件不变,在T3原平衡基础上,再加入一定量NO2,达到新平衡时,与原平衡相比,NO2的体积分数___________ (填“增大、不变或减小”)。
 2NO2(g),平衡体系中N2O4的体积分数(φ) 随温度的变化如图所示:
2NO2(g),平衡体系中N2O4的体积分数(φ) 随温度的变化如图所示:
(1) D点v(正)
(2) A、B、C三点中平衡常数K的值最大的是
(3)若其条件不变,在T3原平衡基础上,再加入一定量NO2,达到新平衡时,与原平衡相比,NO2的体积分数
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)在密闭容器中充入2.0 mol CO和10 mol H2O(g),发生反应:CO(g)+H2O(g) CO2(g)+H2(g),800 ℃时反应达平衡,若K=1。求CO和H2O(g)的转化率
CO2(g)+H2(g),800 ℃时反应达平衡,若K=1。求CO和H2O(g)的转化率__________ 。
(2)PCl5的热分解反应如下:PCl5(g) PCl3(g)+Cl2(g)。
PCl3(g)+Cl2(g)。
①写出反应的平衡常数表达式_________ ;
②已知某温度下,在容积为10.0 L的密闭容器中充入 2.00 mol PCl5,达到平衡后,测得容器内PCl3的浓度为 0.150 mol/L。计算该温度下的平衡常数_________ 。
 CO2(g)+H2(g),800 ℃时反应达平衡,若K=1。求CO和H2O(g)的转化率
CO2(g)+H2(g),800 ℃时反应达平衡,若K=1。求CO和H2O(g)的转化率(2)PCl5的热分解反应如下:PCl5(g)
 PCl3(g)+Cl2(g)。
PCl3(g)+Cl2(g)。①写出反应的平衡常数表达式
②已知某温度下,在容积为10.0 L的密闭容器中充入 2.00 mol PCl5,达到平衡后,测得容器内PCl3的浓度为 0.150 mol/L。计算该温度下的平衡常数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】可通过下列方法合成中性肥料尿素:
第一步:
 (反应速率较快)
(反应速率较快)
第二步: (反应速率较慢)
(反应速率较慢)
第一步反应的平衡常数的表达式为
___________ 。
在1个 的密闭容器中加入
的密闭容器中加入 和
和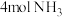 ,在一定条件下反应,
,在一定条件下反应, 时测得
时测得 和尿素的物质的量均为
和尿素的物质的量均为 ,
,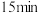 后
后 的物质的量为
的物质的量为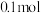 ,如图所示。若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则
,如图所示。若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则 内第一步中生成
内第一步中生成 (氨基甲酸铵)的平均反应速率为
(氨基甲酸铵)的平均反应速率为___________ 。
第一步:

 (反应速率较快)
(反应速率较快)第二步:
 (反应速率较慢)
(反应速率较慢)第一步反应的平衡常数的表达式为

在1个
 的密闭容器中加入
的密闭容器中加入 和
和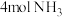 ,在一定条件下反应,
,在一定条件下反应, 时测得
时测得 和尿素的物质的量均为
和尿素的物质的量均为 ,
,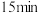 后
后 的物质的量为
的物质的量为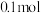 ,如图所示。若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则
,如图所示。若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则 内第一步中生成
内第一步中生成 (氨基甲酸铵)的平均反应速率为
(氨基甲酸铵)的平均反应速率为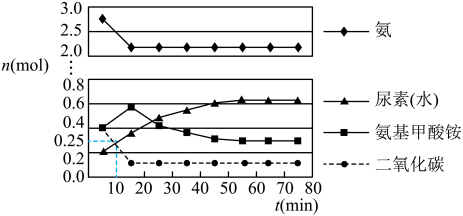
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)反应需要在闪电或极高温条件下发生,说明该反应_________ 。(填字母)
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g) 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表:
①该反应的△H_____ 0。(填“>”、“=”或“<”)
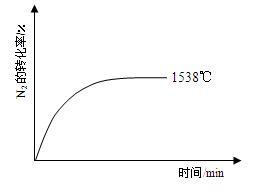
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如右图所示,请补充完成1760℃、2404℃时N2的转化率随时间变化的示意图。
________ 。
(3)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应N2(g)+O2(g) 2NO(g)达到平衡时NO的浓度
2NO(g)达到平衡时NO的浓度_______ 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
(1)反应需要在闪电或极高温条件下发生,说明该反应
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g)
 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表:| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
①该反应的△H
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如右图所示,请补充完成1760℃、2404℃时N2的转化率随时间变化的示意图。

(3)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应N2(g)+O2(g)
 2NO(g)达到平衡时NO的浓度
2NO(g)达到平衡时NO的浓度
您最近一年使用:0次



