已知A、B、C、D、E都是周期表中前四周期的元素,它们的原子序数依次增大。其中A元素原子的核外p电子数比s电子数少1。C是电负性最大的元素。D原子次外层电子数是最外层电子数2倍,E是第Ⅷ族中原子序数最小的元素。
(1)写出基态C原子的电子排布式_________________ 。
(2)A、B两种元素的第一电离能由大到小的顺序为______________ (用元素符号表示),原因是___________________ 。
(3)已知DC4常温下为气体,则该物质的晶体类型是_________ ,组成微粒的中心原子的轨道杂化类型为____________ ,空间构型是___________ 。
(4)Cu2+容易与AH3形成配离子[Cu(AH3)4]2+,但AC3不易与Cu2+形成配离子,其原因是______________________ 。
(5)A、B两元素分别与D形成的共价键中,极性较强的是__________ 。A、B两元素间能形成多种二元化合物,其中与A3—互为等电子体的物质的化学式为__________ 。
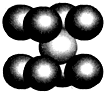
(6)已知E单质的晶胞如图所示,则晶体中E原子的配位数为__________ ,一个E的晶胞质量为___________ 。
(1)写出基态C原子的电子排布式
(2)A、B两种元素的第一电离能由大到小的顺序为
(3)已知DC4常温下为气体,则该物质的晶体类型是
(4)Cu2+容易与AH3形成配离子[Cu(AH3)4]2+,但AC3不易与Cu2+形成配离子,其原因是
(5)A、B两元素分别与D形成的共价键中,极性较强的是
(6)已知E单质的晶胞如图所示,则晶体中E原子的配位数为

更新时间:2018-06-25 18:48:44
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图所示,M原子位于晶胞的棱上与内部。该晶胞中M原子的个数为___________ ,该材料的化学式为___________ 。

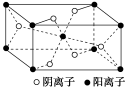
(2)Mg与某元素形成的化合物的晶胞如图所示,晶胞中阴离子与阳离子的个数比是___________ 。
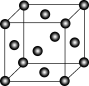
(3)Cu2O在稀硫酸中生成Cu和CuSO4.铜晶胞结构如图所示,铜晶体中每个铜原子周围距离最近的铜原子数目为___________ 。
(1)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图所示,M原子位于晶胞的棱上与内部。该晶胞中M原子的个数为

(2)Mg与某元素形成的化合物的晶胞如图所示,晶胞中阴离子与阳离子的个数比是

(3)Cu2O在稀硫酸中生成Cu和CuSO4.铜晶胞结构如图所示,铜晶体中每个铜原子周围距离最近的铜原子数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】iCo2S4@g-C3N4-CNT是一类很有发展前途的化合物电催化剂。回答下列问题:
(1)基态Co2+的价层电子排布图(轨道表达式)为_________ ;基态S原子电子占据最高能级的电子云轮廓图为______________ 形。
(2)g-C3N4(结构片段如图1,环上化学键与苯环类似)可由三聚氰胺(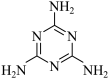 )与(NH4)2SO4共热制得。
)与(NH4)2SO4共热制得。
①g-C3N4分子中环上的氮原子、碳原子杂化方式依次为________ 、_____ 。
②SO42—的空间构型为__________________ 。
③三聚氰胺分子中含σ键______ 个,它不溶于冷水,溶于热水,其主要原因是 ______________________ 。
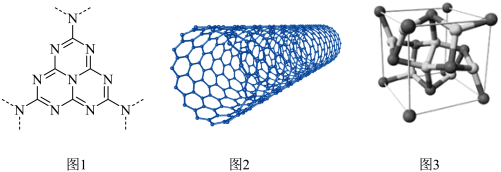
(3)碳纳米管(CNT,结构如图2)具有良好的导电性,其原因是______________ 。
(4)CoS2具有 AB2型立方结构(如图3),晶胞参数为553.4pm。设NA为阿伏加 德罗常数的值,则晶体的密度为________________ g•cm—3(列出计算式) 。
(1)基态Co2+的价层电子排布图(轨道表达式)为
(2)g-C3N4(结构片段如图1,环上化学键与苯环类似)可由三聚氰胺(
 )与(NH4)2SO4共热制得。
)与(NH4)2SO4共热制得。①g-C3N4分子中环上的氮原子、碳原子杂化方式依次为
②SO42—的空间构型为
③三聚氰胺分子中含σ键

(3)碳纳米管(CNT,结构如图2)具有良好的导电性,其原因是
(4)CoS2具有 AB2型立方结构(如图3),晶胞参数为553.4pm。设NA为阿伏加 德罗常数的值,则晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】过渡金属及其化合物在化工、医药、材料等领域有着广泛的应用。已知锆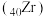 位于第
位于第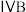 族,根据要求回答下列问题:
族,根据要求回答下列问题:
(1)铜元素在元素周期表的位置为_______ 基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
(2)形成铬锆铜合金的元素中,基态原子中未成对电子最多的是_______ (填元素符号)。
(3) 能与
能与 形成具有对称空间结构的
形成具有对称空间结构的 。
。
① 的
的 键角
键角_______ (填“>”、“=”或“<”) 的
的 键角。
键角。
②若 中两个
中两个 分别被
分别被 取代,能得到
取代,能得到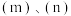 两种不同结构的
两种不同结构的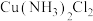 :
:
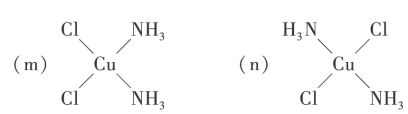
 的空间构型是
的空间构型是_______ ;在水中的溶解度: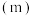
_______ 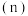 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
③ 与
与 具有相同的空间构型,但
具有相同的空间构型,但 不易与
不易与 形成配离子,理由是
形成配离子,理由是_______ 。
(4)下表是 与
与 的部分电离能数据,
的部分电离能数据, 大于
大于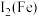 的主要原因是
的主要原因是_______ 。
(5)向 溶液中滴加
溶液中滴加 溶液后,经提纯、结晶后可得到
溶液后,经提纯、结晶后可得到 普鲁士蓝蓝色晶体。
普鲁士蓝蓝色晶体。
①通过_______ 实验可确定该晶体结构。
②可溶性氰化物(如 )有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是
)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是_______ 。
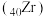 位于第
位于第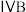 族,根据要求回答下列问题:
族,根据要求回答下列问题:(1)铜元素在元素周期表的位置为
 原子的核外电子排布式为
原子的核外电子排布式为(2)形成铬锆铜合金的元素中,基态原子中未成对电子最多的是
(3)
 能与
能与 形成具有对称空间结构的
形成具有对称空间结构的 。
。①
 的
的 键角
键角 的
的 键角。
键角。②若
 中两个
中两个 分别被
分别被 取代,能得到
取代,能得到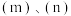 两种不同结构的
两种不同结构的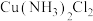 :
: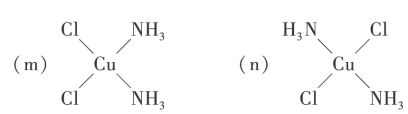
 的空间构型是
的空间构型是
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。③
 与
与 具有相同的空间构型,但
具有相同的空间构型,但 不易与
不易与 形成配离子,理由是
形成配离子,理由是(4)下表是
 与
与 的部分电离能数据,
的部分电离能数据, 大于
大于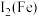 的主要原因是
的主要原因是| 元素 |  |  |
第一电离能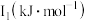 | 759 | 746 |
第二电离能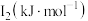 | 1561 | 1958 |
 溶液中滴加
溶液中滴加 溶液后,经提纯、结晶后可得到
溶液后,经提纯、结晶后可得到 普鲁士蓝蓝色晶体。
普鲁士蓝蓝色晶体。①通过
②可溶性氰化物(如
 )有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是
)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氯亚铂酸钾( )是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(
)是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(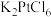 )为原料制备
)为原料制备 ,相关物质性质如下表:
,相关物质性质如下表:
Ⅰ.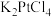 的制备
的制备
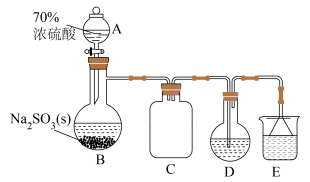
取10.00g氯铂酸钾(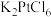 )溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原
)溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原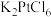 可得
可得 。
。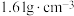 ,其物质的量浓度为
,其物质的量浓度为_____  。
。
(2)为使仪器A中的浓硫酸顺利滴下,需进行的操作为_____ 。
(3)仪器B的名称为_____ ,装置C的作用是_____ 。
(4)装置D中反应的化学方程式为_____ ,装置E中的试剂可选用_____ (填序号)。
A.氨水 B.NaOH溶液 C.澄清石灰水
(5)反应结束后,拆除装置,向装置D中加入足量无水乙醇,经过滤、洗涤、干燥,得红色固体6.25g。
①加入无水乙醇的目的是_____ 。
②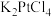 的产率为
的产率为_____ (结果保留三位有效数字)。_____ 。
(7)奥铂中H-N-H的键角大于1,2-环已二胺中H-N-H的键角,原因是_____ 。
(8)1,2-环己二胺的沸点(190℃)高于1,2-环戊二胺(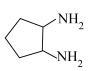 )的沸点(170℃),其主要原因是
)的沸点(170℃),其主要原因是_____ 。
 )是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(
)是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(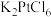 )为原料制备
)为原料制备 ,相关物质性质如下表:
,相关物质性质如下表:| 物质 | 性质 |
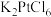 | 黄色粉末,溶于热水,微溶于冷水,几乎不溶于乙醇 |
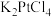 | 红色固体,溶于水,不溶于乙醇,高温易分解 |
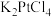 的制备
的制备取10.00g氯铂酸钾(
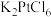 )溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原
)溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原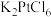 可得
可得 。
。
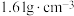 ,其物质的量浓度为
,其物质的量浓度为 。
。(2)为使仪器A中的浓硫酸顺利滴下,需进行的操作为
(3)仪器B的名称为
(4)装置D中反应的化学方程式为
A.氨水 B.NaOH溶液 C.澄清石灰水
(5)反应结束后,拆除装置,向装置D中加入足量无水乙醇,经过滤、洗涤、干燥,得红色固体6.25g。
①加入无水乙醇的目的是
②
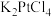 的产率为
的产率为Ⅱ.奥铂(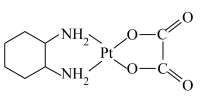 )是一种稳定的水溶性广谱抗肿瘤试剂,1,2-环己二胺(
)是一种稳定的水溶性广谱抗肿瘤试剂,1,2-环己二胺( )是制备奥铂的原料之一。
)是制备奥铂的原料之一。
(7)奥铂中H-N-H的键角大于1,2-环已二胺中H-N-H的键角,原因是
(8)1,2-环己二胺的沸点(190℃)高于1,2-环戊二胺(
 )的沸点(170℃),其主要原因是
)的沸点(170℃),其主要原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】W、X、Y、Z、N是短周期元素且其中只有一种金属元素,它们的核电荷数依次增大。
(1)W单质的化学式为___________ ,Z元素原子核外有___________ 个原子轨道填充了电子。
(2)Y、Z和N三种元素第一电离能由大到小的顺序为___________ (填元素符号)。
(3)X与Z两元素的电负性较大的是___________ (填元素符号)。
(4)Z元素原子共有___________ 种不同运动状态的电子。
| 元素 | 元素性质或原子结构 |
| W | 原子核内无中子 |
| X | 原子核外s能级上的电子总数与p能级上的电子总数相等 |
| Y | 元素的离子半径在该周期中最小 |
| Z | 原子核外p能级上的电子总数比s能级上的电子总数多2 |
| N | 最外层电子数比次外层电子数少1 |
(2)Y、Z和N三种元素第一电离能由大到小的顺序为
(3)X与Z两元素的电负性较大的是
(4)Z元素原子共有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①元素:A_______ 、B_______ 、C_______ 、D______ 、E______
②B、C、D、E四种元素的第一电离能大小顺序是:___________ 。
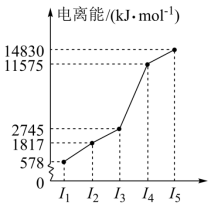
(2)如图是A~F元素中某种元素的部分电离能,由此可判断该元素是___________ 。F元素位于周期表的___________ 区,此区元素的价电子层结构特点是___________ 。
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。(1)请用元素符号完成下列空白:
①元素:A
②B、C、D、E四种元素的第一电离能大小顺序是:
(2)如图是A~F元素中某种元素的部分电离能,由此可判断该元素是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】Cu可形成多种配合物,一水硫酸四氨合铜晶体[Cu(NH3)4SO4·H2O]常用作杀虫剂,媒染剂等。常温下该物质可溶于水,难溶于乙醇,在空气中不稳定,受热时易发生分解。某化学兴趣小组制备[Cu(NH3)4]SO4·H2O晶体并测定其纯度。根据下列信息回答问题:
(1)[Cu(NH3)4]SO4中的中心离子为______ ,若[Cu(NH3)4]2+具有对称的空间结构,且当其中的两个NH3被两个Cl-取代时,能到两种不同结构的产物,则[Cu(NH3)4]2+的空间结构为______ 。
(2)将氨水逐滴加入硫酸铜溶液中,现象如图:
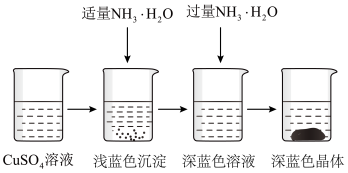
向硫酸铜溶液中加入适量氨水产生浅蓝色沉淀,已知其成分为Cu2(OH)2SO4,生成此沉淀的离子方程式为______ 。继续滴加氨水,溶液变为深蓝色,由该过程可知______ (填“H2O”或“NH3”)与Cu2+形成的配位键更稳定。
(3)向深蓝色溶液中加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O,加乙醇析出深蓝色晶体的原因是_____ ;再经过过滤、洗涤、干燥可得到深蓝色晶体,以下最合适的洗涤液为_____ 。
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
(4)产品纯度的测定。精确称取mg晶体溶于适量水,然后逐滴加入足量NaOH溶液,并将样品液中的氨全部蒸出,用V1mL0.5000mol/L的盐酸标准溶液完全吸收。吸收液用甲基橙作指示剂,用0.5000mol/LNaOH标准溶液滴定锥形瓶中过剩的盐酸,到终点时消耗V2mLNaOH溶液。样品中产品纯度的表达式为______ 。
(1)[Cu(NH3)4]SO4中的中心离子为
(2)将氨水逐滴加入硫酸铜溶液中,现象如图:

向硫酸铜溶液中加入适量氨水产生浅蓝色沉淀,已知其成分为Cu2(OH)2SO4,生成此沉淀的离子方程式为
(3)向深蓝色溶液中加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O,加乙醇析出深蓝色晶体的原因是
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
(4)产品纯度的测定。精确称取mg晶体溶于适量水,然后逐滴加入足量NaOH溶液,并将样品液中的氨全部蒸出,用V1mL0.5000mol/L的盐酸标准溶液完全吸收。吸收液用甲基橙作指示剂,用0.5000mol/LNaOH标准溶液滴定锥形瓶中过剩的盐酸,到终点时消耗V2mLNaOH溶液。样品中产品纯度的表达式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】周期表前四周期的元素a、b、c、d、e、f,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子中的未成对电子有3个;c的最外层电子数为其内层电子数的3倍,d和c同族;e元素的未成对电子在前四周期中最多;f的最外层有1个电子,但次外层有18个电子。试回答以下问题:
(1)d的电子排布式为___________ ,e的价电子排布式为___________ 。f的价电子排布图为___________ 。
(2)a和其他元素形成的二元化合物中,键角呈107°的分子中,空间构型为___________ ,极易与H+形成阳离子基团,该基团中心原子的杂化类型为___________ 。
(3)b、c、d中,第一电离能最大的是___________ (填元素符号),它们分别与a构成的化合物中,含有较强分子间作用力的分子有___________ 。
(4)[Ni(ba3)6]dc4中阴离子的立体构型是___________ 。Ni2+与ba3之间形成的化学键称为___________ ,提供孤电子对的成键原子是___________ ,提供的空轨道成键原子是___________ 。
(1)d的电子排布式为
(2)a和其他元素形成的二元化合物中,键角呈107°的分子中,空间构型为
(3)b、c、d中,第一电离能最大的是
(4)[Ni(ba3)6]dc4中阴离子的立体构型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铁是地球表面最丰富的金属之一,能形成多种配合物,铁系催化剂是工业生产中常用的催化剂。
(1)合成氨工业使用的催化剂是以铁为主体的多成分催化剂。
①NH3中N原子的杂化轨道类型是__________________________ 。
②N与O同属第二周期,N的第一电离能比O大的原因是_________ 。
③根据等电子体原理,写出一种NH4+是等电子体的微粒的化学式____________ 。
(2)二茂铁[(C5H5)2Fe]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如右所示,其中氢原子的化学环境完全相同。

①Fe的基态电子排布式为____________ 。
②二茂铁中Fe2+与环戊二烯离子(C5H5-)之间的化学键类型是_______________ 。
③1mol环戊二烯( )中含有σ键的数目为
)中含有σ键的数目为_________ 个。
(3)普鲁士蓝俗称铁蓝,结构如图所示,K+未画出),每隔一个立方体在立方体中心含有一个K+离子,普鲁士蓝中铁元素的化合价有+2和+3两种,其中Fe3+与Fe2+的个数比为:_____________ 。

(1)合成氨工业使用的催化剂是以铁为主体的多成分催化剂。
①NH3中N原子的杂化轨道类型是
②N与O同属第二周期,N的第一电离能比O大的原因是
③根据等电子体原理,写出一种NH4+是等电子体的微粒的化学式
(2)二茂铁[(C5H5)2Fe]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如右所示,其中氢原子的化学环境完全相同。

①Fe的基态电子排布式为
②二茂铁中Fe2+与环戊二烯离子(C5H5-)之间的化学键类型是
③1mol环戊二烯(
 )中含有σ键的数目为
)中含有σ键的数目为(3)普鲁士蓝俗称铁蓝,结构如图所示,K+未画出),每隔一个立方体在立方体中心含有一个K+离子,普鲁士蓝中铁元素的化合价有+2和+3两种,其中Fe3+与Fe2+的个数比为:

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
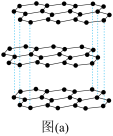
【推荐1】(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为___________ ,碳原子的杂化轨道类型为_________ 。

(2)SiCl4分子的中心原子的价层电子对数为__________ ,分子的立体构型为_______ 。
(3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。
SiX4的沸点依F、Cl、Br、I次序升高的原因是:______________________________________ 。
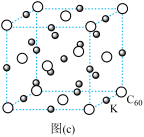
(4)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为_______________ ;其晶胞参数为1.4 nm,晶体密度为___________________________________ g·cm-3(列式并计算保留1位小数)。



(2)SiCl4分子的中心原子的价层电子对数为
(3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。
SiX4的沸点依F、Cl、Br、I次序升高的原因是:
(4)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】[化学——选修3:物质结构与性质]
具有自主知识产权、中国制造的C919,是一款与波音737MAX同等体量的民用飞机。制造C919需要大量的合金材料,其中包括钢,钢是现代社会的物质基础,钢中除含有铁外还含有碳和少量不可避免的硅、锰、磷、硫等元素。请回答下列有关问题:
(1)基态Mn原子的价电子排布式为___________ 。
(2)NO3-的立体构型名称为___________ ,其中心原子的杂化方式为___________ 。
(3)C、O、Si三种元素第一电离能由大到小的顺序是___________ 。
(4)写出和CN-互为等电子体的一种离子的电子式___________ 。
(5)铵盐大多易分解,NH4F和NH4Br两种盐中较易分解的是___________ (填化学式);理由是___________ 。
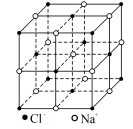
(6)氧化亚铁晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为apm,该晶体的密度为ρg·cm-3,则a=___________ (列出计算式即可,用NA表示阿伏伽德罗常数的值)。
具有自主知识产权、中国制造的C919,是一款与波音737MAX同等体量的民用飞机。制造C919需要大量的合金材料,其中包括钢,钢是现代社会的物质基础,钢中除含有铁外还含有碳和少量不可避免的硅、锰、磷、硫等元素。请回答下列有关问题:
(1)基态Mn原子的价电子排布式为
(2)NO3-的立体构型名称为
(3)C、O、Si三种元素第一电离能由大到小的顺序是
(4)写出和CN-互为等电子体的一种离子的电子式
(5)铵盐大多易分解,NH4F和NH4Br两种盐中较易分解的是
(6)氧化亚铁晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为apm,该晶体的密度为ρg·cm-3,则a=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】钴元素的用途广泛,据古文献记载:宜德时期青花瓷使用的颜料“苏勃泥青"是从一种进口钴毒矿[主要成分: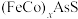 ]中提取出来的。
]中提取出来的。
I.
(1)金属钴原子的堆积方式为六方最密堆积,金属钴的晶胞结构如图所示,其中正六边形的面积为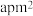 ,棱长为
,棱长为 ;每个Co距离最近且相等的Co原子数目为
;每个Co距离最近且相等的Co原子数目为___________ ;设阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为___________ (用含a、b、 的代数式表示)
的代数式表示) 。
。

Ⅱ.(三氯六氨合钴)是一种重要的化工产品,实验室制备过程如下:
①将一定量的氯化铵和浓氨水置于锥形瓶中,混合均匀;
②分批加入氯化钴粉末,边加边搅拌,直至溶液呈棕色稀浆;
③再向其中滴加 ,当固体完全溶解后,慢慢加入浓盐酸加热10~15min;
,当固体完全溶解后,慢慢加入浓盐酸加热10~15min;
④在室温下冷却,过滤,可得到橙黄色晶体。
(2) 是橙黄色晶体,配体分子的价层电子对互斥模型为
是橙黄色晶体,配体分子的价层电子对互斥模型为___________ 。
(3)“加热”应控温在60℃进行,控温方式可采取___________ 。
(4)沉淀滴定法测定产品中 的质量分数:
的质量分数:
i.准确称取mg的产品,配制成100mL溶液,移取20mL于锥形瓶中;
ii.滴加几滴 溶液为指示剂,用
溶液为指示剂,用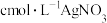 溶液滴定至终点;
溶液滴定至终点;
iii.重复滴定三次,消耗 溶液体积的平均值为
溶液体积的平均值为 ,计算晶体中Cr的质量分数。
,计算晶体中Cr的质量分数。
已知溶解度:
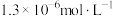 ,
, (砖红色)
(砖红色)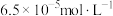
①ii中,滴定至终点的现象是___________ 。
②制备的晶体中 的质量分数是
的质量分数是___________ (列计算式即可)。
(5)已知 的立体结构如图,其中1~6处的小圆圈表示
的立体结构如图,其中1~6处的小圆圈表示 分子,且各相邻的
分子,且各相邻的 分子间的距离相等(图中虚线长度相等)。
分子间的距离相等(图中虚线长度相等)。 位于八面体的中心,若其中两个
位于八面体的中心,若其中两个 被
被 取代,所形成的
取代,所形成的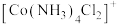 的结构的数目为
的结构的数目为___________ 。

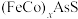 ]中提取出来的。
]中提取出来的。I.
(1)金属钴原子的堆积方式为六方最密堆积,金属钴的晶胞结构如图所示,其中正六边形的面积为
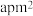 ,棱长为
,棱长为 ;每个Co距离最近且相等的Co原子数目为
;每个Co距离最近且相等的Co原子数目为 ,则该晶体的密度为
,则该晶体的密度为 的代数式表示)
的代数式表示) 。
。
Ⅱ.(三氯六氨合钴)是一种重要的化工产品,实验室制备过程如下:
①将一定量的氯化铵和浓氨水置于锥形瓶中,混合均匀;
②分批加入氯化钴粉末,边加边搅拌,直至溶液呈棕色稀浆;
③再向其中滴加
 ,当固体完全溶解后,慢慢加入浓盐酸加热10~15min;
,当固体完全溶解后,慢慢加入浓盐酸加热10~15min;④在室温下冷却,过滤,可得到橙黄色晶体。
(2)
 是橙黄色晶体,配体分子的价层电子对互斥模型为
是橙黄色晶体,配体分子的价层电子对互斥模型为(3)“加热”应控温在60℃进行,控温方式可采取
(4)沉淀滴定法测定产品中
 的质量分数:
的质量分数:i.准确称取mg的产品,配制成100mL溶液,移取20mL于锥形瓶中;
ii.滴加几滴
 溶液为指示剂,用
溶液为指示剂,用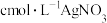 溶液滴定至终点;
溶液滴定至终点;iii.重复滴定三次,消耗
 溶液体积的平均值为
溶液体积的平均值为 ,计算晶体中Cr的质量分数。
,计算晶体中Cr的质量分数。已知溶解度:

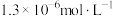 ,
, (砖红色)
(砖红色)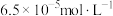
①ii中,滴定至终点的现象是
②制备的晶体中
 的质量分数是
的质量分数是(5)已知
 的立体结构如图,其中1~6处的小圆圈表示
的立体结构如图,其中1~6处的小圆圈表示 分子,且各相邻的
分子,且各相邻的 分子间的距离相等(图中虚线长度相等)。
分子间的距离相等(图中虚线长度相等)。 位于八面体的中心,若其中两个
位于八面体的中心,若其中两个 被
被 取代,所形成的
取代,所形成的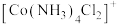 的结构的数目为
的结构的数目为
您最近一年使用:0次



