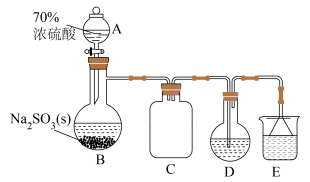
氯亚铂酸钾( )是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(
)是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(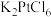 )为原料制备
)为原料制备 ,相关物质性质如下表:
,相关物质性质如下表:
Ⅰ.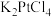 的制备
的制备
取10.00g氯铂酸钾(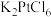 )溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原
)溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原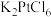 可得
可得 。
。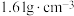 ,其物质的量浓度为
,其物质的量浓度为_____  。
。
(2)为使仪器A中的浓硫酸顺利滴下,需进行的操作为_____ 。
(3)仪器B的名称为_____ ,装置C的作用是_____ 。
(4)装置D中反应的化学方程式为_____ ,装置E中的试剂可选用_____ (填序号)。
A.氨水 B.NaOH溶液 C.澄清石灰水
(5)反应结束后,拆除装置,向装置D中加入足量无水乙醇,经过滤、洗涤、干燥,得红色固体6.25g。
①加入无水乙醇的目的是_____ 。
②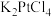 的产率为
的产率为_____ (结果保留三位有效数字)。_____ 。
(7)奥铂中H-N-H的键角大于1,2-环已二胺中H-N-H的键角,原因是_____ 。
(8)1,2-环己二胺的沸点(190℃)高于1,2-环戊二胺(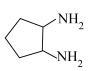 )的沸点(170℃),其主要原因是
)的沸点(170℃),其主要原因是_____ 。
 )是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(
)是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(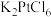 )为原料制备
)为原料制备 ,相关物质性质如下表:
,相关物质性质如下表:| 物质 | 性质 |
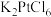 | 黄色粉末,溶于热水,微溶于冷水,几乎不溶于乙醇 |
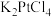 | 红色固体,溶于水,不溶于乙醇,高温易分解 |
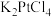 的制备
的制备取10.00g氯铂酸钾(
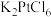 )溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原
)溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原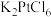 可得
可得 。
。
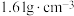 ,其物质的量浓度为
,其物质的量浓度为 。
。(2)为使仪器A中的浓硫酸顺利滴下,需进行的操作为
(3)仪器B的名称为
(4)装置D中反应的化学方程式为
A.氨水 B.NaOH溶液 C.澄清石灰水
(5)反应结束后,拆除装置,向装置D中加入足量无水乙醇,经过滤、洗涤、干燥,得红色固体6.25g。
①加入无水乙醇的目的是
②
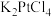 的产率为
的产率为Ⅱ.奥铂(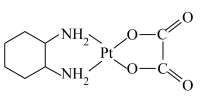 )是一种稳定的水溶性广谱抗肿瘤试剂,1,2-环己二胺(
)是一种稳定的水溶性广谱抗肿瘤试剂,1,2-环己二胺( )是制备奥铂的原料之一。
)是制备奥铂的原料之一。
(7)奥铂中H-N-H的键角大于1,2-环已二胺中H-N-H的键角,原因是
(8)1,2-环己二胺的沸点(190℃)高于1,2-环戊二胺(
 )的沸点(170℃),其主要原因是
)的沸点(170℃),其主要原因是
更新时间:2024-04-20 14:42:29
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某小组同学用如图所示装置进行铜与浓硫酸的反应,并探究产物的性质 (夹持装置已略去)。

(1)试管①中反应的化学方程式是_______ ;浓硫酸表现出了_______ 性和_______ 性。
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是_______ ;若试管②中的试剂为酸性KMnO4溶液,实验时,观察到溶液褪色,则说明生成的气体具有_______ 性。
(3)试管③中的试剂为NaOH溶液,其作用是_______ 。反应的化学方程式是_______ 。

(1)试管①中反应的化学方程式是
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是
(3)试管③中的试剂为NaOH溶液,其作用是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】二氧化硫是重要的化工原料,用途非常广泛。
(1)实验室用如图所示装置B制取连二亚硫酸钠(Na2S2O4)。
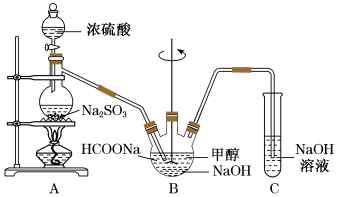
①实验中要控制生成SO2的速率,可采取的措施有(至少写一条)_________
②B装置中用甲醇作溶剂,C中NaOH的作用是__________ 。
(2)二氧化硫能够抑制细菌的滋生,可用作防腐剂,但必须严格按照国家标准使用。实验室用已知浓度的碘水来测定某粉丝样品中二氧化硫的残留量,装置如图所示。
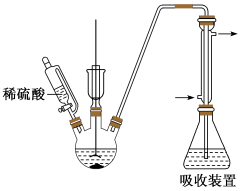
①将粉丝样品粉碎,准确称取5.0 g,放入三颈烧瓶中,加入稀硫酸浸泡30分钟,再加适量蒸馏水,加热1小时(加热装置略去),使二氧化硫完全进入吸收装置。
②往吸收装置中加入3滴淀粉溶液作指示剂,再逐滴加入0.001 mol·L-1 I2标准溶液。
当溶液颜色__________ 时,恰好完全反应,写出反应的离子方程式________ ;恰好反应时消耗I2标准溶液10.00 mL,测得样品中SO2的残留量为________ g·kg-1。
③在配制I2标准溶液,定容加水时仰视刻度线,则测得SO2含量_______ (填“偏高”“偏低”或“不变”)。
(1)实验室用如图所示装置B制取连二亚硫酸钠(Na2S2O4)。

①实验中要控制生成SO2的速率,可采取的措施有(至少写一条)
②B装置中用甲醇作溶剂,C中NaOH的作用是
(2)二氧化硫能够抑制细菌的滋生,可用作防腐剂,但必须严格按照国家标准使用。实验室用已知浓度的碘水来测定某粉丝样品中二氧化硫的残留量,装置如图所示。

①将粉丝样品粉碎,准确称取5.0 g,放入三颈烧瓶中,加入稀硫酸浸泡30分钟,再加适量蒸馏水,加热1小时(加热装置略去),使二氧化硫完全进入吸收装置。
②往吸收装置中加入3滴淀粉溶液作指示剂,再逐滴加入0.001 mol·L-1 I2标准溶液。
当溶液颜色
③在配制I2标准溶液,定容加水时仰视刻度线,则测得SO2含量
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】NaClO2的漂白能力是漂白粉的4∼5倍,NaClO2广泛用于造纸工业、污水处理等。工业上生产NaClO2的工艺流程如下:

(1)吸收器中反应的离子方程式为________ ,吸收器中的反应温度不能过高,可能的原因_______ 。
(2)反应结束后,向ClO2发生器中通入一定量空气的目的:________ 。
(3) ClO2发生器中的反应为2NaClO3+SO2+H2SO4═2ClO2+2NaHSO4,实际工业生产中可用硫磺、浓硫酸代替反应原料中的SO2,其原因是______ (用化学方程式表示)。
(4)某化学兴趣小组用如图所示装置制备SO2并探究SO2与Na2O2的反应:

①为除去过量的SO2,C中盛放的试剂为______________ 。
②D中收集到的气体可使带余烬的木条复燃,B中硬质玻璃管内发生反应的化学方程式为_______ 。
③有同学认为B中硬质玻璃管内可能还有NaSO4生成。为检验是否有 Na2SO4生成,他们设计了如下方案:

同学们经过讨论,认为上述方案不合理,其理由是:a____________ ;b_______________ 。

(1)吸收器中反应的离子方程式为
(2)反应结束后,向ClO2发生器中通入一定量空气的目的:
(3) ClO2发生器中的反应为2NaClO3+SO2+H2SO4═2ClO2+2NaHSO4,实际工业生产中可用硫磺、浓硫酸代替反应原料中的SO2,其原因是
(4)某化学兴趣小组用如图所示装置制备SO2并探究SO2与Na2O2的反应:

①为除去过量的SO2,C中盛放的试剂为
②D中收集到的气体可使带余烬的木条复燃,B中硬质玻璃管内发生反应的化学方程式为
③有同学认为B中硬质玻璃管内可能还有NaSO4生成。为检验是否有 Na2SO4生成,他们设计了如下方案:

同学们经过讨论,认为上述方案不合理,其理由是:a
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】氟是特种塑料、橡胶和冷冻剂(氟氯烷)中的关键元素。回答下列问题:
(1)基态F原子核外电子的空间运动状态有_______ 种。
(2)同周期元素N、O、F的第一电离能由大到小的顺序为_______ ,N、O、F 常见的氢化物NH3、H2O、HF的稳定性由强到弱的顺序为_______ 。
(3)氟气与水的反应复杂,主要生成HF和O2,副反应生成少量的H2O2、OF2等。OF2分子的空间构型为_______ ;HF与水能以任意比例互溶,原因是_______ 。 在一定浓度的氢氟酸溶液中,部分溶质以二分子缔合(HF)2形式存在,使HF分子缔合的作用力是_______
(4)同主族元素Cl、Br、I的单质均可与水反应生成次卤酸,则ClO-中氯原子的杂化方式为_______ 。
(5)XeF2晶体属四方晶系,晶胞结构如图所示,晶胞棱边夹角均为90.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。图中原子A的分数坐标为(0,0,0) ,原子B的分数坐标为( ,
, ,
, )。已知Xe- F键长为r pm,则原子C的分数坐标为
)。已知Xe- F键长为r pm,则原子C的分数坐标为_______ ;设NA为阿伏加德罗常数的值,XeF2的密度为_______ (列计算式)g·cm-3。

(1)基态F原子核外电子的空间运动状态有
(2)同周期元素N、O、F的第一电离能由大到小的顺序为
(3)氟气与水的反应复杂,主要生成HF和O2,副反应生成少量的H2O2、OF2等。OF2分子的空间构型为
(4)同主族元素Cl、Br、I的单质均可与水反应生成次卤酸,则ClO-中氯原子的杂化方式为
(5)XeF2晶体属四方晶系,晶胞结构如图所示,晶胞棱边夹角均为90.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。图中原子A的分数坐标为(0,0,0) ,原子B的分数坐标为(
 ,
, ,
, )。已知Xe- F键长为r pm,则原子C的分数坐标为
)。已知Xe- F键长为r pm,则原子C的分数坐标为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知X、Y、Z、R都是周期表中前四周期的元素,它们的核电荷数依次增大。X是空气中含量最高的元素,Z基态原子核外K、L、M三层电子数之比为1∶4∶2,R基态原子的3d原子轨道上的电子数是4s原子轨道上的4倍,Y基态原子的最外层电子数等于Z、R基态原子的最外层电子数之和。(答题时,X、Y、Z、R用所对应的元素符号表示)
(1)X、Y、Z的第一电离能由小到大的顺序为________ ,写出一种与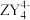 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:________ 。
(2)R3+基态核外电子排布式为________ 。
(3)化合物Z3X4熔点高达1900℃以上,硬度很大。该物质的晶体类型是________ 。
(4)Y、Z形成的某晶体的晶胞结构如图所示,则该化合物的化学式为________ 。

(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)6]2+,1mol[R(NH3)6]2+中含有σ键的数目为________ 。
(1)X、Y、Z的第一电离能由小到大的顺序为
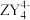 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:(2)R3+基态核外电子排布式为
(3)化合物Z3X4熔点高达1900℃以上,硬度很大。该物质的晶体类型是
(4)Y、Z形成的某晶体的晶胞结构如图所示,则该化合物的化学式为

(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)6]2+,1mol[R(NH3)6]2+中含有σ键的数目为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】W、X、Y、Z、Q是原子序数依次增大的五种短周期元素,相关描述如下:
回答下列问题。
(1)写出W、Y的元素符号:W___________ 、Y___________ 。
(2)X元素位于周期表的___________ 区,Q元素的基态原子核外电子排布式是___________ 。
(3)X、Y、Z的电负性由大到小的顺序是___________ (填元素符号)。
(4)W的简单氢化物中心原子的杂化轨道类型为___________ ,分子的空间结构为___________ ,其中的键属于___________ 键(填“σ”或“π”)。
(5)W和X的氢化物相比,键长:W-H___________ X-H(填“>”或“<”);键能:W-H___________ X-H(填“>”或“<”)。
(6)由W、X、Y组成的化合物溶于水后,滴加酚酞呈红色,用化学用语解释原因___________ 。
(7)从电子排布的角度解释元素Z的第一电离能高于同周期相邻元素的原因___________ 。
| 元素 | 元素性质或原子结构 |
| W | 其价电子中,在不同形状的原子轨道中运动的电子数相等 |
| X | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能低于同周期相邻元素 |
| Y | 在同周期元素中,原子半径最大、第一电离能最小 |
| Z | 电离能/(kJ/mol)数据: ; ;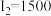 ; ; ; ;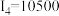 …… …… |
| Q | 最高能级有两对成对电子 |
(1)写出W、Y的元素符号:W
(2)X元素位于周期表的
(3)X、Y、Z的电负性由大到小的顺序是
(4)W的简单氢化物中心原子的杂化轨道类型为
(5)W和X的氢化物相比,键长:W-H
(6)由W、X、Y组成的化合物溶于水后,滴加酚酞呈红色,用化学用语解释原因
(7)从电子排布的角度解释元素Z的第一电离能高于同周期相邻元素的原因
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】新疆可可托海的矿物资源非常丰富,可可托海三号矿坑以“地质矿产博物馆”闻名世界,蕴藏着稀有金属铍、锂、钽、铌、铯等,有色金属铜、镍、锌、锰、铋、锡等。请用相关知识回答下列问题:
(1)基态Ni原子的价层电子的轨道表示式为_______ 。
(2)锰、锌同周期,二者的部分性质数据如下表。
请结合原子结构的知识解释Mn的第一电离能比Zn小的原因:_______ 。
(3)可可托海的Be含量居全国首位,无水BeCl2固态时具有链状结构(a),气态时存在二聚体分子(BeCl2)2(b),结构如图。
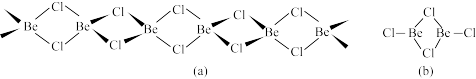
请用“→”标出(b)中的配位键_______ 。铍、铝在周期表中处于对角线位置,其单质和化合物的某些性质相似,请用化学方程式解释向BeCl2溶液中加入足量氢氧化钠溶液时先产生沉淀后沉淀溶解的原因:_______ 、_______ 。
(4)可可托海矿藏含Si量也很高,硅单质和卤素单质反应可以得到SiX4,其熔、沸点如下表:
问SiF4、SiCl4、SiB4、SiI4的熔、沸点依次升高的原因是_______ 。
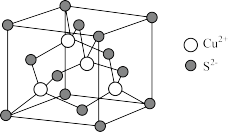
(5)纳米硫化铜具有优异的光电特性、催化能力、电导和电容特性等,在光学、电学、传感、催化等领域都具有广泛的应用前景。硫化铜的立方晶胞结构如图所示,已知S2-与Cu2+时的最近距离为anm,则该晶胞的棱长b=_______ (用含a的代数式表示)nm,NA为阿伏加德罗常数的值,则CuS的密度为_______ (用含b和NA的代数式表示)g·cm-3。
(1)基态Ni原子的价层电子的轨道表示式为
(2)锰、锌同周期,二者的部分性质数据如下表。
| 元素 | 原子半径/pm | 第一电离能/(kJ·mol-1) |
| Mn | 117 | 717.3 |
| Zn | 125 | 906.4 |
(3)可可托海的Be含量居全国首位,无水BeCl2固态时具有链状结构(a),气态时存在二聚体分子(BeCl2)2(b),结构如图。

请用“→”标出(b)中的配位键
(4)可可托海矿藏含Si量也很高,硅单质和卤素单质反应可以得到SiX4,其熔、沸点如下表:
| SiX4 | SiF4 | SiCl4 | SiBr4 | SiI4 |
| 熔点/K | 183 | 203.2 | 274.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
(5)纳米硫化铜具有优异的光电特性、催化能力、电导和电容特性等,在光学、电学、传感、催化等领域都具有广泛的应用前景。硫化铜的立方晶胞结构如图所示,已知S2-与Cu2+时的最近距离为anm,则该晶胞的棱长b=

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氟在自然界中常以CaF2的形式存在。
(1)下列关于CaF2的表述正确的是_______ 。
A.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
B.Ca2+与F-间仅存在静电吸引作用
C.CaF2、SiO2均属于离子晶体
D.CaF2中的化学键为离子键,CaF2在熔融状态下能导电
(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是_______ (用离子方程式表示)。已知[AlF6]3-在溶液中可稳定存在。
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为_______ ,其中氧原子的杂化方式为_______ 。
(4)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等,C1F3和BrF3在通常状况下分别是气体和液体。已知:Cl2(g)+3F2(g)=2C1F3(g) △H=-313kJ·mol-1,F-F键键能为159kJ·mol-1,Cl-Cl键键能为242kJ·mol-1,则ClF3中C1-F键的平均键能为_______ kJ·mol-1。ClF3的熔、沸点比BrF3的_______ (填“高”或“低”)。
(1)下列关于CaF2的表述正确的是
A.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
B.Ca2+与F-间仅存在静电吸引作用
C.CaF2、SiO2均属于离子晶体
D.CaF2中的化学键为离子键,CaF2在熔融状态下能导电
(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为
(4)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等,C1F3和BrF3在通常状况下分别是气体和液体。已知:Cl2(g)+3F2(g)=2C1F3(g) △H=-313kJ·mol-1,F-F键键能为159kJ·mol-1,Cl-Cl键键能为242kJ·mol-1,则ClF3中C1-F键的平均键能为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硼及其化合物在工业中有很多用处。一些硼的卤化物的沸点如图所示:
(1)硼原子的核外共有____ 种形状不同的电子云;溴原子的最外层电子排布式为____ 。
(2)表中三种卤化物分子的空间构型均为平面正三角形,由此推断F—B—F的键角为____ ,BF3属于____ 分子(填“极性”或“非极性”)。
(3)解释表中三种卤化硼沸点存在差异的原因____ 。
CS2是一种重要的化工原料。
(4)工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g) CS2(g)+2H2S(g),CS2的结构式为
CS2(g)+2H2S(g),CS2的结构式为____ ,利用燃煤废气(含N2、O2、SO2、CO2、H2O、NOx等)使尾气中的H2S转化为单质硫,可实现废物利用,保护环境,写出其中一个反应的化学方程式____ 。
| 卤化物 | BF3 | BCl3 | BBr3 |
| 沸点/℃ | -100.3 | 12.5 | 90 |
(2)表中三种卤化物分子的空间构型均为平面正三角形,由此推断F—B—F的键角为
(3)解释表中三种卤化硼沸点存在差异的原因
CS2是一种重要的化工原料。
(4)工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g)
 CS2(g)+2H2S(g),CS2的结构式为
CS2(g)+2H2S(g),CS2的结构式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,但使用过量会使人中毒。某学习小组针对亚硝酸钠设计了如下实验:
【制取NaNO2】
设计的制取装置如下图(夹持装置略去):
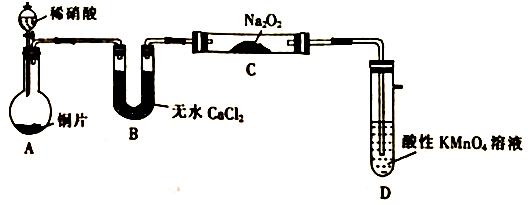
该小组查阅资料可知:①2NO+Na2O2=2NaNO2、2NO2+Na2O2=2NaNO3;
②NO能被酸性高锰酸钾氧化为NO3-。
(1)装置A中用于盛放稀硝酸的仪器名称为____________ ,装置A中发生主要反应的离子方程式为____________________________________ 。
(2)装置D的作用是____________________________________ 。
(3)若无装置B,则进入装置D中的气体除N2、NO外还可能有__________________ 。
(4)甲同学检查装置气密性后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。下列可以提高NaNO2纯度的方案是_________ (填字母)。
a.将B中的药品换为碱石灰 b.将稀硝酸换为浓硝酸
c.实验开始前通一段时间CO2 d.在装置A、B之间增加盛有水的洗气瓶
【测定制得的样品中NaNO2的含量】
(5)该实验中需配制KMnO4标准溶液并酸化,应选择_________ (填化学式)来酸化KMnO4溶液。
(6)已知:在酸性溶液中,NO2-可将MnO4-还原为Mn2+。为测定样品中亚硝酸钠的含量,该小组称取4.0g样品溶于水配制成250mL溶液,取25.00mL溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液进行滴定,消耗20.00mL酸性KMnO4溶液。滴定过程中酸性KMnO4溶液的作用是__________________ ,所得样品中NaNO2的质量分数为_________ 。
【制取NaNO2】
设计的制取装置如下图(夹持装置略去):

该小组查阅资料可知:①2NO+Na2O2=2NaNO2、2NO2+Na2O2=2NaNO3;
②NO能被酸性高锰酸钾氧化为NO3-。
(1)装置A中用于盛放稀硝酸的仪器名称为
(2)装置D的作用是
(3)若无装置B,则进入装置D中的气体除N2、NO外还可能有
(4)甲同学检查装置气密性后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。下列可以提高NaNO2纯度的方案是
a.将B中的药品换为碱石灰 b.将稀硝酸换为浓硝酸
c.实验开始前通一段时间CO2 d.在装置A、B之间增加盛有水的洗气瓶
【测定制得的样品中NaNO2的含量】
(5)该实验中需配制KMnO4标准溶液并酸化,应选择
(6)已知:在酸性溶液中,NO2-可将MnO4-还原为Mn2+。为测定样品中亚硝酸钠的含量,该小组称取4.0g样品溶于水配制成250mL溶液,取25.00mL溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液进行滴定,消耗20.00mL酸性KMnO4溶液。滴定过程中酸性KMnO4溶液的作用是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室采用高温加热三氟化硼( )与氯化铝(
)与氯化铝( )的方法制备
)的方法制备 ,装置如图所示(夹持装置及加热装置略),已知
,装置如图所示(夹持装置及加热装置略),已知 与
与 均易与水反应,
均易与水反应, 沸点低、易升华。
沸点低、易升华。
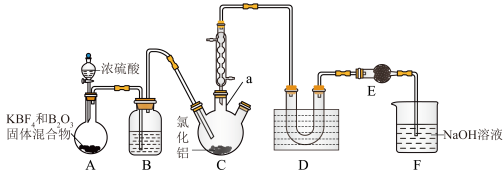
部分物质的沸点如表所示:
回答下列问题:
(1)仪器a的名称为_______ 。
(2)氟硼酸钾(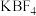 )中B元素的化合价为
)中B元素的化合价为_______ 。实验中滴入浓硫酸并加热装置A,除产生气体外,还生成一种酸式盐,写出反应的化学方程式:_______ 。
(3)装置F的作用为_______ 。
(4)实验开始时,A、C两处加热装置应先加热A处,原因是_______ 。
(5)装置D采用的是或_______ (填“水浴加热”或“冷水浴”)。
(6) 产品中氯元素含量的测定:称取
产品中氯元素含量的测定:称取 样品置于蒸馏水中完全水解,并配成
样品置于蒸馏水中完全水解,并配成 溶液,量取
溶液,量取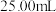 于锥形瓶中,向其中加入
于锥形瓶中,向其中加入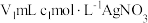 溶液使
溶液使 充分沉淀,加入一定量硝基苯用力振荡,静置后,滴加几滴
充分沉淀,加入一定量硝基苯用力振荡,静置后,滴加几滴 溶液,用
溶液,用 标准溶液滴定至溶液变为红色且半分钟内不褪色,消耗
标准溶液滴定至溶液变为红色且半分钟内不褪色,消耗 标准溶液的体积为
标准溶液的体积为 ,则产品中氯元素含量为
,则产品中氯元素含量为_______ (列出计算式即可)。(已知: )
)
 )与氯化铝(
)与氯化铝( )的方法制备
)的方法制备 ,装置如图所示(夹持装置及加热装置略),已知
,装置如图所示(夹持装置及加热装置略),已知 与
与 均易与水反应,
均易与水反应, 沸点低、易升华。
沸点低、易升华。
部分物质的沸点如表所示:
| 物质 |  |  |  |
| 沸点/℃ | 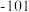 | 12.5 | 180 |
(1)仪器a的名称为
(2)氟硼酸钾(
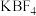 )中B元素的化合价为
)中B元素的化合价为(3)装置F的作用为
(4)实验开始时,A、C两处加热装置应先加热A处,原因是
(5)装置D采用的是或
(6)
 产品中氯元素含量的测定:称取
产品中氯元素含量的测定:称取 样品置于蒸馏水中完全水解,并配成
样品置于蒸馏水中完全水解,并配成 溶液,量取
溶液,量取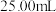 于锥形瓶中,向其中加入
于锥形瓶中,向其中加入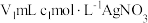 溶液使
溶液使 充分沉淀,加入一定量硝基苯用力振荡,静置后,滴加几滴
充分沉淀,加入一定量硝基苯用力振荡,静置后,滴加几滴 溶液,用
溶液,用 标准溶液滴定至溶液变为红色且半分钟内不褪色,消耗
标准溶液滴定至溶液变为红色且半分钟内不褪色,消耗 标准溶液的体积为
标准溶液的体积为 ,则产品中氯元素含量为
,则产品中氯元素含量为 )
)
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】次硫酸氢钠甲醛(aNaHSO2•bHCHO•cH2O)在印染、医药以及原子能工业中应用广泛。以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
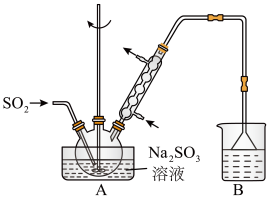
步骤1:在如图所示装置的烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH约为4,制得NaHSO3溶液。
步骤2:将装置A中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90℃下,反应约3h,冷却至室温,抽滤。
步骤3:将滤液真空蒸发浓缩,冷却结晶。
(1)装置B的烧杯中应加入的溶液是___ 。
(2)步骤2中加入锌粉时有NaHSO2和Zn(OH)2生成。
①写出加入锌粉时发生反应的化学方程式:___ 。
②生成的Zn(OH)2会覆盖在锌粉表面阻止反应进行,防止该现象发生的措施是___ 。
(3)冷凝管中回流的主要物质除H2O外,还有___ (填化学式)。
(4)步骤3中次硫酸氢钠甲醛不在敞口容器中蒸发浓缩的原因是___ 。
(5)步骤2抽滤所得滤渣的成分为Zn和Zn(OH)2,利用滤渣制备ZnO的实验步骤为:将滤渣置于烧杯中,___ ,900℃煅烧。(已知:Zn与铝类似,能与NaOH溶液反应;Zn2+开始沉淀的pH为5.9,沉淀完全的pH为8.9,pH>11时,Zn(OH)2能生成ZnO22-。实验中须使用的试剂有1.0mol•L-1NaOH溶液、1.0mol•L-1HCl溶液、水)
(6)产物组成测定实验:
准确称取1.5400g样品,溶于水配成l00mL溶液;取25.00mL样品溶液经AHMT分光光度法测得溶液吸光度A=0.4000(如图);另取25.00mL样品溶液,加入过量碘水后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到BaSO4固体0.5825g。

①样品溶液HCHO浓度为___ mol•L-1。
②通过计算确定aNaHSO2·bHCHO•cH2O的化学式为___ 。

步骤1:在如图所示装置的烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH约为4,制得NaHSO3溶液。
步骤2:将装置A中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90℃下,反应约3h,冷却至室温,抽滤。
步骤3:将滤液真空蒸发浓缩,冷却结晶。
(1)装置B的烧杯中应加入的溶液是
(2)步骤2中加入锌粉时有NaHSO2和Zn(OH)2生成。
①写出加入锌粉时发生反应的化学方程式:
②生成的Zn(OH)2会覆盖在锌粉表面阻止反应进行,防止该现象发生的措施是
(3)冷凝管中回流的主要物质除H2O外,还有
(4)步骤3中次硫酸氢钠甲醛不在敞口容器中蒸发浓缩的原因是
(5)步骤2抽滤所得滤渣的成分为Zn和Zn(OH)2,利用滤渣制备ZnO的实验步骤为:将滤渣置于烧杯中,
(6)产物组成测定实验:
准确称取1.5400g样品,溶于水配成l00mL溶液;取25.00mL样品溶液经AHMT分光光度法测得溶液吸光度A=0.4000(如图);另取25.00mL样品溶液,加入过量碘水后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到BaSO4固体0.5825g。

①样品溶液HCHO浓度为
②通过计算确定aNaHSO2·bHCHO•cH2O的化学式为
您最近半年使用:0次



