①9.8gH2SO4的物质的量为_____ mol,约含有_____ 个H2SO4分子。
②标准状况下,22.4LH2的质量为______ g。
③将30mL0.5mol/LNaCl溶液加水稀释到500mL,稀释后NaCl溶液的物质的量浓度为__________ mol/L。
④摩尔质量的符号为_______ ,单位是__________ (符号)。
②标准状况下,22.4LH2的质量为
③将30mL0.5mol/LNaCl溶液加水稀释到500mL,稀释后NaCl溶液的物质的量浓度为
④摩尔质量的符号为
更新时间:2018-09-22 22:41:07
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)NaOH的摩尔质量是__________________ 。将4gNaOH溶于水配制成100mL溶液,所得溶液中NaOH的物质的量浓度是____________________ 。取出10mL上述溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度是________________ 。
(2)根据交叉分类法,请用直线将下面的酸与酸的分类连接起来
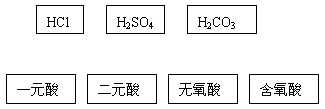
还可以补充的酸的分类标准有(只填一种):________________________________ ,从而将酸分成__________________________________________ 。
(2)根据交叉分类法,请用直线将下面的酸与酸的分类连接起来

还可以补充的酸的分类标准有(只填一种):
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】物质的量是高中化学中常用的物理量,请按要求完成下列各小题。
(1)9.03×1023个NH3含______ mol氢原子,______ mol质子,在标准状况下的体积约为_____ L。
(2)在一密闭容器中充入amolNO和bmolO2,可发生如下反应:2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比为______ 。
(3)______ molCO2分子中含有的氧原子数与1.806×1024个H2O中含有的氧原子数相同。
(4)8.4gN2与9.6g某单质Rx所含原子个数相同,且分子数之比为3∶2,则R的摩尔质量为______ ,x值为______ 。
(1)9.03×1023个NH3含
(2)在一密闭容器中充入amolNO和bmolO2,可发生如下反应:2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比为
(3)
(4)8.4gN2与9.6g某单质Rx所含原子个数相同,且分子数之比为3∶2,则R的摩尔质量为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】实验室常用加热高锰酸钾的方法制备少量氧气。
(1)请写出该反应的化学方程式___________ 。
(2)现欲制备3.36L(标准状况)氧气,理论上需要________ 克高锰酸钾?
(3)用制备的3.36L(标准状况)氧气与H2完全反应生成水,理论上需要________ 升H2的体积(标准状况)?
(1)请写出该反应的化学方程式
(2)现欲制备3.36L(标准状况)氧气,理论上需要
(3)用制备的3.36L(标准状况)氧气与H2完全反应生成水,理论上需要
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】完成下列空白(设NA为阿伏加德罗常数的值,也可使用阿伏加德罗常数的近似值):
(1)4g H 2的物质的量是_______ mol;2molH2O中H个数为_______ ;在标准状况下, 2molO2占有的体积是 _______ L。
(2)18.6 g Na2R含0.6 mol Na+,则Na2R的摩尔质量为_______ 。
(3)22gCO2中的质子数为_______ ;物质的量为0.45mol的CO2和CO的混合气体,质量为18g,则CO2和CO的分子数之比为_______ 。
(1)4g H 2的物质的量是
(2)18.6 g Na2R含0.6 mol Na+,则Na2R的摩尔质量为
(3)22gCO2中的质子数为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】现有八种物质: ①铁粉 ②NH3 ③稀盐酸 ④熔融FeCl3 ⑤CH4 ⑥CaCO3固体 ⑦CuSO4溶液 ⑧Fe3O4。
(1)①-⑥属于电解质的是_______ 。
(2)写出③与⑧反应的离子方程式_______ 。将③与⑧反应后的溶液和⑦混合,再加入过量的①,反应结束后,一定没有的阳离子为_________ 。
(3)标准状况下,4.8g⑤中所含氢原子数与______ molH2O所含氢原子数相等。
(4)标准状况下,将22.4L②溶于83mL水中形成溶液的密度为0.88g/cm3,该氨水溶质的物质的量浓度为______ mol/L ,溶质的质量分数为_______ 。
(1)①-⑥属于电解质的是
(2)写出③与⑧反应的离子方程式
(3)标准状况下,4.8g⑤中所含氢原子数与
(4)标准状况下,将22.4L②溶于83mL水中形成溶液的密度为0.88g/cm3,该氨水溶质的物质的量浓度为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】钠及其重要化合物之间的转化关系如图所示:

回答下列问题;
(1)钠元素在周期表中的位置___ ,少量的钠应保存在___ 。
(2)Na2O2的颜色为___ ,其用途为___ 。
(3)反应①中的氧化剂是___ 。
(4)反应①中4.6g的金属钠与足量的水反应生成标况下___ L氢气,转移的电子的物质的量为___ mol。

回答下列问题;
(1)钠元素在周期表中的位置
(2)Na2O2的颜色为
(3)反应①中的氧化剂是
(4)反应①中4.6g的金属钠与足量的水反应生成标况下
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】物质的量是学习化学的基础。
(1)14.4gCO和CO2的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为___ 。
(2)市售浓H2SO4的质量分数为98%、密度为1.84g/cm3,其浓度为___ mol•L-1。
(3)19g某二价金属的氯化物ACl3中含有0.4molCl-离子,金属A的相对原子质量是___ 。
(4)根据反应14CuSO4+5FeS2+12H2O 7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为
7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为__ mol。
(1)14.4gCO和CO2的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为
(2)市售浓H2SO4的质量分数为98%、密度为1.84g/cm3,其浓度为
(3)19g某二价金属的氯化物ACl3中含有0.4molCl-离子,金属A的相对原子质量是
(4)根据反应14CuSO4+5FeS2+12H2O
 7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为
7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】已知下列物质:①NH3,②稀硫酸,③氢氧化钡,④饱和FeCl3溶液,⑤稀硝酸,⑥硫酸铝。根据上述提供的物质,回答下列问题:
(1)属于非电解质的是_______ (填序号),属于电解质的是_______ (填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为_______ 。
(3)实验室制备少量Fe(OH)3胶体所用的物质是_______ (填序号),具体操作是_______ ,Fe(OH)3胶体与稀硫酸是两种不同的分散系,其本质区别是_______ 。
(4)实验室配制245 mL 0.5 mol·L-1硫酸铝溶液,从配制好的溶液中取出100 mL,其中硫酸铝的浓度是_______ mol/L,含有的SO 的数目为
的数目为_______ (设NA为阿伏加德罗常数的值),将该100 mL稀释至200 mL,硫酸铝的浓度是_______ mol/L, Al3+的浓度是_______ mol/L。
(1)属于非电解质的是
(2)上述物质间发生的某反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为
(3)实验室制备少量Fe(OH)3胶体所用的物质是
(4)实验室配制245 mL 0.5 mol·L-1硫酸铝溶液,从配制好的溶液中取出100 mL,其中硫酸铝的浓度是
 的数目为
的数目为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】将标准状况下22.4L氯化氢气体溶于水得到500mL的溶液,计算
(1)所得溶液溶质的物质的量浓度为_______ mol/L。
(2)上述溶液可与_______ mL2mol/L的氢氧化钠溶液恰好完全反应。
(1)所得溶液溶质的物质的量浓度为
(2)上述溶液可与
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】按照要求回答下列问题。
(1)已知下列七种物质:①NaCl②Cu③SO2④氯化铁溶液⑤稀硫酸⑥硫酸钡⑦熔融KNO3,其中属于电解质的是____ 。
(2)工业中常将钠块加入正己烷中,除去微量的水,反应的化学方程式为____ ;若将23g钠与一定量的水发生上述反应,最终形成1L的溶液,其溶液的物质的量浓度为____ ,同时生成的气体在标准状况下的体积为____ 。
(3)利用焰色试验的原理既可制作五彩缤纷的节日烟花,也可定性鉴别某些金属盐,立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。灼烧立德粉样品时,钡的焰色为____ 。
(4)工业废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。
+14H+=6Fe3++2Cr3++7H2O。
①在该反应中还原产物是____ (填离子符号);
②用单线桥标出该反应电子转移的方向和数目____ 。
(1)已知下列七种物质:①NaCl②Cu③SO2④氯化铁溶液⑤稀硫酸⑥硫酸钡⑦熔融KNO3,其中属于电解质的是
(2)工业中常将钠块加入正己烷中,除去微量的水,反应的化学方程式为
(3)利用焰色试验的原理既可制作五彩缤纷的节日烟花,也可定性鉴别某些金属盐,立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。灼烧立德粉样品时,钡的焰色为
| A.黄色 | B.砖红色 | C.紫色 | D.黄绿色 |
(4)工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放,工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。
+14H+=6Fe3++2Cr3++7H2O。①在该反应中还原产物是
②用单线桥标出该反应电子转移的方向和数目
您最近半年使用:0次



