钠、氯及其化合物有如下转化关系,请按要求填空:

(1)一小块金属钠投入水中(含酚酞)的反应方程式是:______________ ,现象:__________________ 。
(2)写出Na2O2生成NaOH的反应方程式:__________________________________ 。
(3)新制的氯水滴入AgNO3溶液中,观察到____________________ 现象,说明氯水中含有____________ 。
(4)工业上用氯气和石灰乳反应制漂白粉,漂白粉的有效成分是__________ ,漂白粉长时期露至在空气中会失效,写出漂白粉失效的方程式__________________ 。

(1)一小块金属钠投入水中(含酚酞)的反应方程式是:
(2)写出Na2O2生成NaOH的反应方程式:
(3)新制的氯水滴入AgNO3溶液中,观察到
(4)工业上用氯气和石灰乳反应制漂白粉,漂白粉的有效成分是
18-19高一上·陕西渭南·阶段练习 查看更多[4]
(已下线)易错专题16 氯水的成分及性质-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)(已下线)2019年11月22日 《每日一题》高一化学人教版(必修1)——Cl?的检验(已下线)2018年11月23日 《每日一题》人教必修1-Cl?的检验陕西省渭南中学2018-2019学年高一上学期教学质量检测月考(一)化学试题
更新时间:2018-09-24 18:42:09
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】运用分类的方法研究物质及变化的规律是化学学习的有效途径。
Ⅰ.物质的组成和性质都是对物质进行分类常用的依据,运用分类的方法可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。
(1)①现有下列四种物质: 、
、 、
、 、
、 ,按类别将上述四种物质填入下表:
,按类别将上述四种物质填入下表:
②为了保护环境,应减少 在大气中的排放。
在大气中的排放。 属于酸性氧化物,可与NaOH、
属于酸性氧化物,可与NaOH、___________ (填与NaOH不同类别的一种具体物质,写化学式)等反应。写出 与足量NaOH溶液反应的化学方程式
与足量NaOH溶液反应的化学方程式___________ 。
Ⅱ.现有下列物质:① 、②稀硫酸、③熔化的
、②稀硫酸、③熔化的 、④无水酒精、⑤
、④无水酒精、⑤ 、⑥
、⑥ 、⑦镁铝合金,请回答下列问题:
、⑦镁铝合金,请回答下列问题:
(2)其中属于混合物的有___________ (填序号);属于电解质的有___________ (填序号)。
(3)写出②和⑤反应的离子方程式___________ 。
(4)请写出 在①中燃烧的实验现象:
在①中燃烧的实验现象:___________ 。
Ⅰ.物质的组成和性质都是对物质进行分类常用的依据,运用分类的方法可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。
(1)①现有下列四种物质:
 、
、 、
、 、
、 ,按类别将上述四种物质填入下表:
,按类别将上述四种物质填入下表: | 类别 | 酸 | 碱 | 盐 | 酸性氧化物 |
| 物质 | a | b | c | d |
②为了保护环境,应减少
 在大气中的排放。
在大气中的排放。 属于酸性氧化物,可与NaOH、
属于酸性氧化物,可与NaOH、 与足量NaOH溶液反应的化学方程式
与足量NaOH溶液反应的化学方程式Ⅱ.现有下列物质:①
 、②稀硫酸、③熔化的
、②稀硫酸、③熔化的 、④无水酒精、⑤
、④无水酒精、⑤ 、⑥
、⑥ 、⑦镁铝合金,请回答下列问题:
、⑦镁铝合金,请回答下列问题:(2)其中属于混合物的有
(3)写出②和⑤反应的离子方程式
(4)请写出
 在①中燃烧的实验现象:
在①中燃烧的实验现象:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Cl2是一种重整的化工原料,在生产、生活和工业上均有很多用途。
(1)可与氢气化合制得盐酸。化学方程式为________________ 。
(2)可与NaOH溶液反应制得漂白液(84消毒液),离子方程式为_______________ 。
(3)可用于工业上制得高锰酸钾(KMnO4),KMnO4中Mn的化合价为_______________ 。其工业制备的部分工艺如下:
Ⅰ.将软锰矿(主要成分为MnO2)粉碎后,与KOH固体混合,通入氯气充分焙烧,生成暗绿色熔融态物质。
Ⅱ.冷却,将固体研细,用稀KOH溶液慢取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体。
Ⅳ.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料: K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液源中易发生歧化反应(Mn的化合价既升高又降低)。
①Ⅰ中,粉碎软锰矿的目的是_____________ 。
②Ⅰ中,生成K2MnO4的化学方程式是____________ 。
③Ⅱ中,浸取时用稀KOH溶液的原因是_____________ 。
④Ⅲ中,CO2和K2MnO4在溶液中反应的离子方程式是:MnO +CO2 +H2O→MnO
+CO2 +H2O→MnO +MnO2 +HCO
+MnO2 +HCO (未配平),氧化产物和还原产物的物质的量之比为
(未配平),氧化产物和还原产物的物质的量之比为____________ 。
(1)可与氢气化合制得盐酸。化学方程式为
(2)可与NaOH溶液反应制得漂白液(84消毒液),离子方程式为
(3)可用于工业上制得高锰酸钾(KMnO4),KMnO4中Mn的化合价为
Ⅰ.将软锰矿(主要成分为MnO2)粉碎后,与KOH固体混合,通入氯气充分焙烧,生成暗绿色熔融态物质。
Ⅱ.冷却,将固体研细,用稀KOH溶液慢取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体。
Ⅳ.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料: K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液源中易发生歧化反应(Mn的化合价既升高又降低)。
①Ⅰ中,粉碎软锰矿的目的是
②Ⅰ中,生成K2MnO4的化学方程式是
③Ⅱ中,浸取时用稀KOH溶液的原因是
④Ⅲ中,CO2和K2MnO4在溶液中反应的离子方程式是:MnO
 +CO2 +H2O→MnO
+CO2 +H2O→MnO +MnO2 +HCO
+MnO2 +HCO (未配平),氧化产物和还原产物的物质的量之比为
(未配平),氧化产物和还原产物的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据所学知识回答下列有关问题。
(1)下列说法正确的是________ (填序号)。
A 漂白粉久置在空气中容易失效的原因是Ca(ClO)2不稳定、易分解
B 次氯酸和过氧化钠都有漂白作用,但漂白原理不同
C Ca(ClO)2中含有氯离子
D 漂白粉与84消毒液的消毒原理相同
(2)工业上将氯气通入石灰乳[主要成分为Ca(OH)2]制取漂白粉,反应的化学方程式为___________________________________________________________ ;
湿润的Cl2也具有漂白性,但人们常将Cl2制成漂白粉使用,其主要目的是____________________________________________________________ 。
(3)漂白粉与空气中的CO2和H2O作用,即可产生具有漂白、杀菌作用的次氯酸,反应的化学方程式为______________________________________________________________ 。
(1)下列说法正确的是
A 漂白粉久置在空气中容易失效的原因是Ca(ClO)2不稳定、易分解
B 次氯酸和过氧化钠都有漂白作用,但漂白原理不同
C Ca(ClO)2中含有氯离子
D 漂白粉与84消毒液的消毒原理相同
(2)工业上将氯气通入石灰乳[主要成分为Ca(OH)2]制取漂白粉,反应的化学方程式为
湿润的Cl2也具有漂白性,但人们常将Cl2制成漂白粉使用,其主要目的是
(3)漂白粉与空气中的CO2和H2O作用,即可产生具有漂白、杀菌作用的次氯酸,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】写出下列有关反应的化学方程式
(1)氯气与水的反应________ ;
(2)制取漂粉精________ ;漂粉精放置在空气中失效的化学方程式___________ ;
(3)次氯酸见光分解________ ;
(4)实验室制氯气________ ;
(5)实验室制氯化氢气体________ 。
(1)氯气与水的反应
(2)制取漂粉精
(3)次氯酸见光分解
(4)实验室制氯气
(5)实验室制氯化氢气体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】含氧化合物具有广泛的应用,请回答下列问题。
(1) 中含有的电子数目为
中含有的电子数目为___________ 。
(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是___________ (填微粒符号,下同),Ⅱ是___________ ,Ⅲ是___________ 。
(3)氯气和氢氧化钠溶液反应可制备“84消毒液”,其化学方程式为___________ 。
(4)漂白粉漂白时,通入 可增加漂白效果,其化学方程式为
可增加漂白效果,其化学方程式为___________ 。
(5)用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,反应的现象为___________ 。
(6) 是酸性氧化物,
是酸性氧化物, 和碱反应生成
和碱反应生成 的化学方程式为
的化学方程式为___________ 。
(1)
 中含有的电子数目为
中含有的电子数目为(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是
(3)氯气和氢氧化钠溶液反应可制备“84消毒液”,其化学方程式为
(4)漂白粉漂白时,通入
 可增加漂白效果,其化学方程式为
可增加漂白效果,其化学方程式为(5)用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,反应的现象为
(6)
 是酸性氧化物,
是酸性氧化物, 和碱反应生成
和碱反应生成 的化学方程式为
的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】钠是一种非常活泼、具有广泛应用的金属。
(1)钠的原子结构示意图为 ,钠在反应中容易
,钠在反应中容易___________ 电子(填“得到”或“失去”)。
(2)金属钠非常活泼,通常保存在___________ 里,以隔绝空气。
(3)汽车安全气囊的气体发生剂 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。
ⅰ.当汽车发生较严重的碰撞时,引发 分解
分解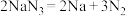 ,从而为气囊充气。产生的Na立即与
,从而为气囊充气。产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是___________ 。
ⅱ. 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为___________ 。
ⅲ.一个安全气囊通常装有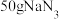 ,其完全分解所释放的
,其完全分解所释放的 为
为___________ mol。
(4)工业通过电解NaCl生产金属钠: ,过程如下:
,过程如下:

已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入 从而把熔点降至约580℃。
从而把熔点降至约580℃。
①把NaCl固体加热至熔融状态,目的是___________ 。
②电解时,要避免产生的Na与 接触而重新生成NaCl。NaCl的电离方程式为
接触而重新生成NaCl。NaCl的电离方程式为___________ 。
③粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是___________ 。
④过程Ⅰ中, 能发生像NaCl那样的电解反应而被消耗。但在过程Ⅰ中
能发生像NaCl那样的电解反应而被消耗。但在过程Ⅰ中 却不断地被重新生成,用化学方程式解释原因
却不断地被重新生成,用化学方程式解释原因___________ 。
(1)钠的原子结构示意图为
 ,钠在反应中容易
,钠在反应中容易(2)金属钠非常活泼,通常保存在
(3)汽车安全气囊的气体发生剂
 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。ⅰ.当汽车发生较严重的碰撞时,引发
 分解
分解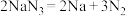 ,从而为气囊充气。产生的Na立即与
,从而为气囊充气。产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是ⅱ.
 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为ⅲ.一个安全气囊通常装有
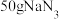 ,其完全分解所释放的
,其完全分解所释放的 为
为(4)工业通过电解NaCl生产金属钠:
 ,过程如下:
,过程如下:
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入
 从而把熔点降至约580℃。
从而把熔点降至约580℃。①把NaCl固体加热至熔融状态,目的是
②电解时,要避免产生的Na与
 接触而重新生成NaCl。NaCl的电离方程式为
接触而重新生成NaCl。NaCl的电离方程式为③粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是
④过程Ⅰ中,
 能发生像NaCl那样的电解反应而被消耗。但在过程Ⅰ中
能发生像NaCl那样的电解反应而被消耗。但在过程Ⅰ中 却不断地被重新生成,用化学方程式解释原因
却不断地被重新生成,用化学方程式解释原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知钠、氯及其化合物间有如下转化关系,
请按要求填空:
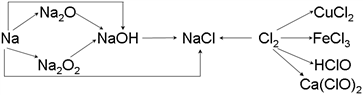
(1)实验室中金属钠通常保存在_______ 中,一小块金属钠投入水中反应的化学方程式是________________ 。
(2)Na2O2常用于呼吸面具中,有关反应的化学方程式为_____________________________ ,_________________________________ 。
(3)新制的氯水滴入紫色石蕊试液中,观察到的现象是___________________________ 。
请写出氯气与水反应的化学方程式_______________________________ 。
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为_____________________________________ 。
请按要求填空:

(1)实验室中金属钠通常保存在
(2)Na2O2常用于呼吸面具中,有关反应的化学方程式为
(3)新制的氯水滴入紫色石蕊试液中,观察到的现象是
请写出氯气与水反应的化学方程式
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】高三一年的化学复习,学生要抓住两方面,一方面是教材,另一方面是历年的高考真题。每年的高考题,在教材中几乎都能找到影子,所以同学们一定要紧紧抓住教材,根据《必修一》第三章和第四章的内容回答下列问题:
(1)实验3-1是取用钠单质的实验,用品有小刀,_____ 、_____ 、培养皿。
(2)铁是人类应用最广泛,铁的氧化物有三种,其中Fe3O4是一种具有_____ 的黑色晶体,俗称磁性氧化铁.Fe2O3的用途________ (举一例)。
(3)氢氧化铝其有两性,写出氢氧化铝分别溶于强酸和强碱的离子方程式_____ ,_______ 。
(4)在抗震救灾中要用到大量漂白粉和漂白液杀菌消毒,漂白粉的制取过程如下:通过煅烧石灰石得到生石灰,生石灰溶于水得石灰乳,在向石灰乳中通入氯气反应得漂白粉,有关的反应化学方程式为:CaCO3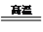 CaO+CO2↑
CaO+CO2↑_________ 、_________ 。
(1)实验3-1是取用钠单质的实验,用品有小刀,
(2)铁是人类应用最广泛,铁的氧化物有三种,其中Fe3O4是一种具有
(3)氢氧化铝其有两性,写出氢氧化铝分别溶于强酸和强碱的离子方程式
(4)在抗震救灾中要用到大量漂白粉和漂白液杀菌消毒,漂白粉的制取过程如下:通过煅烧石灰石得到生石灰,生石灰溶于水得石灰乳,在向石灰乳中通入氯气反应得漂白粉,有关的反应化学方程式为:CaCO3
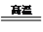 CaO+CO2↑
CaO+CO2↑
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有下列物质:①过氧化钠、②氧化铝、③硅、④二氧化硅。请根据它们的用途填空:
(1)能作光导纤维的是___________ (填序号,下同)。
(2)可用于呼吸面具中作为氧气来源的是___________ 。
(3)能作耐火材料的金属氧化物是___________ 。
(1)能作光导纤维的是
(2)可用于呼吸面具中作为氧气来源的是
(3)能作耐火材料的金属氧化物是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀,W溶液中滴加KSCN溶液出现血红色。

(1)物质A的化学式为___________ ,F化学式为___________ ;
(2)B和R在溶液中反应生成F的离子方程式为___________ ;
(3)H在潮湿空气中变成M的实验现象是___________ ;
(4)A和水反应生成B和C的化学方程式为_____ ,由此反应可知A有作为____ 的用途;

(1)物质A的化学式为
(2)B和R在溶液中反应生成F的离子方程式为
(3)H在潮湿空气中变成M的实验现象是
(4)A和水反应生成B和C的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求写出下列方程式:
(1)NaHCO3受热分解的化学方程式_______ 。
(2)少量Na2O2投入CuSO4溶液中的离子方程式_______ 。
(3)向NaHSO4溶液中加入Ba(OH)2至 刚好沉淀完全的离子方程式
刚好沉淀完全的离子方程式_______ 。
(4)MnO2溶于用H2SO4酸化的FeSO4溶液的离子方程式_______ 。
(1)NaHCO3受热分解的化学方程式
(2)少量Na2O2投入CuSO4溶液中的离子方程式
(3)向NaHSO4溶液中加入Ba(OH)2至
 刚好沉淀完全的离子方程式
刚好沉淀完全的离子方程式(4)MnO2溶于用H2SO4酸化的FeSO4溶液的离子方程式
您最近一年使用:0次



