海洋是一座巨大的化学资源宝库,从中可以提取许多常见的化学物质,结合所学知识回答下列问题,
(1)“吹出法”提溴空气吹出法是工业规模提溴的常用方法,其流程如下:

其中步骤②、④的目的是________________________________________________ 。步骤③反应的离子方程式为_______________________________ 。除SO2外,步骤③还可以选用Na2CO3溶液吸收溴,主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),吸收1molBr2时,转移电子的物质的量为____________ mol
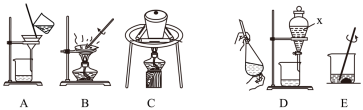
(2)实验室模拟从海带中提取碘,可能经历如下操作(或过程),请选择必要的操作(或过程),并按实验的先后顺序排列___________________________ (填写编号)
(3)卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+和Mn2+等杂质离子。现以卤块为原料按下图流程制备轻质氧化镁,若要求产品尽量不含杂质,而且生产成本较低 ,请根据表1和表2提供的资料,回答下列问题:

已知:Fe2+氢氧化物呈絮状,不易从溶液中除去。
步骤①反应的离子方程式为:_____________________________________
步骤②的反应方程式为:_________________________________________
(1)“吹出法”提溴空气吹出法是工业规模提溴的常用方法,其流程如下:

其中步骤②、④的目的是
(2)实验室模拟从海带中提取碘,可能经历如下操作(或过程),请选择必要的操作(或过程),并按实验的先后顺序排列

(3)卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+和Mn2+等杂质离子。现以卤块为原料按下图流程制备轻质氧化镁,若要求产品尽量不含杂质,而且

表1 生成氢氧化物沉淀的 pH | ||
| 物质 | 开始沉淀 | 完成沉淀 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
表2 原料价格 | |
| 物质 | 价格(元/吨) |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去。
步骤①反应的离子方程式为:
步骤②的反应方程式为:
更新时间:2018-10-09 18:57:55
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】二氧化锰常用作电池的正极材料,一种以软锰矿粉(主要成分是 ,含少量
,含少量 、
、 ,CuO、
,CuO、 等)为原料制备化学纯二氧化锰的流程如下:
等)为原料制备化学纯二氧化锰的流程如下:
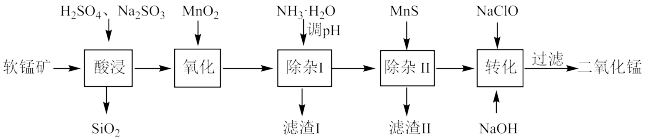
已知;
①二氧化锰不溶于水,稀酸和稀碱,可以与浓酸、浓碱缓慢反应,“酸浸”时二氧化锰转化为可溶性的硫酸锰;
②常温下,此工艺条件下各种阳离子转化为氢氧化物的pH如下:
(1)“酸浸”时将软锰矿粉碎的目的是_______ ,亚硫酸钠的作用是_______ 。
(2)“氧化”时反应的离子方程式为_______ 。
(3)“除杂Ⅰ”时,调节溶液pH的范围为_______ 。
(4)滤渣Ⅱ为_______ (填化学式)。
(5)“转化”时反应的离子方程式为_______ ,“转化”时NaOH的浓度不能太大,量不能太多的原因是_______ 。
 ,含少量
,含少量 、
、 ,CuO、
,CuO、 等)为原料制备化学纯二氧化锰的流程如下:
等)为原料制备化学纯二氧化锰的流程如下:
已知;
①二氧化锰不溶于水,稀酸和稀碱,可以与浓酸、浓碱缓慢反应,“酸浸”时二氧化锰转化为可溶性的硫酸锰;
②常温下,此工艺条件下各种阳离子转化为氢氧化物的pH如下:
 |  |  |  | 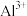 | |
| 开始沉淀 | 8.0 | 5.7 | 7.1 | 2.5 | 4.0 |
| 完全沉淀 | 9.0 | 7.5 | 10.1 | 3.2 | 4.7 |
(2)“氧化”时反应的离子方程式为
(3)“除杂Ⅰ”时,调节溶液pH的范围为
(4)滤渣Ⅱ为
(5)“转化”时反应的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】氧化亚铜(Cu2O)是一种用途广泛的光电材料,在高温下易被空气氧化成CuO。某工厂以硫化铜矿石(含 CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:
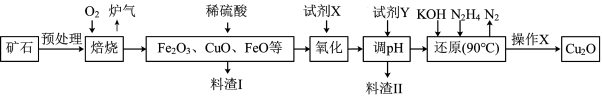
常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
(1)焙烧过程中产生的炉气是一种能造成酸雨有害气体,其化学式是___________ ,Cu2S与O2反应时,氧化剂与还原剂的物质的量之比为___________ 。
(2)若试剂X是H2O2溶液,其目的是为了将Fe2+离子变成Fe3+,写出相应反应的离子方程式___ 。当试剂X是___________ 时,更有利于降低生产成本。
(3)调pH时,加入的试剂Y可以为_______ ,pH的调控范围是________________ 。
(4)操作X包括________ 、洗涤、烘干等一系列操作,其中烘干时要隔绝空气,其目的是_____ 。

常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
| Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀 | 7.5 | 2.7 | 4.8 |
| 完全沉淀 | 9.0 | 3.7 | 6.4 |
(1)焙烧过程中产生的炉气是一种能造成酸雨有害气体,其化学式是
(2)若试剂X是H2O2溶液,其目的是为了将Fe2+离子变成Fe3+,写出相应反应的离子方程式
(3)调pH时,加入的试剂Y可以为
(4)操作X包括
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】乙酸硅是白色至米色晶体。某校同学设计实验先制备SiCl4,再由SiCl4与乙酸酐反应制备乙酸硅。已知部分物质性质如表:
回答下列问题:
(1)制备SiCl4装置(部分夹持仪器已省略)如图:
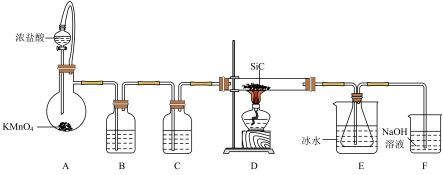
①A中制取Cl2的反应中,被氧化与未被氧化HCl的物质的量之比为_____ (写最简比),C中盛放的试剂是_____ 。
②装置D中发生的是置换反应,其化学方程式为_____ 。
③装置E用冰水浴的目的是_____ 。
④上述设计的装置有一处明显不妥,改进的方法是_____ 。
(2)制备(CH3COO)4Si的反应装置如图所示。将一定量的SiCl4放入三颈烧瓶中,在电磁搅拌下,由滴液漏斗滴入过量的乙酸酐,关闭活塞。SiCl4和(CH3CO)2O的反应为放热反应,反应后反应混合物带色,并开始析出(CH3COO)4Si晶体。
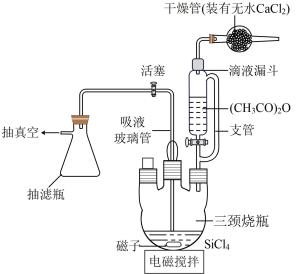
①写出生成(CH3COO)4Si的化学方程式:_____ (生成物有两种)。
②完成反应后,将反应混合液放置数日,再用干冰一丙酮浴冷却后,将导管伸入液面以下,_____ (结合装置图填写操作),获得(CH3COO)4Si晶体粗品,若得到较纯的(CH3COO)4Si,则下一步操作为_____ 。
| 物质 | 化学式 | 熔点 | 沸点 | 性质 |
| 乙酸硅 | (CH3COO)4Si | 110℃ | 148℃ | 白色至米色晶体 |
| 四氯化硅 | SiCl4 | -70℃ | 57.6℃ | 极易水解 |
| 乙酸酐 | (CH3CO)2O | -73℃ | 140℃ |
(1)制备SiCl4装置(部分夹持仪器已省略)如图:

①A中制取Cl2的反应中,被氧化与未被氧化HCl的物质的量之比为
②装置D中发生的是置换反应,其化学方程式为
③装置E用冰水浴的目的是
④上述设计的装置有一处明显不妥,改进的方法是
(2)制备(CH3COO)4Si的反应装置如图所示。将一定量的SiCl4放入三颈烧瓶中,在电磁搅拌下,由滴液漏斗滴入过量的乙酸酐,关闭活塞。SiCl4和(CH3CO)2O的反应为放热反应,反应后反应混合物带色,并开始析出(CH3COO)4Si晶体。

①写出生成(CH3COO)4Si的化学方程式:
②完成反应后,将反应混合液放置数日,再用干冰一丙酮浴冷却后,将导管伸入液面以下,
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】我国化学家侯德榜发明了联合制碱法(又称侯氏制碱法),对世界制碱工业做出了巨大贡献。侯氏制碱法的主要过程如下图所示(部分物质已略去)。

回答下列问题:
(1)①~③所涉及的操作中,属于过滤的是___________ (填序号)。
(2)将下列化学方程式补充完整___________ :NH3+CO2+___________+___________=NaHCO3↓+NH4Cl
(3)写出操作②发生反应的化学方程式___________ 。
(4)下列说法中正确的是___________ (填字母序号)。
a.NH3与CO2的通入顺序为先通入CO2,再通入NH3
b.副产物NH4Cl可用作肥料
c.CO2可循环使用

回答下列问题:
(1)①~③所涉及的操作中,属于过滤的是
(2)将下列化学方程式补充完整
(3)写出操作②发生反应的化学方程式
(4)下列说法中正确的是
a.NH3与CO2的通入顺序为先通入CO2,再通入NH3
b.副产物NH4Cl可用作肥料
c.CO2可循环使用
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】钠及其化合物的生产、应用,是化工生产与研究的重要组成部分。
Ⅰ.Na2O2用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备Na2O2并检验其纯度的实验流程如图所示。回答下列问题:

(1)生成Na2O2的化学方程式是_____ 。
(2)样液中加入MnO2后产生氧气,说明Na2O2与水反应的过程中还生成了_____ (化学式)。
(3)用该方法制备的Na2O2中含有碳酸钠。生成白色沉淀的离子方程式是_____ 。
Ⅱ.工业上以侯氏制碱法为基础生产焦亚硫酸钠(Na2S2O5,能溶于水)的工艺流程如图:
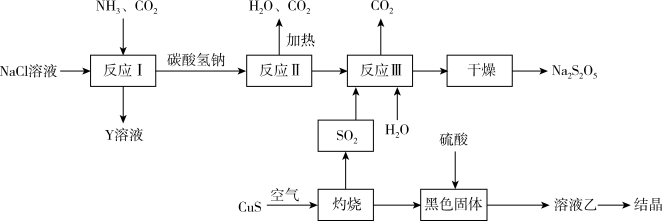
(4)反应II的化学方程式是______ 。
(5)关于上述流程,下列说法不正确的是______ (填字母)。
(6)反应III包含多步反应:
第一步:……
第二步:2NaHSO4=Na2S2O5+H2O
为了减少产品Na2S2O5中的杂质含量,理论上需控制第一步反应中气体反应物与固体反应物的物质的量之比为______ 。
(7)已知Na2S2O5与稀硫酸反应生成SO2,其离子方程式为______ 。
Ⅰ.Na2O2用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备Na2O2并检验其纯度的实验流程如图所示。回答下列问题:

(1)生成Na2O2的化学方程式是
(2)样液中加入MnO2后产生氧气,说明Na2O2与水反应的过程中还生成了
(3)用该方法制备的Na2O2中含有碳酸钠。生成白色沉淀的离子方程式是
Ⅱ.工业上以侯氏制碱法为基础生产焦亚硫酸钠(Na2S2O5,能溶于水)的工艺流程如图:

(4)反应II的化学方程式是
(5)关于上述流程,下列说法不正确的是
| A.NH3是一种碱性气体 |
| B.反应I是置换反应 |
| C.该流程中,CO2可以循环使用 |
| D.溶液乙的结晶产物是硫酸铜晶体 |
第一步:……
第二步:2NaHSO4=Na2S2O5+H2O
为了减少产品Na2S2O5中的杂质含量,理论上需控制第一步反应中气体反应物与固体反应物的物质的量之比为
(7)已知Na2S2O5与稀硫酸反应生成SO2,其离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】金属镍广泛应用于制造记忆合金、储氢合金以及用作加氢反应的催化剂,是重要的战略物资,但资源匮乏。某废镍催化剂主要含有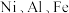 的氧化物及少量不溶性杂质,采用如下工艺流程回收其中的镍制备硫酸镍晶体
的氧化物及少量不溶性杂质,采用如下工艺流程回收其中的镍制备硫酸镍晶体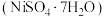 :
:

已知:① 等溶于
等溶于 溶液生成的酸根离子为
溶液生成的酸根离子为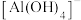 ,不是
,不是 ;
;
②溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
如下表所示:
(1) 的原子序数为
的原子序数为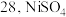 中
中 的简化电子排布式为
的简化电子排布式为_____ 。
(2)“碱浸”时发生反应的离子方程式为_____ 。
(3)滤渣③的主要成分为_____ 。
(4)利用已知②的表格数据,计算 的
的
_____ 。如果“转化”后的溶液中 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是_____ 。
(5)硫酸镍在强碱性溶液中用 氧化,可沉淀出能用作镍镉电池正极材料的
氧化,可沉淀出能用作镍镉电池正极材料的 。以
。以 溶液为介质的镍镉电池正极反应式可能为
溶液为介质的镍镉电池正极反应式可能为_____ 。
(6)将分离出硫酸镍晶体后的母液收集、并入滤液③进行循环使用,这么做的意义为_____ 。
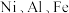 的氧化物及少量不溶性杂质,采用如下工艺流程回收其中的镍制备硫酸镍晶体
的氧化物及少量不溶性杂质,采用如下工艺流程回收其中的镍制备硫酸镍晶体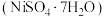 :
:
已知:①
 等溶于
等溶于 溶液生成的酸根离子为
溶液生成的酸根离子为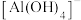 ,不是
,不是 ;
;②溶液中金属离子开始沉淀和完全沉淀的
 如下表所示:
如下表所示:| 金属离子 |  |  |  |  |
开始沉淀时 的 的 | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时 的 的 | 8.7 | 4.7 | 3.2 | 9.0 |
(1)
 的原子序数为
的原子序数为 中
中 的简化电子排布式为
的简化电子排布式为(2)“碱浸”时发生反应的离子方程式为
(3)滤渣③的主要成分为
(4)利用已知②的表格数据,计算
 的
的
 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是(5)硫酸镍在强碱性溶液中用
 氧化,可沉淀出能用作镍镉电池正极材料的
氧化,可沉淀出能用作镍镉电池正极材料的 。以
。以 溶液为介质的镍镉电池正极反应式可能为
溶液为介质的镍镉电池正极反应式可能为(6)将分离出硫酸镍晶体后的母液收集、并入滤液③进行循环使用,这么做的意义为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
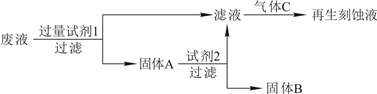
【推荐1】Ⅰ.在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(含有Fe2+、Fe3+、Cu2+)处理和资源回收很有意义。分析下面处理方案,回答下列问题:
(1)试剂2是_______ ,固体B是_______ ,通往的气体C是______ 。(填化学式)。
(2)写出加入试剂1发生反应的离子方程式:________ 、_________ 。
Ⅱ.综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:
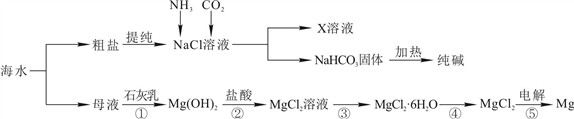
(1)反应①-⑤中,属于氧化还原反应的是_________ (填符号)。
(2)写出反应②的离子方程式____________ 。
(3)X溶液中的主要阳离子是Na+和__________ 。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③________ ;④加适量盐酸;⑤_________ (请补全缺少的实验步骤)。
(5)检验纯碱样品中是否含NaCl应选用的试剂是________ 。
(1)试剂2是
(2)写出加入试剂1发生反应的离子方程式:
Ⅱ.综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:

(1)反应①-⑤中,属于氧化还原反应的是
(2)写出反应②的离子方程式
(3)X溶液中的主要阳离子是Na+和
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③
(5)检验纯碱样品中是否含NaCl应选用的试剂是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海洋是一个远未完全开发的巨大化学资源宝库。
(1)无需经过化学变化就能从海水中获得的物质是________ (填序号)
A 氯气 B 淡水 C烧碱 D 食盐
(2)从海水制得的粗盐中含有较多的Mg2+、Ca2+、SO 等,要除去这些离子,下列加入药品顺序正确的是
等,要除去这些离子,下列加入药品顺序正确的是________ (填序号)
A NaOH溶液→Na2CO3溶液→BaCl2溶液B BaCl2溶液→NaOH溶液→Na2CO3溶液
C NaOH溶液→BaCl2溶液→Na2CO3溶液D Na2CO3溶液 →NaOH溶液→ BaCl2溶液
(3)从海水中得到溴的过程如下:
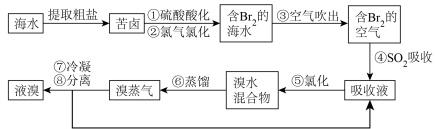
①写出由“苦卤”变成“含溴海水”的离子方程式________
②写出④发生反应的化学方程式________
③某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图所示实验装置:

图中仪器B冷却水的出口为______ (填“甲”或“乙”),D装置的作用是__________ ,反应的离子方程式为__________ ,整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________ 。
(4)已知某溶液中Cl-、Br-、I-的物质的量之比为2:3:4,现欲使溶液中的Cl-、Br-、I-的物质的量之比为变为4:3:2,那么通入Cl2的物质的量是原溶液中I-的物质的量的__________
(1)无需经过化学变化就能从海水中获得的物质是
A 氯气 B 淡水 C烧碱 D 食盐
(2)从海水制得的粗盐中含有较多的Mg2+、Ca2+、SO
 等,要除去这些离子,下列加入药品顺序正确的是
等,要除去这些离子,下列加入药品顺序正确的是A NaOH溶液→Na2CO3溶液→BaCl2溶液B BaCl2溶液→NaOH溶液→Na2CO3溶液
C NaOH溶液→BaCl2溶液→Na2CO3溶液D Na2CO3溶液 →NaOH溶液→ BaCl2溶液
(3)从海水中得到溴的过程如下:

①写出由“苦卤”变成“含溴海水”的离子方程式
②写出④发生反应的化学方程式
③某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图所示实验装置:

图中仪器B冷却水的出口为
(4)已知某溶液中Cl-、Br-、I-的物质的量之比为2:3:4,现欲使溶液中的Cl-、Br-、I-的物质的量之比为变为4:3:2,那么通入Cl2的物质的量是原溶液中I-的物质的量的
您最近半年使用:0次
【推荐3】地球的表面积为5.1亿平方公里,其中海洋的面积为3.67亿平方公里,占整个地球表面积的70.8%。海洋是一个巨大的化学资源宝库,如图是海水资源综合利用的部分流程图,请根据该图回答下列问题:
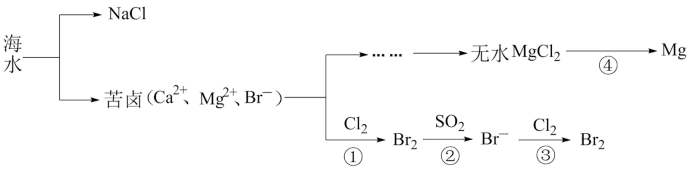
(1)淡化海水的方法有________ (写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO 等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、
等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、________ (填化学式),之后________ (填操作名称),再加入适量________ (填试剂名称)。
(2)Mg(OH)2中加入盐酸后,要获得MgCl2晶体,需要进行的实验操作依次为:________ 、________ 、过滤、洗涤、干燥。由MgCl2·6H2O脱去结晶水得到无水MgCl2,反应④由无水MgCl2制取金属镁的常用工业方法是________ 。
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,目的是________ 。写出反应②的离子方程式________ 。
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2。写出反应的化学方程式:________ 。

(1)淡化海水的方法有
 等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、
等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、(2)Mg(OH)2中加入盐酸后,要获得MgCl2晶体,需要进行的实验操作依次为:
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,目的是
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2。写出反应的化学方程式:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足的盐矿资源。盐体矿床以钾矿为主,伴生着镁、溴等多种矿产。某研究性学习小组拟取盐湖苦卤的浓缩液(富含 、
、 、
、 、
、 、
、 等)来制取较纯净的氯化钾晶体及液溴(
等)来制取较纯净的氯化钾晶体及液溴( ),他们设计了如下流程:
),他们设计了如下流程:
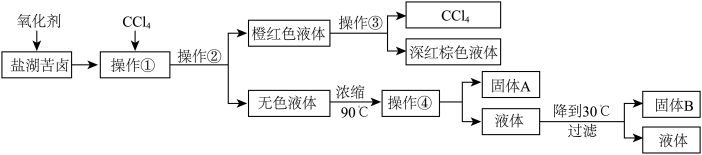
请根据以上流程,回答相关问题:
(1)操作①是_____________ ;操作②是_____________ ;操作③是_____________ ;操作④所需要的玻璃仪器有__________________________ 。
(2)参照如图所示溶解度曲线,欲得到较纯净的氯化钾晶体需用少量的____________ (填“热水”或“冷水”)洗涤固体____________ (填“A”或“B”)。
 、
、 、
、 、
、 、
、 等)来制取较纯净的氯化钾晶体及液溴(
等)来制取较纯净的氯化钾晶体及液溴( ),他们设计了如下流程:
),他们设计了如下流程:
请根据以上流程,回答相关问题:
(1)操作①是
(2)参照如图所示溶解度曲线,欲得到较纯净的氯化钾晶体需用少量的
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称。
(1)空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:

步骤①中获得Br2的离子方程式为___________ ;步骤③的化学方程式为___________ ;目的为__________ 。
(2)碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

① 设计“操作Ⅰ”的主要步骤:溶解、___________ 。
② “试剂a”通常应具有一定的___________ 性。
③ 利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:___________ 。
___________KI+___________H2O2=___________KOH+___________I2
④ 由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___________ 。(选填编号)
⑤“操作II”宜选用的装置是___________ 。(选填编号)
A. B.
B. C.
C. D.
D.
⑥在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:___________ 。
(1)空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:

步骤①中获得Br2的离子方程式为
(2)碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

① 设计“操作Ⅰ”的主要步骤:溶解、
② “试剂a”通常应具有一定的
③ 利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:
___________KI+___________H2O2=___________KOH+___________I2
④ 由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.氯仿 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶不与反应 | 与水不互溶不与I2反应 | 与水不互溶不与I2反应 | 与水不互溶与I2反应 |
A.
 B.
B. C.
C. D.
D.
⑥在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】已知海水中溴元素主要以Br-形式存在,工业上从海水中提取溴的流程如下:

(1)写出“氧化”反应的离子方程式:_______ 。
(2)将吹出后的含Br2的空气按一定速率通入吸收塔,用SO2和水进行吸收,吸收后的空气进行循环利用。
①写出吸收反应的离子方程式:_______ 。
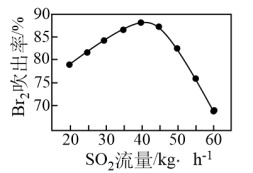
②吹出时,Br2吹出率与吸收塔中SO2流量的关系如图所示。SO2流量过大,Br2吹出率反而下降的原因是_______ 。
(3)对于较低浓度的溴水,可采用萃取的方法提取Br2。四氯化碳可作为Br2的萃取剂,其原因除四氯化碳不与溴反应外,还有_______ 。
(4)除了四氯化碳,还可以选择下列_______ 试剂
A. 苯 B.酒精 C.氢氧化钠溶液

(1)写出“氧化”反应的离子方程式:
(2)将吹出后的含Br2的空气按一定速率通入吸收塔,用SO2和水进行吸收,吸收后的空气进行循环利用。
①写出吸收反应的离子方程式:
②吹出时,Br2吹出率与吸收塔中SO2流量的关系如图所示。SO2流量过大,Br2吹出率反而下降的原因是

(3)对于较低浓度的溴水,可采用萃取的方法提取Br2。四氯化碳可作为Br2的萃取剂,其原因除四氯化碳不与溴反应外,还有
(4)除了四氯化碳,还可以选择下列
A. 苯 B.酒精 C.氢氧化钠溶液
您最近半年使用:0次



