25℃时用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH。______
2018高二·全国·专题练习 查看更多[3]
高二人教版选修4 第三章 章末基础排查(三)(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点27 水的电离和溶液的pH-备战2023年高考化学一轮复习考点帮(全国通用)
更新时间:2018-12-04 21:10:37
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m__________ n(填“大于”、“等于”或“小于”)。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】合成氨对人类生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮,其合成原理为:
 。产物氨气溶于水得到氨水
。产物氨气溶于水得到氨水
(1)氨水呈碱性,这是因为_______ (选填字母)
a.pH>7 b.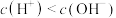
c. d.
d.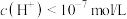
(2)常温下,测得某浓度的氨水中 的浓度为
的浓度为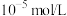 ,则该溶液的pH=
,则该溶液的pH=_______ 。

 。产物氨气溶于水得到氨水
。产物氨气溶于水得到氨水(1)氨水呈碱性,这是因为
a.pH>7 b.
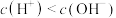
c.
 d.
d.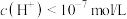
(2)常温下,测得某浓度的氨水中
 的浓度为
的浓度为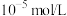 ,则该溶液的pH=
,则该溶液的pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】按要求回答问题:
(1)已知某温度下纯水的 。
。
① 的溶液呈
的溶液呈___________ (填“酸性”“中性”或“碱性”)。
②该温度下, 的盐酸的
的盐酸的
___________ 。该温度下, 的
的 溶液的
溶液的
___________ 。
③该温度下,将 的苛性钠溶液
的苛性钠溶液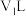 与
与 的稀硫酸
的稀硫酸 混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则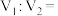
___________ 。
(2)某温度下测得纯水中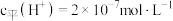 ,则此时
,则此时
___________ ;该温度下向纯水中加盐酸使 ,则此时
,则此时
___________ 。
(1)已知某温度下纯水的
 。
。①
 的溶液呈
的溶液呈②该温度下,
 的盐酸的
的盐酸的
 的
的 溶液的
溶液的
③该温度下,将
 的苛性钠溶液
的苛性钠溶液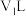 与
与 的稀硫酸
的稀硫酸 混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则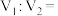
(2)某温度下测得纯水中
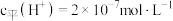 ,则此时
,则此时
 ,则此时
,则此时
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】常温下,将某一元酸HX和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,若a___ 7(填“>”“<”或“=”),则HX为强酸;若a ____ 7(填“>”“<”或“=”),则HX为弱酸。
(2)在乙组混合溶液中离子浓度c(X-)与c(Na+)的大小关系是____ 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HX是___ 酸(填“强”或“弱”)。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=__ mol/L。
实验 编号 | HX物质的量 浓度(mol/L) | NaOH物质的 量浓度(mol/L) | 混合溶液的pH |
甲 | 0.2 | 0.2 | pH=a |
乙 | c1 | 0.2 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | c2 | c2 | pH=10 |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,若a
(2)在乙组混合溶液中离子浓度c(X-)与c(Na+)的大小关系是
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HX是
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】Ⅰ.已知95 ℃时水的离子积KW=1×10-12,25 ℃时KW=1×10-14,回答下列问题:
(1)95 ℃时水的电离常数_______ (填“>”“=”或“<”) 25 ℃时水的电离常数。
(2)95 ℃纯水中c(H+)_______ (填“>”“=”或“<”)c(OH-)。
(3)95 ℃时向纯水中加入NaOH,c(OH-)=1×10-1 mol·L-1,此时pH=_______ 。
Ⅱ.(25 ℃),将20mL0.01 mol·L-1 KOH溶液与30mL0.005mol·L-1H2SO4溶液混合并加水至100ml,求混合液的pH值_______________ (写计算过程)。
(1)95 ℃时水的电离常数
(2)95 ℃纯水中c(H+)
(3)95 ℃时向纯水中加入NaOH,c(OH-)=1×10-1 mol·L-1,此时pH=
Ⅱ.(25 ℃),将20mL0.01 mol·L-1 KOH溶液与30mL0.005mol·L-1H2SO4溶液混合并加水至100ml,求混合液的pH值
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】现有①0.2 mol·L-1 NaOH溶液 ②0.2 mol·L-1 HX溶液,两溶液等体积混合后,测得溶液中c(Na+)>c(X-)。则
(1)①中由水电离出的c(OH-)________ ②中由水电离出的c(H+) (填“>”、“=”或“<”)。
(2)上述混合液中共存在______ 种粒子,且c(HX)________ c(X-)(填“>”“=”或“<”,下同),c(HX)+c(X-)________ 0.1 mol·L-1(忽略体积变化)。
(3)上述混合液显________ 性(填“酸”、“碱”或“中”),其原因用离子方程式表示为______________________________________ 。
(1)①中由水电离出的c(OH-)
(2)上述混合液中共存在
(3)上述混合液显
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】维生素C是一种水溶性维生素(其水溶液呈酸性),化学式为C6H8O6。人体缺乏维生素C可得坏血症,故维生素C又称抗坏血酸。新鲜的果蔬、乳制品富含维生素C。某校课外活动小组测定了某牌子橙汁中维生素C的含量。
测定原理: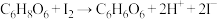
(1)实验用品及试剂:
试剂:___________ 指示剂(填名称),浓度为8.00×10-3mol·L-1的I2标准溶液、蒸馏水等。
I2标准溶液一般用棕色酸式滴定管盛装,请解释原因:___________ 。
(2)实验过程:
A.润洗后装好标准碘溶液、赶气泡、调零待用
B.用蒸馏水洗净所需仪器
C.用20mL移液管向锥形瓶中移入20.00mL待测橙汁
D.检查滴定管是否漏液
E.左手控制滴定管的活塞开关,右手摇动锥形瓶,眼睛注视锥形瓶,直到滴定终点。
F.向待测液中滴入2滴指示剂
①滴定操作的正确顺序是_____________ 。(用序号填写)
②滴定中消耗标准碘溶液体积是15.00mL,则此橙汁中维生素C的含量是_________ mg/L。

(3)问题讨论:
若摇动过程中使锥形瓶内溶液溅出,则测得的结果将会________ (填“偏大”、“偏小”或“不变”,下同);若滴定后发现滴定管尖嘴处还挂有一滴标准液,则测得的结果________ 。
(4)有同学分析实验过程,认为实验结果可能存在较大误差,除了未做防护,维生素C可能被氧化导致误差以外,也有可能是因为______________ 。
测定原理:
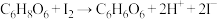
(1)实验用品及试剂:
试剂:
I2标准溶液一般用棕色酸式滴定管盛装,请解释原因:
(2)实验过程:
A.润洗后装好标准碘溶液、赶气泡、调零待用
B.用蒸馏水洗净所需仪器
C.用20mL移液管向锥形瓶中移入20.00mL待测橙汁
D.检查滴定管是否漏液
E.左手控制滴定管的活塞开关,右手摇动锥形瓶,眼睛注视锥形瓶,直到滴定终点。
F.向待测液中滴入2滴指示剂
①滴定操作的正确顺序是
②滴定中消耗标准碘溶液体积是15.00mL,则此橙汁中维生素C的含量是

(3)问题讨论:
若摇动过程中使锥形瓶内溶液溅出,则测得的结果将会
(4)有同学分析实验过程,认为实验结果可能存在较大误差,除了未做防护,维生素C可能被氧化导致误差以外,也有可能是因为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】钛白粉(TiO2)广泛应用于涂料、化妆品、食品以及医药等行业。利用黑钛矿石[主要成分为(Mg0.5Fe0.5)Ti2O5,含有少量Al2Ca(SiO4)2]制备TiO2,工艺流程如下,回答下列问题:
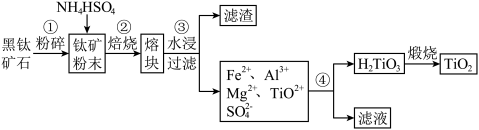
已知:TiOSO4易溶于水,在热水中易水解生成H2TiO3
常用硫酸铁铵[NH4Fe(SO4)2]滴定法测定钛白粉的纯度,其步骤为:用足量酸溶解ag二氧化钛样品,用铝粉做还原剂,过滤、洗涤,将滤液定容为100mL,取20.00mL,以NH4SCN作指示剂,用标准硫酸铁铵溶液滴定至终点,反应原理为:Ti3++Fe3+=Ti4++Fe2+
滴定终点的现象为___________ 。

已知:TiOSO4易溶于水,在热水中易水解生成H2TiO3
常用硫酸铁铵[NH4Fe(SO4)2]滴定法测定钛白粉的纯度,其步骤为:用足量酸溶解ag二氧化钛样品,用铝粉做还原剂,过滤、洗涤,将滤液定容为100mL,取20.00mL,以NH4SCN作指示剂,用标准硫酸铁铵溶液滴定至终点,反应原理为:Ti3++Fe3+=Ti4++Fe2+
滴定终点的现象为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】邻苯二甲酸(分子式为 ,常用
,常用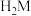 表示)是一种二元弱酸,
表示)是一种二元弱酸,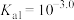 ,
,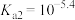 。邻苯二甲酸样品中含有少量杂质(不参与反应),某同学现用中和滴定的方法测定邻苯二甲酸样品中邻苯二甲酸的质量分数。
。邻苯二甲酸样品中含有少量杂质(不参与反应),某同学现用中和滴定的方法测定邻苯二甲酸样品中邻苯二甲酸的质量分数。
(1)用NaOH固体配制250mL 标准溶液,必须使用的仪器除天平、烧杯、玻璃棒、量筒外,还需要
标准溶液,必须使用的仪器除天平、烧杯、玻璃棒、量筒外,还需要___________ 。
(2)将NaOH标准溶液装入___________ (填“酸式”或“碱式”)滴定管中;滴定管在使用前,需要进行的操作是___________ 。
(3)盛放NaOH标准溶液的滴定管尖嘴部分留有气泡,排除气泡的方法应采用___________ (填标号)中的操作。若滴定前尖嘴部分有气泡,滴定后尖嘴部分无气泡,则测得该样品中邻苯二甲酸的质量分数将___________ (填“偏高”、“偏低”或“无影响”)。
a. b.
b. c.
c. d.
d.
(4)称取2.50g邻苯二甲酸样品,配制成100mL溶液,取10.00mL待测液于锥形瓶中,并滴入2~3滴酚酞试液作为___________ 。
(5)有关数据记录如表:
第一次滴定前、后滴定管中液面的位置如图所示,则该次滴定所消耗NaOH标准溶液的体积为___________ mL。
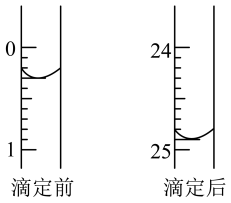
(6)到达滴定终点的现象是___________ 。
(7)根据所给数据,该邻苯二甲酸样品中邻苯二甲酸的质量分数为___________ (保留三位有效数字)。
 ,常用
,常用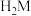 表示)是一种二元弱酸,
表示)是一种二元弱酸,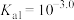 ,
,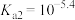 。邻苯二甲酸样品中含有少量杂质(不参与反应),某同学现用中和滴定的方法测定邻苯二甲酸样品中邻苯二甲酸的质量分数。
。邻苯二甲酸样品中含有少量杂质(不参与反应),某同学现用中和滴定的方法测定邻苯二甲酸样品中邻苯二甲酸的质量分数。(1)用NaOH固体配制250mL
 标准溶液,必须使用的仪器除天平、烧杯、玻璃棒、量筒外,还需要
标准溶液,必须使用的仪器除天平、烧杯、玻璃棒、量筒外,还需要(2)将NaOH标准溶液装入
(3)盛放NaOH标准溶液的滴定管尖嘴部分留有气泡,排除气泡的方法应采用
a.
 b.
b. c.
c. d.
d.
(4)称取2.50g邻苯二甲酸样品,配制成100mL溶液,取10.00mL待测液于锥形瓶中,并滴入2~3滴酚酞试液作为
(5)有关数据记录如表:
| 滴定序号 | 待测样品溶液体积/mL | NaOH标准溶液 | ||
| 滴定前的刻度/mL | 滴定后的刻度/mL | 消耗的体积/mL | ||
| 1 | 10.00 | |||
| 2 | 10.00 | 0.10 | 24.74 | 24.64 |
| 3 | 10.00 | 1.23 | 25.85 | 24.62 |

(6)到达滴定终点的现象是
(7)根据所给数据,该邻苯二甲酸样品中邻苯二甲酸的质量分数为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】室温下,某一元弱酸HA的电离常数K=1.6×10-6。向20.00mL浓度约为0.1mol·L-1HA溶液中逐滴加入0.1000mol·L-1的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:
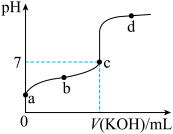
(1)a、b、c、d四点中水的电离程度最大的是_______ 点,滴定过程中宜选用__________ 作指示剂,滴定终点在__________ (填“c点以上”或“c点以下”)。
(2)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_____ (填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(3)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____ mol/L。(保留4位有效数字)
(4)a点溶液中pH约为________ ,此时溶液中H2O电离出的c(H+)为________ 。

(1)a、b、c、d四点中水的电离程度最大的是
(2)滴定过程中部分操作如下,下列各操作使测量结果偏高的是
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(3)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为
| 实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
| 1 | 21.01 | 20.00 |
| 2 | 20.99 | 20.00 |
| 3 | 21.60 | 20.00 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】25℃时有以下5种溶液:①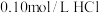 溶液;②
溶液;②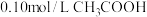 溶液;③
溶液;③ 溶液;④
溶液;④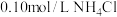 溶液;⑤
溶液;⑤ 溶液。
溶液。
(1)泡沫灭火器中的原料之一是上述5种溶液中的一种,此灭火器灭火的原理为_______ (用离子方程式表示)。
(2)往②加入少量 固体,此溶液的pH
固体,此溶液的pH_______ (填“增大”“减小”或“不变”)。
(3)①和②两种溶液中水的电离程度大小为①_______ ②(填“>”“<”或者“=”)。
(4)将②与③等体积混合后,溶液中存在的离子浓度由大到小的顺序是_______ (用离子符号表示)。
(5)用pH试纸测得④的 ,则此溶液中水电离出来的氢氧根离子浓度为
,则此溶液中水电离出来的氢氧根离子浓度为_______  。
。
(6)用 的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
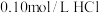 溶液;②
溶液;②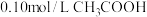 溶液;③
溶液;③ 溶液;④
溶液;④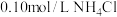 溶液;⑤
溶液;⑤ 溶液。
溶液。(1)泡沫灭火器中的原料之一是上述5种溶液中的一种,此灭火器灭火的原理为
(2)往②加入少量
 固体,此溶液的pH
固体,此溶液的pH(3)①和②两种溶液中水的电离程度大小为①
(4)将②与③等体积混合后,溶液中存在的离子浓度由大到小的顺序是
(5)用pH试纸测得④的
 ,则此溶液中水电离出来的氢氧根离子浓度为
,则此溶液中水电离出来的氢氧根离子浓度为 。
。(6)用
 的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。| A.用蒸馏水洗净酸式滴定管、锥形瓶后可分别直接注入标准盐酸和待测液NaOH溶液 |
| B.滴定时左手旋转滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视滴定管液面变化 |
| C.此中和滴定实验的指示剂可采用酚酞,滴定终点的现象为:溶液由无色变为红色,且30s内颜色不变 |
| D.若滴定前仰视读数、滴定后俯视读数,则所测NaOH溶液的浓度偏低 |
您最近一年使用:0次



