25℃时,已知弱酸的电离常数:K(CH3COOH)=1.8×10-5;K1(H2C03)=4.4×10-7, K2(H2C03)=5.6×10-11;K(HCl0)=3.0×10-8。下列说法中正确的是
| A.25℃时,0.1mol·L-1的醋酸溶液比0.Olmol·L-1 的醋酸溶液的K值小 |
| B.25℃时,CH3COOH溶液中加入少量NaHC03固体,醋酸的电离程度增大 |
| C.新制氯水与NaHC03溶液不发生反应 |
| D.NaCl0溶液中通入少量CO2发生反应的离子方程式:2NaCl0+CO2+H2O=Na2CO3+2HCl0 |
更新时间:2018-12-07 10:17:35
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】有①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25mL,物质的量浓度均为0.1mol·L-1,下列说法正确的是
| A.3种溶液pH的大小顺序是③>②>① |
| B.若将3种溶液稀释相同倍数,pH变化最大的是② |
| C.若分别加入25mL 0.1mol·L-1盐酸后,pH最大的是① |
| D.三种溶液中,水的电离程度最大的是③ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】100mL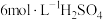 跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量:①
跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量:① ②
②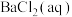 ③
③ ④
④ 固体⑤
固体⑤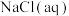 ,其中组合正确的是
,其中组合正确的是
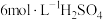 跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量:①
跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量:① ②
②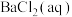 ③
③ ④
④ 固体⑤
固体⑤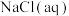 ,其中组合正确的是
,其中组合正确的是| A.①②③ | B.②④⑤ | C.③④⑤ | D.①③④ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】在相同温度时,100mL HF溶液与10mL
HF溶液与10mL HF溶液相比较,下列数值中,前者大于后者的是
HF溶液相比较,下列数值中,前者大于后者的是
 HF溶液与10mL
HF溶液与10mL HF溶液相比较,下列数值中,前者大于后者的是
HF溶液相比较,下列数值中,前者大于后者的是| A.HF的电离常数 | B.溶液中H+的物质的量 |
| C.中和时所需NaOH的物质的量 | D.溶液中HF的物质的量 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如下图所示。下列说法正确的是
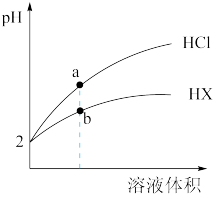

| A.稀释前,c(HX)=0.01mol/L | B.稀释10倍,HX溶液的pH=3 |
| C.a、b两点:c(X-)>c(Cl-) | D.溶液的导电性:a>b |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列图示与对应的叙述相符的是


| A.图1表示向氨水中通入HCl气体,溶液的导电能力变化 |
| B.图2表示不同温度下水溶液中H+和OH-浓度变化的曲线,图中温度T2>T1 |
| C.图3可表示pH相同的NaOH溶液与氨水稀释过程的pH变化,其中曲线a对应氨水 |
D.图4表示同一温度下,在不同容积的容器中进行反应2BaO2(s) 2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系 2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】部分弱电解质的电离平衡常数如下表,下列说法不正确的是
| 弱电解质 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25 ℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
A.结合质子的能力:CO >CN->HCO >CN->HCO >HCOO- >HCOO- |
B.可发生2CN-+ H2O +CO2 = 2HCN + CO |
C.等浓度NaCN和NaHCO3溶液中:c(Na+)>c(HCO )>c(CN-)>c(OH-)>c(H+) )>c(CN-)>c(OH-)>c(H+) |
| D.相同浓度HCOOH和HCN溶液,HCOOH的pH更小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】25 ℃,c(HCN)+c(CN-)=0.1 mol·L-1的一组HCN和NaCN的混合溶液,溶液中 c(HCN)、c(CN-)与pH的关系如图所示。下列有关离子浓度关系叙述正确的是


| A.将 0.1 mol·L-1的 HCN 溶液和 0.1 mol·L-1NaCN溶液等体积混合(忽略溶液体积变化):c(Na+)>c(HCN)>c(CN-)>c(OH-)>c(H+) |
| B.W 点表示溶液中:c(Na+)=c(HCN)+c(CN-) |
| C.pH=8的溶液中:c(Na+)+c(H+)+c(HCN)=0.1 mol·L-1+c(OH-) |
| D.将0.3 mol·L-1 HCN溶液和0.2 mol·L-1NaOH溶液等体积混合(忽略溶液体积变化):c(CN-)+3c(OH-)=c(HCN)+3c(H+) |
您最近半年使用:0次

 及其与
及其与 形成的微粒的物质的量分数随溶液
形成的微粒的物质的量分数随溶液 变化的关系如图所示。已知
变化的关系如图所示。已知 的
的 。向
。向 溶液中滴加氨水关于该过程的说法正确的是
溶液中滴加氨水关于该过程的说法正确的是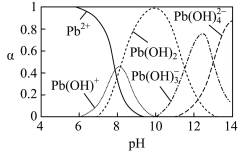

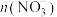 与
与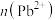 的比值先减小后增大
的比值先减小后增大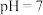 时,存在的阳离子有
时,存在的阳离子有 、
、 和
和
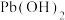 浓度相等时,氨主要以
浓度相等时,氨主要以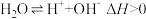 。下列叙述正确的是
。下列叙述正确的是 降低
降低 增大,
增大,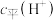 不变
不变 ,
,

