现有浓度均为0.01mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水。请回答下列问题:
(1)①、②、③、④四种溶液中,水电离出的c(H+)由大到小的顺序是_________ (填序号)。
(2)④、⑤、⑥、⑦四种溶液中,c(NH4+)由大到小的顺序是_______ (填序号)。
(3)将③和④按体积比1:2混合后,混合液中各离子浓度由大到小的顺序是_______ 。
(4)已知T℃时,③溶液的pH=11,该温度下,水的离子积Kw=______________ ;该温度下,将pH之和为13的NaOH溶液和醋酸溶液等体积混合后,所得溶液呈____ (填“酸”“碱”或“中”)性。T℃时,将aL pH=11的NaOH溶液与bL pH=1的H2SO4溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a:b=________ 。
(1)①、②、③、④四种溶液中,水电离出的c(H+)由大到小的顺序是
(2)④、⑤、⑥、⑦四种溶液中,c(NH4+)由大到小的顺序是
(3)将③和④按体积比1:2混合后,混合液中各离子浓度由大到小的顺序是
(4)已知T℃时,③溶液的pH=11,该温度下,水的离子积Kw=
更新时间:2018-12-30 14:53:20
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】按要求回答下列问题:
(1)设Ag=lg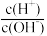 ,常温下,pH=12的Ba(OH)2与0.01mol/LNaHSO4等体积混合,则溶液中的AG=
,常温下,pH=12的Ba(OH)2与0.01mol/LNaHSO4等体积混合,则溶液中的AG=____ 。
(2)已知25℃时,Na2CO3的Kh1=2×10-4mol•L-1,则当Na2CO3溶液中c(HCO ):c(CO
):c(CO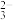 )=2:1时,求溶液的pH=
)=2:1时,求溶液的pH=____ 。
(3)常温下,pH=2的某酸(HxA)溶液与pH=12的某碱[B(OH)y]溶液等体积混合,充分反应后溶液的pH为10,若该盐中只存在一种能水解的离子,则水解的离子方程式为____ ,混合溶液中水电离出的c(H+)=____ 。
(4)某温度下,测得0.01mol/LNaOH溶液的pH=11,则将此温度下pH=12的NaOH溶液VxL与pH=2的H2SO4溶液VyL混合,所得溶液pH=10,则Vx:Vy=____ 。
(5)室温时,CH3COOH的Ka=1.8×10-5,将amol/L醋酸与bmol/LBa(OH)2溶液以2:1体积比混合(忽略溶液体积变化),若混合溶液中2c(Ba2+)=c(CH3COO-),则溶液呈____ 性,混合后溶液中CH3COOH的浓度为_____ mol/L。(用含相关字母的最简代数式表示)
(6)常温下,用300mL浓度为1mol/L的Na2SO3溶液吸收SO2的过程中,溶液pH随吸收SO2物质的量的变化曲线如图所示:
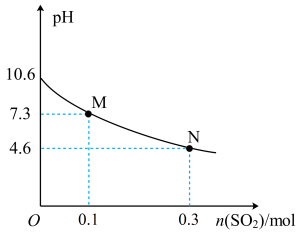
常温下,H2SO3的二级电离平衡常数Ka2约为_____ 。
(1)设Ag=lg
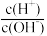 ,常温下,pH=12的Ba(OH)2与0.01mol/LNaHSO4等体积混合,则溶液中的AG=
,常温下,pH=12的Ba(OH)2与0.01mol/LNaHSO4等体积混合,则溶液中的AG=(2)已知25℃时,Na2CO3的Kh1=2×10-4mol•L-1,则当Na2CO3溶液中c(HCO
 ):c(CO
):c(CO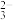 )=2:1时,求溶液的pH=
)=2:1时,求溶液的pH=(3)常温下,pH=2的某酸(HxA)溶液与pH=12的某碱[B(OH)y]溶液等体积混合,充分反应后溶液的pH为10,若该盐中只存在一种能水解的离子,则水解的离子方程式为
(4)某温度下,测得0.01mol/LNaOH溶液的pH=11,则将此温度下pH=12的NaOH溶液VxL与pH=2的H2SO4溶液VyL混合,所得溶液pH=10,则Vx:Vy=
(5)室温时,CH3COOH的Ka=1.8×10-5,将amol/L醋酸与bmol/LBa(OH)2溶液以2:1体积比混合(忽略溶液体积变化),若混合溶液中2c(Ba2+)=c(CH3COO-),则溶液呈
(6)常温下,用300mL浓度为1mol/L的Na2SO3溶液吸收SO2的过程中,溶液pH随吸收SO2物质的量的变化曲线如图所示:

常温下,H2SO3的二级电离平衡常数Ka2约为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】25℃时,有浓度均为0.1mol•L-1的下列4种溶液:
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④Na2CO3溶液
(1)H3PO2是一元中强酸,具有较强的还原性。写出其电离方程式______ 。
(2)上述4种溶液pH最小的是______ (填序号),其中②由水电离的H+浓度为_____ mol•L-1。
(3)①中各离子浓度由大到小的顺序是______ 。
(4)现有浓度为0.02mol/L的HCN与0.01moL/LNaOH等体积混合后(忽略体积变化),测得c(Na+)>c(CN-),下列关系正确的是______ 。(填标号)
(5)25℃时,测得HCN和NaCN的混合溶液的pH=11,则 约为
约为_____ (计算结果保留两位小数)。向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:_____ 。
(6)已知t℃时,Kw=1×10-13,则t℃_____ 25℃(填“>”、“<”或“=”)。在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 =
=_____ 。
(7)25℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH值pH1与强碱的pH值pH2之间应满足的关系是_____ 。
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④Na2CO3溶液
| HCN | H2CO3 | CH3COOH |
| Ka=4.9×10-10 | Ka1=4.4×10-7 Ka2=4.7×10-11 | Ka=1.75×10-5 |
(2)上述4种溶液pH最小的是
(3)①中各离子浓度由大到小的顺序是
(4)现有浓度为0.02mol/L的HCN与0.01moL/LNaOH等体积混合后(忽略体积变化),测得c(Na+)>c(CN-),下列关系正确的是
| A.c(H+)>c(OH-) | B.c(H+)<c(OH-) |
| C.c(H+)+c(HCN)=c(OH-) | D.c(HCN)+c(CN-)=0.01mol/L |
 约为
约为(6)已知t℃时,Kw=1×10-13,则t℃
 =
=(7)25℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH值pH1与强碱的pH值pH2之间应满足的关系是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】已知在室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,回答下列问题:
(1)两溶液中c(H+) • c(OH-)=___________
(2)两溶液中由水电离出的c(H+)分别为:H2SO4溶液________ ;NH4Cl溶液__________
(3)各取5mL上述溶液,分别加水稀释至50mL,pH较大的是________ 溶液
(4)各取5mL上述溶液,分别加热到90℃,pH较小的是________ 溶液
(5)取5mL NH4Cl溶液,加水稀释至50mL,c(H+)__________ 10-6mol·L-1(填“>”、“<”或“=”),c(NH4+)/c(H+)________ (填“增大”、“减小”或“不变”)
(1)两溶液中c(H+) • c(OH-)=
(2)两溶液中由水电离出的c(H+)分别为:H2SO4溶液
(3)各取5mL上述溶液,分别加水稀释至50mL,pH较大的是
(4)各取5mL上述溶液,分别加热到90℃,pH较小的是
(5)取5mL NH4Cl溶液,加水稀释至50mL,c(H+)
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】盐在化学工业中有重要的应用,请回答下列问题
(1)用离子方程式表示FeCl3可作净水剂的原因:___________________ 。
(2)常温下,在pH=3的硫酸与pH=11的Na2S溶液中,水电离出来的c(OH-)之比为_____ , 向Na2S溶液中加入AlCl3溶液时,产生白色沉淀和有臭鸡蛋味的气体,其离子方程式为:_________________ 。
(3)c(NH4+)相等的下列溶液① NH4Cl ②NH4HSO4 ③(NH4)2SO4 ④CH3COONH4
⑤NH3 H2O,溶液的物质的量浓度由小到大的顺序是__________ (用序号表示)
(4)已知t ℃时AgCl的Ksp=2×10-10 ;(2)在t ℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列正确的是_______
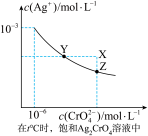
A.在t ℃时,Ag2CrO4的Ksp为1×10-9
B.t ℃时,在饱和Ag2CrO4溶液中加入K2CrO4 可使溶液由Y点到X点
C.在t ℃时,以0.01mol/L AgNO3溶液滴定20mL0.01 mol/L KCl和0.01 mol/L的K2CrO4的混合溶液,Cl-先沉淀
D.在t ℃时,AgCl的溶解度大于Ag2CrO4
(5)已知某温度时:Ksp[Fe(OH)3]=1×10-38,Ksp[Cu(OH)2]=1×10-20。在该温度下向Fe3+、Cu2+均为0.01mol•L-1的溶液中逐滴加入NaOH溶液,要Fe3+完全沉淀,而Cu2+不产生沉淀,溶液中PH应控制的范围是_______ 。(当离子浓度小于1×10-5mol/L时,认为完全沉淀)。
(1)用离子方程式表示FeCl3可作净水剂的原因:
(2)常温下,在pH=3的硫酸与pH=11的Na2S溶液中,水电离出来的c(OH-)之比为
(3)c(NH4+)相等的下列溶液① NH4Cl ②NH4HSO4 ③(NH4)2SO4 ④CH3COONH4
⑤NH3 H2O,溶液的物质的量浓度由小到大的顺序是
(4)已知t ℃时AgCl的Ksp=2×10-10 ;(2)在t ℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列正确的是

A.在t ℃时,Ag2CrO4的Ksp为1×10-9
B.t ℃时,在饱和Ag2CrO4溶液中加入K2CrO4 可使溶液由Y点到X点
C.在t ℃时,以0.01mol/L AgNO3溶液滴定20mL0.01 mol/L KCl和0.01 mol/L的K2CrO4的混合溶液,Cl-先沉淀
D.在t ℃时,AgCl的溶解度大于Ag2CrO4
(5)已知某温度时:Ksp[Fe(OH)3]=1×10-38,Ksp[Cu(OH)2]=1×10-20。在该温度下向Fe3+、Cu2+均为0.01mol•L-1的溶液中逐滴加入NaOH溶液,要Fe3+完全沉淀,而Cu2+不产生沉淀,溶液中PH应控制的范围是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】25℃时,物质的量浓度均为0.1mol•L﹣1的几种盐溶液的pH如表:
(1)①中由水电离出的c(OH-)________ (填“>”“=”或“<”)②中由水电离出的c(H+)。
(2)③中共存在______ 种粒子,pH=8.4的原因:_______________________________ ;
(3)下列说法正确的是_____ 。
A.c(NH4+):①>②
B.物质的量浓度和体积均相等的NaCl和CH3COONH4两种溶液中,离子总数相等
C.等体积的③和⑤形成的混合溶液中:c(HCO3﹣)+c(CO32﹣)=0.1mol•L﹣1
D.将pH相同的CH3COOH和HX溶液加水稀释相同倍数,HX溶液的pH变化小
(4)常温下在20 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
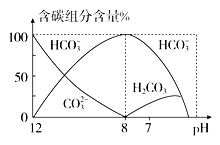
回答下列问题:
①当pH=7时,溶液中含碳元素的主要微粒为________
②已知在25 ℃时,CO 水解反应的平衡常数Kh=
水解反应的平衡常数Kh=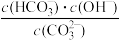 =2.0×10-4 mol·L-1,当溶液中c(HCO
=2.0×10-4 mol·L-1,当溶液中c(HCO )∶c(CO
)∶c(CO )=2∶1时,溶液的pH=
)=2∶1时,溶液的pH=______________ 。
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 溶液 | NH4Cl | CH3COONH4 | NaHCO3 | NaX | Na2CO3 |
| pH | 5 | 7 | 8.4 | 9.7 | 11.6 |
(2)③中共存在
(3)下列说法正确的是
A.c(NH4+):①>②
B.物质的量浓度和体积均相等的NaCl和CH3COONH4两种溶液中,离子总数相等
C.等体积的③和⑤形成的混合溶液中:c(HCO3﹣)+c(CO32﹣)=0.1mol•L﹣1
D.将pH相同的CH3COOH和HX溶液加水稀释相同倍数,HX溶液的pH变化小
(4)常温下在20 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。

回答下列问题:
①当pH=7时,溶液中含碳元素的主要微粒为
②已知在25 ℃时,CO
 水解反应的平衡常数Kh=
水解反应的平衡常数Kh=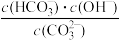 =2.0×10-4 mol·L-1,当溶液中c(HCO
=2.0×10-4 mol·L-1,当溶液中c(HCO )∶c(CO
)∶c(CO )=2∶1时,溶液的pH=
)=2∶1时,溶液的pH=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】按要求填写下列相关内容:
(1)实验表明,液氨也能像水那样进行自耦电离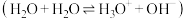 ,碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
,碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
①写出液氨自耦电离的方程式_______ 。
②写出碳酸钠溶于液氨后第一级氨解的离子方程式:_______ 。
(2)室温下 的盐酸和
的盐酸和 的碳酸钠溶液,水电离出的
的碳酸钠溶液,水电离出的 的比值为
的比值为_______ ,将二者等体积混合,溶液显_______ 性。
(3)某温度时, 的
的 溶液的
溶液的 是12,在此温度下,将
是12,在此温度下,将 的盐酸溶液
的盐酸溶液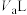 与
与 的
的 溶液
溶液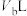 混合,所得混合液为中性,若
混合,所得混合液为中性,若 ,则
,则
_______ 。
(4)若 水解的离子方程式为
水解的离子方程式为 ,室温下该水解反应的平衡常数
,室温下该水解反应的平衡常数
_______ 。(已知室温下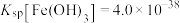 )
)
(5) 在水溶液中的电离如下:
在水溶液中的电离如下: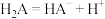 ,
, ,
,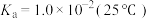
①向 溶液中滴加少量氨水,该反应的离子方程式为
溶液中滴加少量氨水,该反应的离子方程式为_______ 。
②已知 电离平衡常数
电离平衡常数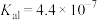 ,
, ,则
,则 和
和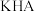 两溶液混合反应的离子方程式为
两溶液混合反应的离子方程式为_______ 。
(1)实验表明,液氨也能像水那样进行自耦电离
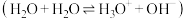 ,碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
,碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。①写出液氨自耦电离的方程式
②写出碳酸钠溶于液氨后第一级氨解的离子方程式:
(2)室温下
 的盐酸和
的盐酸和 的碳酸钠溶液,水电离出的
的碳酸钠溶液,水电离出的 的比值为
的比值为(3)某温度时,
 的
的 溶液的
溶液的 是12,在此温度下,将
是12,在此温度下,将 的盐酸溶液
的盐酸溶液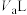 与
与 的
的 溶液
溶液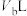 混合,所得混合液为中性,若
混合,所得混合液为中性,若 ,则
,则
(4)若
 水解的离子方程式为
水解的离子方程式为 ,室温下该水解反应的平衡常数
,室温下该水解反应的平衡常数
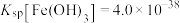 )
)(5)
 在水溶液中的电离如下:
在水溶液中的电离如下: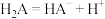 ,
, ,
,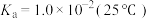
①向
 溶液中滴加少量氨水,该反应的离子方程式为
溶液中滴加少量氨水,该反应的离子方程式为②已知
 电离平衡常数
电离平衡常数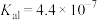 ,
, ,则
,则 和
和 两溶液混合反应的离子方程式为
两溶液混合反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】25℃时,有关物质的电离平衡常数如下:
(1)以上三种电解质由强至弱顺序为________________________ (用化学式表示,下同)。
(2)常温下,0.02 mol·L-1的CH3COOH溶液的电离度约为_____________ ,体积为10mLpH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者_____ 后者(填“>、<或=”)。
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为___________________________________________________ 。
(4)已知NaHSO3溶液显酸性,其原因是____________________ (离子方程式配适当文字叙述)。
(5)H2SO3溶液和NaHCO3溶液反应的主要离子方程式为_______________________ 。
| 化学式 | CH3COOH | H2CO3 | H2SO3 |
| 电离平衡常数K | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)以上三种电解质由强至弱顺序为
(2)常温下,0.02 mol·L-1的CH3COOH溶液的电离度约为
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为
(4)已知NaHSO3溶液显酸性,其原因是
(5)H2SO3溶液和NaHCO3溶液反应的主要离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如表所示:所给几种钠盐的阴离子,结合氢离子能力最弱的是_______ (填离子符号),根据表中数据判断,将浓度均为0.01 mol·L-1的下列四种酸的溶液分别稀释100倍,pH变化最小的是_______ (填序号)。
A. HCN B. HClO C. CH3COOH D. H2CO3
(2) 浓度均为0.1 mol·L-1的Na2CO3和NaHCO3的混合液,所得溶液中各离子的浓度由大到小的顺序为:_______
(3)已知,常温下几种离子开始沉淀时溶液的pH如表所示:
当向含有相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,_______ 后沉淀(填离子符号);Ksp[Fe(OH)2]_______ Ksp[Mg(OH)2] (填“>”“=”或“<”)
常温下,要使0.2 mol·L-1的硫酸铜溶液中铜离子沉淀较为完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液使溶液pH=_______ 。(Ksp[Cu(OH)2]=2×10-20)
(1)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如表所示:所给几种钠盐的阴离子,结合氢离子能力最弱的是
A. HCN B. HClO C. CH3COOH D. H2CO3
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
(2) 浓度均为0.1 mol·L-1的Na2CO3和NaHCO3的混合液,所得溶液中各离子的浓度由大到小的顺序为:
(3)已知,常温下几种离子开始沉淀时溶液的pH如表所示:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
当向含有相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,
常温下,要使0.2 mol·L-1的硫酸铜溶液中铜离子沉淀较为完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液使溶液pH=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱电解质的电离平衡常数:
请回答下面问题:
(1)上述四种酸中,酸性最弱的是_____________ (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是________________ (填序号)。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈________ (选填“酸性”“中性”或“碱性”),理由是__________________ ,溶液中各离子浓度大小的关系是_____________________ 。
(3)物质的量1∶1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子的浓度从大到小排列为_____________________________________ 。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度达到0.0lmol·L-1以上,则溶液中CO32-物质的量浓度应 ≥____________ mol·L-1。
| 酸或碱 | 电离常数(Ka或Kb) | 难(微)溶物 | 溶度积常数(Ksp) |
| CH3COOH | 1.8×10-5 | BaSO4 | 1×10-10 |
| HNO2 | 4.6×10-4 | BaCO3 | 2.6×10-9 |
| HCN | 5×10-10 | CaSO4 | 7×10-5 |
| HClO | 3×10-8 | CaCO3 | 5×10-9 |
| NH3·H2O | 1.8×10-5 |
请回答下面问题:
(1)上述四种酸中,酸性最弱的是
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈
(3)物质的量1∶1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子的浓度从大到小排列为
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度达到0.0lmol·L-1以上,则溶液中CO32-物质的量浓度应 ≥
您最近一年使用:0次



