二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知:①Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O;
②2SO2+SeO2+2H2O===Se+2SO42—+4H+。
(1) Se与浓H2SO4的反应中,氧化剂是________________ ,还原剂是_______________ 。当有标准状况下22.4 L SO2气体生成时,转移电子的物质的量是________ mol。
(2)依据反应①、②判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是______________________ 。
(3)用单线桥法标出反应②电子转移的方向和数目:_____________________________ 。
(4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3―→Se+I2+KNO3+H2O配平上述反应的化学方程式______________________________________________ 。
已知:①Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O;
②2SO2+SeO2+2H2O===Se+2SO42—+4H+。
(1) Se与浓H2SO4的反应中,氧化剂是
(2)依据反应①、②判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是
(3)用单线桥法标出反应②电子转移的方向和数目:
(4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3―→Se+I2+KNO3+H2O配平上述反应的化学方程式
更新时间:2019/01/08 19:42:10
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】化学与生产、生活密切相关,回答下列问题:
(1)如图为刻蚀在玻璃上的精美花纹图案,工人师傅常用_______ 刻蚀玻璃。

(2)金属钠着火时不能用水灭火,原因是_______ (用离子方程式表示)。
(3)下列物质:空气、氧气、食盐水、氢氧化钾、铜、蔗糖中,属于电解质的是_______ ,属于非电解质的是_______ 。
(4)已知某植物营养液配方为0.3 mol KCl、0.2 mol K2SO4、0.1 mol ZnSO4和1 L水。若以KCl、K2SO4、ZnCl2和1 L水为原料配得相同组成的营养液,则需K2SO4的物质的量为_______ mol。
(5)下列生产、生活中的事例中发生了氧化还原反应的是_______ (填字母)。
(6)“雷雨肥庄稼”涉及的化学方程式为_______ 、_______ 、_______ 。
(1)如图为刻蚀在玻璃上的精美花纹图案,工人师傅常用

(2)金属钠着火时不能用水灭火,原因是
(3)下列物质:空气、氧气、食盐水、氢氧化钾、铜、蔗糖中,属于电解质的是
(4)已知某植物营养液配方为0.3 mol KCl、0.2 mol K2SO4、0.1 mol ZnSO4和1 L水。若以KCl、K2SO4、ZnCl2和1 L水为原料配得相同组成的营养液,则需K2SO4的物质的量为
(5)下列生产、生活中的事例中发生了氧化还原反应的是
 |  |  |  |
| A.铁的冶炼 | B.早期的农业耕作 | C.简单机械织布 | D.祥云火炬燃烧 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用双线桥表示反应的电子转移方向和数目:____ 。该反应中氧化剂为_______ ,还原剂为_________
(2)写出NH4Cl在溶液中的电离方程式___ ,在其溶液中分散质粒子的直径范围为___ 。
(3)将1mol/LFeCl3饱和溶液滴入煮沸的蒸馏水中,继续加热至液体变为红褐色,得到的是__________ ;Fe(OH)3胶体与Fe(OH)3沉淀的本质区别在于_________ 。
(1)用双线桥表示反应的电子转移方向和数目:
(2)写出NH4Cl在溶液中的电离方程式
(3)将1mol/LFeCl3饱和溶液滴入煮沸的蒸馏水中,继续加热至液体变为红褐色,得到的是
您最近半年使用:0次
【推荐3】分析以下A~D四个涉及H2O2的反应(未配平),填空:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是__ ,H2O2仅体现还原性的反应是___ ,H2O2既体现氧化性,又体现还原性的反应是___ ,H2O2既不作氧化剂又不作还原剂的反应是___ (填序号)。
(2)用单线桥法表示D反应中电子转移的方向和数目:___ 。
3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
该反应中氧化剂是___ ,氧化产物是___ 。
(3)配平下列反应的化学方程式
①P+CuSO4+H2O=Cu+H3PO4+H2SO4:___ 。
②FeSO4+H2O+O2=Fe2(SO4)3+Fe(OH)3↓:___ 。
③C6H12O6+NaClO3+H2SO4=ClO2↑+CO2↑+H2O+Na2SO4:___ 。
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是
(2)用单线桥法表示D反应中电子转移的方向和数目:
3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
该反应中氧化剂是
(3)配平下列反应的化学方程式
①P+CuSO4+H2O=Cu+H3PO4+H2SO4:
②FeSO4+H2O+O2=Fe2(SO4)3+Fe(OH)3↓:
③C6H12O6+NaClO3+H2SO4=ClO2↑+CO2↑+H2O+Na2SO4:
您最近半年使用:0次
【推荐1】填空。
(1)请用双线桥法表示反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O的电子转移:_______ 。该反应的氧化剂是_______ ,氧化产物是_______ ,若该反应转移的电子数是3mol,则生成的NO气体的体积是_______ L(标准状况下),被还原硝酸的物质的量是_______ mol。
(2)一种制备高效氧化型漂白剂NaClO2的实验流程如图所示
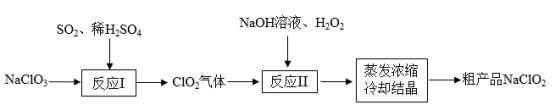
①反应Ⅰ的化学方程式为:3NaClO3+4SO2+3H2O=2ClO2+Na2SO4+3H2SO4+NaCl;反应Ⅰ中氧化产物和还原产物物质的量之比为_______ ,反应Ⅱ中H2O2做_______ (填“氧化剂”或“还原剂”)
②写出NaClO2的电离方程式:_____ ;该漂白剂与HClO的漂白原理______ 相同(填“是”或“否”)
(1)请用双线桥法表示反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O的电子转移:
(2)一种制备高效氧化型漂白剂NaClO2的实验流程如图所示

①反应Ⅰ的化学方程式为:3NaClO3+4SO2+3H2O=2ClO2+Na2SO4+3H2SO4+NaCl;反应Ⅰ中氧化产物和还原产物物质的量之比为
②写出NaClO2的电离方程式:
您最近半年使用:0次
【推荐2】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)被还原的元素是___________ ,还原剂是___________ ,还原产物是___________ 。
(2)该反应中的氧化剂与还原剂个数之比是___________ 。
(3)12个Na2SO3恰好与4个K2Cr2O7完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为___________ 。
(4)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:KMnO4+HCl(浓)—KCl+MnCl2+Cl2↑+H2O(未配平)。配平该化学方程式并用单线桥 法标出电子转移情况___________ 。
(1)被还原的元素是
(2)该反应中的氧化剂与还原剂个数之比是
(3)12个Na2SO3恰好与4个K2Cr2O7完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
(4)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:KMnO4+HCl(浓)—KCl+MnCl2+Cl2↑+H2O(未配平)。配平该化学方程式并用
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】亚硝酸钠易溶于水,水溶液显碱性,有氧化性,也有还原性。由于NaNO2有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
___ NaNO2+___ KI+_____ →___ NO↑+___ I2+___ K2SO4+___ Na2SO4+______
(1)请完成该化学方程式并配平。
(2)将上述反应方程式改写为离子反应方程式:______________________ ;
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是______________________ 。从环保角度来讲,要处理NaNO2,所用的物质的______ (填“氧化性”或“还原性”)应该比KI更________ (填“强”或“弱”)。
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式并用单线桥表示其电子转移的方向和数目_____________________________ 。
(1)请完成该化学方程式并配平。
(2)将上述反应方程式改写为离子反应方程式:
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式并用单线桥表示其电子转移的方向和数目
您最近半年使用:0次
【推荐1】二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。已知:工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。完成下列填空:
(1)请配平下列反应的化学方程式(CH3OH中H为+1价,O为-2价):_____ 。
_______CH3OH +______NaClO3 +_______ →______CO2↑+_______ClO2↑+________ Na2SO4 +___________H2O
→______CO2↑+_______ClO2↑+________ Na2SO4 +___________H2O
该反应中,被氧化的元素是___________ ,还原产物与氧化产物的物质的量之比是___________ 。
(2)根据上述反应可推知___________
a.氧化性:C1O2>NaClO3 b.氧化性:NaClO3>CH3OH
c.还原性:CH3OH>ClO2 d.还原性:CH3OH>Na2SO4
(3)若转移的电子数目为0.3NA(NA为阿伏加德罗常数),则反应产生气体(标准状况)为___________ 升。
(1)请配平下列反应的化学方程式(CH3OH中H为+1价,O为-2价):
_______CH3OH +______NaClO3 +_______
 →______CO2↑+_______ClO2↑+________ Na2SO4 +___________H2O
→______CO2↑+_______ClO2↑+________ Na2SO4 +___________H2O该反应中,被氧化的元素是
(2)根据上述反应可推知
a.氧化性:C1O2>NaClO3 b.氧化性:NaClO3>CH3OH
c.还原性:CH3OH>ClO2 d.还原性:CH3OH>Na2SO4
(3)若转移的电子数目为0.3NA(NA为阿伏加德罗常数),则反应产生气体(标准状况)为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】海水(主要含有NaCl,也含有大量Mg2+、Br-等)可以制备金属镁、溴等物质,其流程如下图:

(1)提取Mg的线路中,如何确定步骤“过滤、洗涤”已洗涤干净,具体操作是____________ 。
(2)工业上由无水MgCl2制取Mg的化学方程式为____________ 。
(3)海水提溴可以通过如下两种方法
方法一:空气吹出SO2吸收法。“吸收”步骤中用SO2水溶液吸收Br2,吸收率可达95%,有关反应的化学方程式为____________ 。
方法二:空气吹出纯碱吸收法。利用热空气将Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3,相关反应为3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2,其中被还原与被氧化的Br2的物质的量之比为____________ ;用稀硫酸酸化吸收液可得到Br2,由此可知酸性条件下的氧化性____________ >____________ 。

(1)提取Mg的线路中,如何确定步骤“过滤、洗涤”已洗涤干净,具体操作是
(2)工业上由无水MgCl2制取Mg的化学方程式为
(3)海水提溴可以通过如下两种方法
方法一:空气吹出SO2吸收法。“吸收”步骤中用SO2水溶液吸收Br2,吸收率可达95%,有关反应的化学方程式为
方法二:空气吹出纯碱吸收法。利用热空气将Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3,相关反应为3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2,其中被还原与被氧化的Br2的物质的量之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】含铜元素的氧化还原反应在工业生产、环保及科研中有广泛的应用。
Ⅰ.碘化亚铜( )是难溶于水的白色固体。碘水因溶解碘单质而呈黄色。
)是难溶于水的白色固体。碘水因溶解碘单质而呈黄色。
已知:氧化性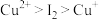 ,还原性
,还原性 。
。
(1) 可用于监测空气中是否含有汞(
可用于监测空气中是否含有汞( )蒸气:
)蒸气: (
( 为+2价)
为+2价) 。其中还原剂为
。其中还原剂为___________ ;每生成1个 原子,电子转移数目为
原子,电子转移数目为___________ 。
(2)久置于空气中的 溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,黄色消失的反应的化学方程式为
溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,黄色消失的反应的化学方程式为__________ 。
(3)根据物质氧化性还原性的强弱推测,在溶液中 和过量的
和过量的 反应的产物是
反应的产物是_____ 、___ 。
Ⅱ.氢化亚铜( )是一种难溶物质,不稳定,易分解,与稀盐酸反应能生成气体。
)是一种难溶物质,不稳定,易分解,与稀盐酸反应能生成气体。 在酸性条件下发生的反应是
在酸性条件下发生的反应是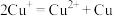 。
。
(4)“与稀盐酸反应能生成气体”的气体为___________ (填化学式)。
(5) 溶解在稀硫酸中反应的离子方程式为
溶解在稀硫酸中反应的离子方程式为___________ 。
Ⅰ.碘化亚铜(
 )是难溶于水的白色固体。碘水因溶解碘单质而呈黄色。
)是难溶于水的白色固体。碘水因溶解碘单质而呈黄色。已知:氧化性
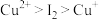 ,还原性
,还原性 。
。(1)
 可用于监测空气中是否含有汞(
可用于监测空气中是否含有汞( )蒸气:
)蒸气: (
( 为+2价)
为+2价) 。其中还原剂为
。其中还原剂为 原子,电子转移数目为
原子,电子转移数目为(2)久置于空气中的
 溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,黄色消失的反应的化学方程式为
溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,黄色消失的反应的化学方程式为(3)根据物质氧化性还原性的强弱推测,在溶液中
 和过量的
和过量的 反应的产物是
反应的产物是Ⅱ.氢化亚铜(
 )是一种难溶物质,不稳定,易分解,与稀盐酸反应能生成气体。
)是一种难溶物质,不稳定,易分解,与稀盐酸反应能生成气体。 在酸性条件下发生的反应是
在酸性条件下发生的反应是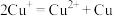 。
。(4)“与稀盐酸反应能生成气体”的气体为
(5)
 溶解在稀硫酸中反应的离子方程式为
溶解在稀硫酸中反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
Ⅰ.(1)所含铁元素既有氧化性又有还原性的物质是________ (填字母)。
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是( )
A. NaNO2被氧化 B. 药品美蓝是还原剂
C. NaNO2是还原剂 D. 药品美蓝被还原
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:________________________________ 。
Ⅱ. 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中Na2O2是________ (填“氧化剂”或“还原剂”)。
(5)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。
、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:__________________________________________ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为________ mol。
Ⅰ.(1)所含铁元素既有氧化性又有还原性的物质是
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A. NaNO2被氧化 B. 药品美蓝是还原剂
C. NaNO2是还原剂 D. 药品美蓝被还原
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
Ⅱ. 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中Na2O2是
(5)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。
、Cl-、H2O。①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列填空:
(1)标况下,0.66g某气态氧化物RO2体积为336mL,此氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(2)相同质量的CO和CO2,它们所含的原子数之比为_______ 。
(3)同温同压下,A容器中充满O2,B容器中充满O3。若两容器中所含原子总数相等,则A容器和B容器的容积比是_______ ,密度之比为_______ ,质量之比为_______ 。
(4)写出实验室制氯气的化学方程式_______ ,在此过程中呈酸性的HCl与参加反应的总HCl的质量之比为_______ ,每产生1mol氯气转移电子数为 _______ 。
(5)配平化学方程式:_______ 。
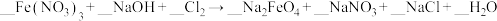
(1)标况下,0.66g某气态氧化物RO2体积为336mL,此氧化物的摩尔质量为
(2)相同质量的CO和CO2,它们所含的原子数之比为
(3)同温同压下,A容器中充满O2,B容器中充满O3。若两容器中所含原子总数相等,则A容器和B容器的容积比是
(4)写出实验室制氯气的化学方程式
(5)配平化学方程式:
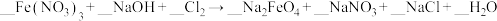
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】磷和砷是同主族的非金属元素。
(1)砷(As)元素位于元素周期表第____ 列;As原子能量最高的3个轨道在空间相互____ ;1个黄砷(As4)分子中含有_____ 个As﹣As键,键角_____ 度.
(2)黑磷的结构与石墨相似.最近中国科学家将黑磷“撕”成了二维结构,硬度和导电能力都大大提高,这种二维结构属于____ (选填编号).
a.离子晶体 b.原子晶体 c.分子晶体 d.其它类型
(3)与硫元素的相关性质比,以下不能说明P的非金属性比S弱的是_____ (选填编号).
a.磷难以与氢气直接化合 b.白磷易自燃 c.P﹣H的键能更小 d.H3PO4酸性更弱
(4)次磷酸钠(NaH2PO2)可用于化学镀镍,即通过化学反应在塑料镀件表面沉积镍﹣磷合金.
化学镀镍的溶液中含有Ni2+和H2PO2﹣,在酸性条件下发生以下镀镍反应:
___ Ni2++___ H2PO2﹣+___ H2O →____ Ni+____ H2PO3﹣+___ H+
①请配平上述化学方程式。
②上述反应中,若生成1mol H2PO3﹣,反应中转移电子的物质的量为______ 。
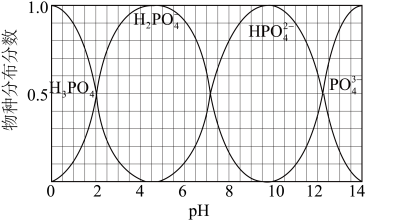
(5)NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。
①pH=8时,溶液中主要含磷物种浓度大小关系为_________________ 。
②为获得尽可能纯的NaH2PO4,pH应控制在______________________________ 。
(1)砷(As)元素位于元素周期表第
(2)黑磷的结构与石墨相似.最近中国科学家将黑磷“撕”成了二维结构,硬度和导电能力都大大提高,这种二维结构属于
a.离子晶体 b.原子晶体 c.分子晶体 d.其它类型
(3)与硫元素的相关性质比,以下不能说明P的非金属性比S弱的是
a.磷难以与氢气直接化合 b.白磷易自燃 c.P﹣H的键能更小 d.H3PO4酸性更弱
(4)次磷酸钠(NaH2PO2)可用于化学镀镍,即通过化学反应在塑料镀件表面沉积镍﹣磷合金.
化学镀镍的溶液中含有Ni2+和H2PO2﹣,在酸性条件下发生以下镀镍反应:
①请配平上述化学方程式。
②上述反应中,若生成1mol H2PO3﹣,反应中转移电子的物质的量为
(5)NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。

①pH=8时,溶液中主要含磷物种浓度大小关系为
②为获得尽可能纯的NaH2PO4,pH应控制在
您最近半年使用:0次



