按要求作答:
(1)1.00gCH4完全燃烧生成液态水和CO2,放出55.6kJ的热量,计算CH4的燃烧热为_____ kJ/mol
(2)4.0g硫粉在O2中完全燃烧生成SO2,放出37kJ热量,计算S的燃烧热为____________ kJ/mol
(3)已知下列反应:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) △H2=-393.5kJ/mol
③H2(g)+1/2O2(g)=H2O(l) △H3=-285.8kJ/mol
则反应2C(s)+2H2(g)+O2(g) =CH3COOH(l)的反应热为△H=_____________ kJ/mol
(1)1.00gCH4完全燃烧生成液态水和CO2,放出55.6kJ的热量,计算CH4的燃烧热为
(2)4.0g硫粉在O2中完全燃烧生成SO2,放出37kJ热量,计算S的燃烧热为
(3)已知下列反应:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) △H2=-393.5kJ/mol
③H2(g)+1/2O2(g)=H2O(l) △H3=-285.8kJ/mol
则反应2C(s)+2H2(g)+O2(g) =CH3COOH(l)的反应热为△H=
更新时间:2019-01-08 20:55:31
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】填空
(1)醋酸在水溶液中的电离方程式为_______ 。
(2)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2固体和H2O(1)。已知室温下2 gSiH4自燃放出热量89.2 kJ,该反应的热化学方程式为:_______ 。
(3)已知反应:N2(g) + O2(g) = 2NO(g) △H1
2H2(g) + O2(g) = 2H2O(g) △H2
N2(g) + 3H2(g) = 2NH3(g) △ H3
利用上述三个反应,计算4NH3(g) + 5O2(g) = 4NO(g) + 6H2O(g)的反应焓变△H4为:_______ (用含△H1、△H2、△H3的式子表示)。
(1)醋酸在水溶液中的电离方程式为
(2)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2固体和H2O(1)。已知室温下2 gSiH4自燃放出热量89.2 kJ,该反应的热化学方程式为:
(3)已知反应:N2(g) + O2(g) = 2NO(g) △H1
2H2(g) + O2(g) = 2H2O(g) △H2
N2(g) + 3H2(g) = 2NH3(g) △ H3
利用上述三个反应,计算4NH3(g) + 5O2(g) = 4NO(g) + 6H2O(g)的反应焓变△H4为:
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学反应过程既是物质的转化过程,也是能量的转化过程。
(1)下列属于吸热过程的是___________ (填序号)。
a.CO燃烧 b.铝和稀盐酸反应 c.碳酸氢钠溶于水 d.石灰石分解
(2)t℃时,关于N2、NH3的两个反应的信息如下表所示:
请写出t℃时,NH3被NO氧化生成无毒气体的热化学方程式___________ (反应热用a、b、c、d代数式表示)。t℃时,该反应的平衡常数___________ (用K1和K2表示)。
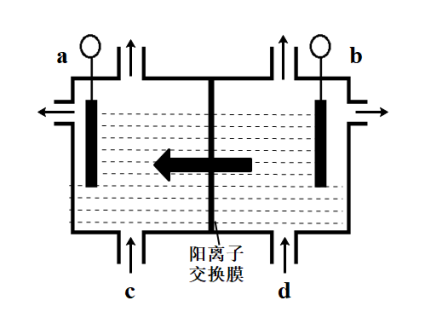
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出如图所示用电解法制取ClO2的新工艺。用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。精制饱和食盐水入口是_______ 口(填“c”或“d”)产生ClO2的电极反应式为_______ 。
(1)下列属于吸热过程的是
a.CO燃烧 b.铝和稀盐酸反应 c.碳酸氢钠溶于水 d.石灰石分解
(2)t℃时,关于N2、NH3的两个反应的信息如下表所示:
| 化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
| N2(g)+O2(g)=2NO(g) △H>0 | akJ/mol | bkJ/mol | K1 |
| 4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H<0 | ckJ/mol | dkJ/mol | K2 |
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出如图所示用电解法制取ClO2的新工艺。用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。精制饱和食盐水入口是

您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为____ 。
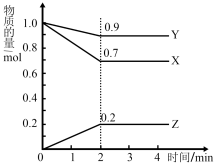
反应开始至2min,Z的平均反应速率为____ 。
(2)甲烷作为能源燃烧放出大量的热,已知:
①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H1=-1214kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2=-566kJ/mol
则表示甲烷燃烧热的热化学方程式____ 。
(1)某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为

反应开始至2min,Z的平均反应速率为
(2)甲烷作为能源燃烧放出大量的热,已知:
①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H1=-1214kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2=-566kJ/mol
则表示甲烷燃烧热的热化学方程式
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】已知下列两个热化学方程式:H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ/mol,C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=-2220.0kJ/mol。
(1)H2的燃烧热为_______ ,C3H8的燃烧热为_______ 。
(2)实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态的水时放热6264.5kJ,则混合气体中H2和C3H8的体积比是_______ 。
(3)1molH2和2molC3H8组成的混合气体完全燃烧释放的热量为:_______ 。
(4)已知H2O(l)=H2O(g) △H=+44kJ/mol。写出丙烷燃烧生成CO2和气态水的热化学方程式:_______ 。
(1)H2的燃烧热为
(2)实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态的水时放热6264.5kJ,则混合气体中H2和C3H8的体积比是
(3)1molH2和2molC3H8组成的混合气体完全燃烧释放的热量为:
(4)已知H2O(l)=H2O(g) △H=+44kJ/mol。写出丙烷燃烧生成CO2和气态水的热化学方程式:
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)===2H2O(1) ΔH=-572 kJ·mol-1。请回答下列问题:
(1)生成物能量总和________ (填“大于”“小于”或“等于”)反应物能量总和。
(2)若2 mol氢气燃烧生成水蒸气,则放出的热量________ (填“大于”“小于”或“等于”)572 kJ。
(3)H2的标准燃烧热ΔH=________ 。
(1)生成物能量总和
(2)若2 mol氢气燃烧生成水蒸气,则放出的热量
(3)H2的标准燃烧热ΔH=
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求填空
(1)Cr2O 的颜色是
的颜色是___________ 。
(2)已知:16.0g甲烷气体完全燃烧生成液态水放出的热量为890.3kJ(298K、1.01×105Pa时测定)。写出该条件下,甲烷燃烧的热化学方程式___________ 。
(1)Cr2O
 的颜色是
的颜色是(2)已知:16.0g甲烷气体完全燃烧生成液态水放出的热量为890.3kJ(298K、1.01×105Pa时测定)。写出该条件下,甲烷燃烧的热化学方程式
您最近半年使用:0次
【推荐1】盖斯定律:内容:1840年,瑞典化学家盖斯通过大量实验证明:不管化学反应是_______ 完成或__________ 完成,其反应热是_______ 的。也就是说,化学反应的反应热只与反应体系的_____ 和______ 有关而与反应的途径无关。
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】醇是重要的有机化工原料。一定条件下,甲醇可同时发生下面两个反应:
i .2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
ii.2CH3OH(g) C2H4(g)+2H2O(g)
C2H4(g)+2H2O(g)
(1)上述反应过程中能量变化如图所示:
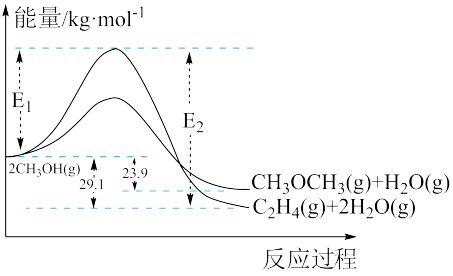
在某密闭容器中,充入一定量CH3OH(g)发生上述两个反应,反应________ (填“i”或“ii”)的速率较大,其原因为___________ 。若在容器中加入催化剂,使ii的反应速率增大,则E1和E2−E1的变化是:E1__________ ;E2−E1___________ (填“增大”、“减小”或“不变”)。
(2)已知:CH3CH2OH(g)=CH3OCH3(g) ΔH =+50.7 kJ∙mol−1。则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的ΔH=______ 。
i .2CH3OH(g)
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)ii.2CH3OH(g)
 C2H4(g)+2H2O(g)
C2H4(g)+2H2O(g)(1)上述反应过程中能量变化如图所示:

在某密闭容器中,充入一定量CH3OH(g)发生上述两个反应,反应
(2)已知:CH3CH2OH(g)=CH3OCH3(g) ΔH =+50.7 kJ∙mol−1。则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的ΔH=
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】已知E1=134kJ·mol-1、E2=368kJ·mol-1请参考题中图表,按要求填空:
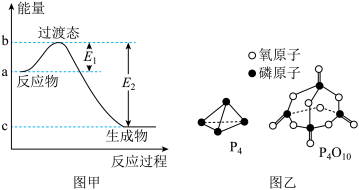
(1)图甲是1mol NO2(g)和1mol CO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂。反应速率加快,E1的变化是___________ (填“增大”“减小”或“不变”,下同),ΔH的变化是___________ ,请写出NO2和CO反应的热化学方程式:___________ 。
(2)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g) (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g) NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g) 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
则ΔH3与ΔH1、ΔH2之间的关系是ΔH3=___________ 。
(3)下表所示是部分化学键的键能参数。
已知P4(g)+5O2(g)═P4O10(g) ΔH=-dkJ•mol-1,P4及P4O10的结构如图乙所示。表中x=___________ kJ·mol-1。(用含a、b、c、d的代数式表示)

(1)图甲是1mol NO2(g)和1mol CO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂。反应速率加快,E1的变化是
(2)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)
 (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1反应Ⅱ:NH3(l)+H2O(l)+CO2(g)
 NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)
 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3则ΔH3与ΔH1、ΔH2之间的关系是ΔH3=
(3)下表所示是部分化学键的键能参数。
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ·mol-1 | a | b | c | x |
您最近半年使用:0次

 的燃烧热为
的燃烧热为 ,则
,则
 。
。 )气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
)气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
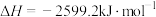 。则1kg乙炔在氧气中完全燃烧放出多少热
。则1kg乙炔在氧气中完全燃烧放出多少热


