将5 g钠铝合金投入200 mL的水中,固体完全溶解,产生4.48 L(标准状况下)气体,溶液中只有一种溶质。试计算(写出计算过程):
(1)钠铝合金中两金属的物质的量_______ ;
(2)所得溶液的物质的量浓度_______ 。(假设溶液体积变化忽略不计)
(1)钠铝合金中两金属的物质的量
(2)所得溶液的物质的量浓度
更新时间:2020-09-23 10:47:49
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】高性能磁带的磁粉主要成分是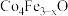 ,某探究小组设计了下图所示流程制取
,某探究小组设计了下图所示流程制取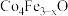 ,图中正极材料的主要成分是
,图中正极材料的主要成分是 ,还含有少量Al和Fe,{已知常温下,
,还含有少量Al和Fe,{已知常温下,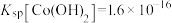 }。
}。

在空气中加热 ,固体残留率随温度的变化如图所示,则A点主要的固体产物为
,固体残留率随温度的变化如图所示,则A点主要的固体产物为_______ (属于氧化物,填化学式)。

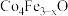 ,某探究小组设计了下图所示流程制取
,某探究小组设计了下图所示流程制取 ,图中正极材料的主要成分是
,图中正极材料的主要成分是 ,还含有少量Al和Fe,{已知常温下,
,还含有少量Al和Fe,{已知常温下,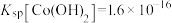 }。
}。
在空气中加热
 ,固体残留率随温度的变化如图所示,则A点主要的固体产物为
,固体残留率随温度的变化如图所示,则A点主要的固体产物为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】物质的量是高中化学中常用的物理量,请按要求完成下列各小题。
(1)9.03×1023个NH3含___________ mol氢原子,___________ mol质子,在标准状况下的体积约为___________ L,氮原子与氢原子个数比___________ 。
(2)___________ molCO2分子中含有的氧原子数与1.806×1024个H2O中含有的氧原子数相同。
(3)在NaCl、MgCl2、MgSO4形成的混合溶液中,C(Na+)=0.10mol·L-1,C(Mg2+)=0.25mol·L-1,C(Cl-)=0.20mol·L-1,则C(S )为
)为___________ 。
(1)9.03×1023个NH3含
(2)
(3)在NaCl、MgCl2、MgSO4形成的混合溶液中,C(Na+)=0.10mol·L-1,C(Mg2+)=0.25mol·L-1,C(Cl-)=0.20mol·L-1,则C(S
 )为
)为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】(Ⅰ)把15.6gNa2O2放入100mL水中,充分反应后,计算:
(1)生成O2在标准状况的体积___________ mL;
(2)反应后所得NaOH的物质的量浓度___________ 。(反应前后溶液体积变化忽略不计)。
(Ⅱ)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经检验该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为4:1。
(3)检验该溶液中无Fe3+的方法及现象____________ 。
(4)则原混合物中Fe2O3与Fe的物质的量之比为___________ 。
(5)若原混合物中铁元素的总物质的量为6mol,则反应中生成H2的为_______ L(标准状况)。
(1)生成O2在标准状况的体积
(2)反应后所得NaOH的物质的量浓度
(Ⅱ)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经检验该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为4:1。
(3)检验该溶液中无Fe3+的方法及现象
(4)则原混合物中Fe2O3与Fe的物质的量之比为
(5)若原混合物中铁元素的总物质的量为6mol,则反应中生成H2的为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】一般情况下,较强的氧化剂如:MnO2、KMnO4、KClO3、Ca(ClO)2等氧化浓盐酸时,有如下反应规律:氧化剂+浓盐酸→金属氯化物+水+氯气。实验室通常用该原理制取少量Cl2。
(1)将214.5gCa(ClO)2放入500mL12.0mol/L的浓盐酸中,生成的Cl2在标准状况下的体积为39.2L。若反应前后溶液的体积保持不变,计算反应后溶液中HCl的物质的量浓度。_______
(2)漂白粉是 Ca(ClO)2、CaCl2 、Ca(OH)2 、H2O 和 CaO 的混合物。漂白粉放出的氯气具有漂白作用,叫有效氯。通常用有效氯表示漂白粉的纯度。漂白粉中的有效氯含量常用滴定碘法进行测定,即在一定量的漂白粉中加入过量的KI ,加H2SO4酸化,有效氯与I-作用析出等量的I2,析出的I2以淀粉指示剂立即用Na2S2O3标准溶液滴定。若测定漂白粉中有效氯时用盐酸酸化,则盐酸的浓度应小于_______ mol/L,否则测定的有效氯将_______ (选填“偏高”、“偏低”或“不变”)。
(1)将214.5gCa(ClO)2放入500mL12.0mol/L的浓盐酸中,生成的Cl2在标准状况下的体积为39.2L。若反应前后溶液的体积保持不变,计算反应后溶液中HCl的物质的量浓度。
(2)漂白粉是 Ca(ClO)2、CaCl2 、Ca(OH)2 、H2O 和 CaO 的混合物。漂白粉放出的氯气具有漂白作用,叫有效氯。通常用有效氯表示漂白粉的纯度。漂白粉中的有效氯含量常用滴定碘法进行测定,即在一定量的漂白粉中加入过量的KI ,加H2SO4酸化,有效氯与I-作用析出等量的I2,析出的I2以淀粉指示剂立即用Na2S2O3标准溶液滴定。若测定漂白粉中有效氯时用盐酸酸化,则盐酸的浓度应小于
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)将30mL0.5mol/L的H2SO4溶液加水稀释到500mL后,从中取出50mL溶液的物质的量浓度为___ 。
(2)常温下,将20.0g14%的NaOH溶液跟30.0g24%的NaOH溶液混合,混合后得到1.2g/mL的混合液,试计算:
①混合后的溶液中NaOH的质量分数为___ 。
②混合后的溶液中NaOH的物质的量浓度为___ mol/L。
③配制100mL同浓度溶液需要溶解___ g的NaOH才能使其浓度与上述混合液浓度相等。
(3)在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g,该混合气体中,CO和CO2的物质的量之比为___ 。
(2)常温下,将20.0g14%的NaOH溶液跟30.0g24%的NaOH溶液混合,混合后得到1.2g/mL的混合液,试计算:
①混合后的溶液中NaOH的质量分数为
②混合后的溶液中NaOH的物质的量浓度为
③配制100mL同浓度溶液需要溶解
(3)在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g,该混合气体中,CO和CO2的物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】设阿伏加德罗常数的值为6.02×1023。
(1)0.3 mol NH3分子中所含原子数目与___________ 个H2O分子中所含原子数目相等。
(2)在0.5L含有质量为10.8克Al3+的Al2(SO4)3溶液中所含SO 的物质的量浓度为
的物质的量浓度为____ 。
(3)同温、同压下,有五种物质:①6g H2,②0.5 mol CO2,③1.204×1024个氯化氢分子,④147g硫酸,⑤92g乙醇(C2H5OH)。它们的物质的量最大的是______ (填序号,下同),含有原子个数最多的是___ ,质量最大的是___ 。
(4)9.5 g某二价金属氯化物(ACl2)中含有0.2 mol Cl-,则ACl2的摩尔质量是_______ ;A的相对原子质量是______ ;ACl2的化学式是______ 。
(1)0.3 mol NH3分子中所含原子数目与
(2)在0.5L含有质量为10.8克Al3+的Al2(SO4)3溶液中所含SO
 的物质的量浓度为
的物质的量浓度为(3)同温、同压下,有五种物质:①6g H2,②0.5 mol CO2,③1.204×1024个氯化氢分子,④147g硫酸,⑤92g乙醇(C2H5OH)。它们的物质的量最大的是
(4)9.5 g某二价金属氯化物(ACl2)中含有0.2 mol Cl-,则ACl2的摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】将一定质量的镁铝合金投入 一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为
一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为 的
的 溶液,生成的沉淀跟加入的
溶液,生成的沉淀跟加入的 溶液的体积关系如图。(横坐标体积单位是
溶液的体积关系如图。(横坐标体积单位是 ,纵坐标质量单位是g)求:
,纵坐标质量单位是g)求:
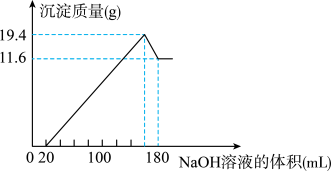
(1)合金中 ,
, 的质量
的质量_____________
(2)所用 的物质的量浓度
的物质的量浓度___________
 一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为
一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为 的
的 溶液,生成的沉淀跟加入的
溶液,生成的沉淀跟加入的 溶液的体积关系如图。(横坐标体积单位是
溶液的体积关系如图。(横坐标体积单位是 ,纵坐标质量单位是g)求:
,纵坐标质量单位是g)求:
(1)合金中
 ,
, 的质量
的质量(2)所用
 的物质的量浓度
的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】称取一定质量镁铝合金放入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图(生成沉淀阶段的图象斜率视为恒定)。
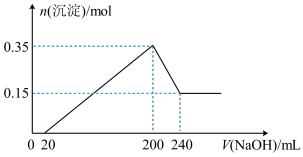
计算:
(1)合金中Al的质量为多少____ ?
(2)所加NaOH溶液的物质的量浓度为多少____ ?

计算:
(1)合金中Al的质量为多少
(2)所加NaOH溶液的物质的量浓度为多少
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求完成下列填空:
(1)某金属氯化物 的摩尔质量为
的摩尔质量为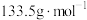 ,取该金属氯化物
,取该金属氯化物 配成水溶液,与足量
配成水溶液,与足量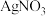 溶液完全反应,生成
溶液完全反应,生成 白色沉淀。则金属M的摩尔质量为
白色沉淀。则金属M的摩尔质量为_______ 。
(2)某物质A加热时按化学方程式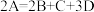 分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对
分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对 的相对密度为20,则反应物A的相对分子质量为
的相对密度为20,则反应物A的相对分子质量为_______ 。
(3)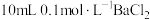 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是_______ 。
(4)一定量的液态化合物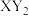 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: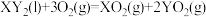 ,冷却后在标准状况下,测得生成物的体积为
,冷却后在标准状况下,测得生成物的体积为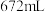 ,则(l表示液态,g表示气态):
,则(l表示液态,g表示气态):
①反应前 的体积是
的体积是_______  。
。
②在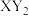 分子中,X、Y两元素的质量比为3∶16,则X、Y两元素的相对原子质量之比为
分子中,X、Y两元素的质量比为3∶16,则X、Y两元素的相对原子质量之比为_______ 。
(5) 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应后,得到
充分反应后,得到 和
和 的混合溶液,向上述所得溶液中,逐滴滴加
的混合溶液,向上述所得溶液中,逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
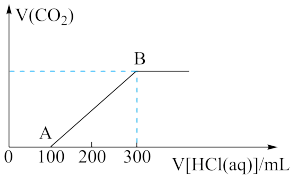
①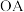 段、
段、 段发生反应的化学方程式
段发生反应的化学方程式_______ 、_______ 。
②B点时,反应所得溶液中溶质的物质的量浓度是_______ 。
③混合溶液中 和
和 的质量比是
的质量比是_______ 。
(1)某金属氯化物
 的摩尔质量为
的摩尔质量为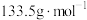 ,取该金属氯化物
,取该金属氯化物 配成水溶液,与足量
配成水溶液,与足量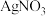 溶液完全反应,生成
溶液完全反应,生成 白色沉淀。则金属M的摩尔质量为
白色沉淀。则金属M的摩尔质量为(2)某物质A加热时按化学方程式
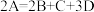 分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对
分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对 的相对密度为20,则反应物A的相对分子质量为
的相对密度为20,则反应物A的相对分子质量为(3)
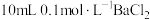 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是(4)一定量的液态化合物
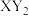 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: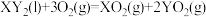 ,冷却后在标准状况下,测得生成物的体积为
,冷却后在标准状况下,测得生成物的体积为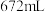 ,则(l表示液态,g表示气态):
,则(l表示液态,g表示气态):①反应前
 的体积是
的体积是 。
。②在
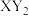 分子中,X、Y两元素的质量比为3∶16,则X、Y两元素的相对原子质量之比为
分子中,X、Y两元素的质量比为3∶16,则X、Y两元素的相对原子质量之比为(5)
 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应后,得到
充分反应后,得到 和
和 的混合溶液,向上述所得溶液中,逐滴滴加
的混合溶液,向上述所得溶液中,逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
①
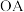 段、
段、 段发生反应的化学方程式
段发生反应的化学方程式②B点时,反应所得溶液中溶质的物质的量浓度是
③混合溶液中
 和
和 的质量比是
的质量比是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】计算
(1)已知酸性条件下, 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,
①写出该反应的离子方程式______ 。
②被还原的 的质量为
的质量为______ 。
(2)为了检验某含有 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为______ (用含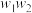 的代数式来表示)。
的代数式来表示)。
(3)有一块表面氧化成氧化钠的金属钠,总质量为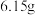 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程_____ 。
(1)已知酸性条件下,
 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,①写出该反应的离子方程式
②被还原的
 的质量为
的质量为(2)为了检验某含有
 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为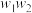 的代数式来表示)。
的代数式来表示)。(3)有一块表面氧化成氧化钠的金属钠,总质量为
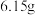 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】把2.3 g钠投入足量水中,充分反应后所得溶液用水稀释至100 mL。求:
(1)生成标准状况下的氢气多少升_______ ;
(2)所得的溶液物质的量浓度_______ ?
(1)生成标准状况下的氢气多少升
(2)所得的溶液物质的量浓度
您最近一年使用:0次



