工业上合成CH3OH的原理为:2H2(g)+CO CH3OH(g),一定温度下,向1L恒容密闭容器中充入H2和CO,反应达平衡时CH3OH的体积分数与反应物投料之比(n(H2)/n(CO))的关系如图所示。下列说法错误的是
CH3OH(g),一定温度下,向1L恒容密闭容器中充入H2和CO,反应达平衡时CH3OH的体积分数与反应物投料之比(n(H2)/n(CO))的关系如图所示。下列说法错误的是
 CH3OH(g),一定温度下,向1L恒容密闭容器中充入H2和CO,反应达平衡时CH3OH的体积分数与反应物投料之比(n(H2)/n(CO))的关系如图所示。下列说法错误的是
CH3OH(g),一定温度下,向1L恒容密闭容器中充入H2和CO,反应达平衡时CH3OH的体积分数与反应物投料之比(n(H2)/n(CO))的关系如图所示。下列说法错误的是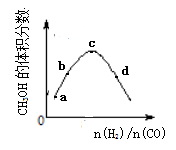
| A.相同条件下,达到平衡时混合气体的密度与反应前相同 |
| B.a、b、c、d四点中,c点CO的转化率最大。 |
| C.若投料时n(CO)不变,a、b、c、d四点中d处CH3OH的物质的量最大 |
| D.图象中 c点到d点,平衡向正反应方向移动 |
更新时间:2019-01-29 08:37:54
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】将一定量氨基甲酸铵加入恒容容器中:NH2COONH4(s) 2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是

 2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是 
| A.该反应的生成物总能量大于反应物总能量 |
| B.处于A点的CO2的消耗速率大于处于C点的CO2消耗速率 |
| C.B点时,v逆>v正 |
| D.CO2的体积分数不变时反应一定达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】每年10月23日上午6:02到下午6:02被脊为“摩尔日”(MoleDay) ,这个时间的美式写法为6:02/10/23 ,外观与阿伏加德罗常数的值6.02 ×1023相似。设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.39 g Na2S和Na2O2组成的混合物中,含有阴离子的数目为0.5 NA |
| B.0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,HI分子总数为0.2 NA |
| C.1 L0.1 mol·L-1CH3COOH水溶液中含有的氧原子数为0.2 NA |
| D.46g分子式为C2H6O的有机物含有的共价键数目为9 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作及现象、得出的结论及解释,均正确的是
选项 | 实验操作及现象 | 结论及解释 |
A | 常温下,用胶头滴管将待测NaClO溶液滴在pH试纸上,与标准比色卡对照, | NaClO溶液显碱性 |
B | 在KSCN与 的混合液中再加入少量KCl固体,溶液颜色加深 的混合液中再加入少量KCl固体,溶液颜色加深 | 增大 浓度,平衡正向移动 浓度,平衡正向移动 |
C | 在相同条件下,向一支试管中加入2 mL 5% 溶液,向另一支试管中加入2 mL 5% 溶液,向另一支试管中加入2 mL 5% 溶液和1 mL 溶液和1 mL 溶液,可观察到后者产生气泡速率更快 溶液,可观察到后者产生气泡速率更快 |  可加快 可加快 分解速率 分解速率 |
D | 在室温下,用pH计分别测定 的 的 溶液、 溶液、 的 的 溶液的pH,前者大于后者 溶液的pH,前者大于后者 | 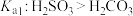 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】可逆反应:2HI(g) H2(g)+I2(g);△H>0。在密闭容器中进行,当达到平衡时欲使混合气体的颜色加深,应采取的措施
H2(g)+I2(g);△H>0。在密闭容器中进行,当达到平衡时欲使混合气体的颜色加深,应采取的措施
 H2(g)+I2(g);△H>0。在密闭容器中进行,当达到平衡时欲使混合气体的颜色加深,应采取的措施
H2(g)+I2(g);△H>0。在密闭容器中进行,当达到平衡时欲使混合气体的颜色加深,应采取的措施| A.加入催化剂 | B.降低温度 | C.增大容器体积 | D.充入HI气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】向绝热恒容密闭容器中通入一定量的 和
和 ,一定条件下发生反应:
,一定条件下发生反应:
 ,测得
,测得 浓度随时间变化如表所示,下列说法正确的是
浓度随时间变化如表所示,下列说法正确的是
 和
和 ,一定条件下发生反应:
,一定条件下发生反应:
 ,测得
,测得 浓度随时间变化如表所示,下列说法正确的是
浓度随时间变化如表所示,下列说法正确的是| 反应时间/s | 40 | 50 | 60 | 70 | 80 | 90 | 100 | 110 |
 浓度 浓度 | 0.10 | 0.14 | 0.21 | 0.26 | 0.30 | 0.32 | 0.33 | 0.33 |
A.50s时, 的生成速率为 的生成速率为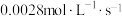 |
B.40s~90s时段: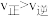 |
| C.0s~50s的反应速率等于70s~80s的反应速率 |
D.110s时,缩小容器体积再次达到平衡后, 的转化率和浓度均保持不变 的转化率和浓度均保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列叙述与图像对应相符合的是


A.图甲表示:一定温度下,将一定量的冰醋酸加水稀释,导电能力的变化,a、b、c三点 的电离程度:a<c<b 的电离程度:a<c<b |
| B.图乙表示:稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则HB酸性更强 |
C.图丙表示:反应 ,在 ,在 时迅速将体积缩小后 时迅速将体积缩小后 的变化 的变化 |
D.图丁表示:反应 ,物质的含量和压强关系,可知E点v(逆)<v(正) ,物质的含量和压强关系,可知E点v(逆)<v(正) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
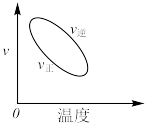
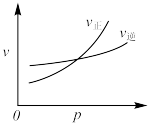
【推荐3】化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是
 |  |  |  |
| ① | ② | ③ | ④ |
| A.根据图①可判断该可逆反应正反应为吸热反应 |
B.图②可表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,且乙的压强大 3C(g)+D(s)的影响,且乙的压强大 |
| C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D.根据图④,若要除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调节pH至4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐1】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g) COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
CO(g)+H2S(g)
 COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
| A.升高温度,H2S浓度增加,表明该反应是吸热反应 |
| B.通入CO后,正反应速率逐渐增大 |
| C.反应前H2S物质的量为7mol |
| D.CO的平衡转化率为80% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】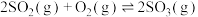
 ,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入6mol
,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入6mol  和3mol
和3mol  ,乙容器恒温恒容,充入6mol
,乙容器恒温恒容,充入6mol  ,丙容器恒温恒压,充入6mol
,丙容器恒温恒压,充入6mol  ,充分反应达到平衡,下列说法正确的是
,充分反应达到平衡,下列说法正确的是
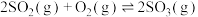
 ,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入6mol
,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入6mol  和3mol
和3mol  ,乙容器恒温恒容,充入6mol
,乙容器恒温恒容,充入6mol  ,丙容器恒温恒压,充入6mol
,丙容器恒温恒压,充入6mol  ,充分反应达到平衡,下列说法正确的是
,充分反应达到平衡,下列说法正确的是A.乙中 的体积分数大于丙 的体积分数大于丙 | B.转化率: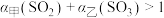 |
C.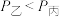 | D.甲和丙中反应的化学平衡常数互为倒数 |
您最近一年使用:0次

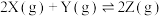 ,若
,若 的起始浓度为
的起始浓度为 (均不为0),当达到平衡时浓度分别为
(均不为0),当达到平衡时浓度分别为 ,则下列判断正确的是
,则下列判断正确的是 和
和 的生成速率之比为
的生成速率之比为
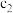 的取值范围
的取值范围
 和
和
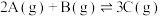
 的正确图像是
的正确图像是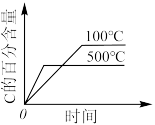

 2SO3(g)并达到平衡。在反应过程中,若甲容器的容积不变,乙容器的压强不变,甲中SO2的转化率为a%,乙容器中SO2的转化率为b%,则a与b的关系为
2SO3(g)并达到平衡。在反应过程中,若甲容器的容积不变,乙容器的压强不变,甲中SO2的转化率为a%,乙容器中SO2的转化率为b%,则a与b的关系为