向绝热恒容密闭容器中通入一定量的 和
和 ,一定条件下发生反应:
,一定条件下发生反应:
 ,测得
,测得 浓度随时间变化如表所示,下列说法正确的是
浓度随时间变化如表所示,下列说法正确的是
 和
和 ,一定条件下发生反应:
,一定条件下发生反应:
 ,测得
,测得 浓度随时间变化如表所示,下列说法正确的是
浓度随时间变化如表所示,下列说法正确的是| 反应时间/s | 40 | 50 | 60 | 70 | 80 | 90 | 100 | 110 |
 浓度 浓度 | 0.10 | 0.14 | 0.21 | 0.26 | 0.30 | 0.32 | 0.33 | 0.33 |
A.50s时, 的生成速率为 的生成速率为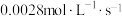 |
B.40s~90s时段: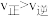 |
| C.0s~50s的反应速率等于70s~80s的反应速率 |
D.110s时,缩小容器体积再次达到平衡后, 的转化率和浓度均保持不变 的转化率和浓度均保持不变 |
更新时间:2022-11-10 22:39:20
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】一定条件下,向1L恒容密闭容器中通入2mol CO2和8mol H2发生反应:CO2(g) +4H2(g) CH4(g) +2H2O(g) ,5min后,测得CO2的物质的量为1.2mol ,则0~5min内用H2表示的化学反应速率是
CH4(g) +2H2O(g) ,5min后,测得CO2的物质的量为1.2mol ,则0~5min内用H2表示的化学反应速率是
 CH4(g) +2H2O(g) ,5min后,测得CO2的物质的量为1.2mol ,则0~5min内用H2表示的化学反应速率是
CH4(g) +2H2O(g) ,5min后,测得CO2的物质的量为1.2mol ,则0~5min内用H2表示的化学反应速率是| A.0.16mol·L-1·min -1 | B.0.24mol·L-1·min -1 | C.0.64mol·L-1·min -1 | D.0.96mol·L-1·min -1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,向2L恒容密闭容器中加入6molA和2molB,发生如下反应: ;2min时,剩余1.2molB,并测得C的浓度为0.8mol/L。下列说法正确的是
;2min时,剩余1.2molB,并测得C的浓度为0.8mol/L。下列说法正确的是
 ;2min时,剩余1.2molB,并测得C的浓度为0.8mol/L。下列说法正确的是
;2min时,剩余1.2molB,并测得C的浓度为0.8mol/L。下列说法正确的是| A.x=1 |
B.0~2min内,A的平均反应速率为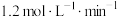 |
| C.当容器内剩余0.4molB时,反应时间为4min |
| D.其它条件相同,若起始时向1L容器中充入6molA和2molB,当剩余1.2molB时,消耗时间小于2min |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】在t℃时,某体积可变的密闭容器内,加入适量反应物发生反应:mA(g)+nB(g) pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:
pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:
则下列有关说法中不正确的是()
 pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:
pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:| 压强 | c(A) | 重新达到平衡所需时间 | |
| 第一次达到平衡 | 2×105Pa | 0.08mol/L | 4min |
| 第二次达到平衡 | 5×105Pa | 0.20mol/L | xmin |
| 第三次达到平衡 | 1×106Pa | 0.44mol/L | 0.8min |
| A.第二次平衡到第三次平衡中,A的平均反应速率为0.3mol/(L·min) |
| B.维持压强为2×105Pa,假设当反应达到平衡状态时体系中共有amol气体,再向体系中加入bmolB,则重新达到平衡时体系中共有(a+b)mol气体 |
C.当压强为1×106Pa时,此反应的平衡常数表达式为K=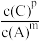 |
| D.m+n=p,x=0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作、现象和所得到的结论均正确的是
| 选项 | 实验内容 | 实验结论 |
| A | 在容积可变的密闭容器中发生反应: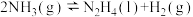 ,把容积的体积缩小一半 ,把容积的体积缩小一半 | 正反应速率加快,逆反应速率减慢 |
| B | 室温下,用pH试纸分别测定浓度为0.1 mol•L-1HClO溶液和0.1 mol•L-1HF溶液的pH,前者pH大于后者 | HClO的酸性小于HF |
| C | 将等浓度等体积的FeCl3溶液和KI溶液混合,充分反应后滴入KSCN溶液,溶液变红 | 溶液中存在平衡: 2Fe3++2I-⇌2Fe2++I2 |
| D | 测量熔融状态下NaHSO4的导电性 | 熔融状态下NaHSO4能电离出Na+、H+、SO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将Al条插入6 mol·L-1盐酸中,反应过程中产生H2速率变化情况如图1所示。下列说法错误的是
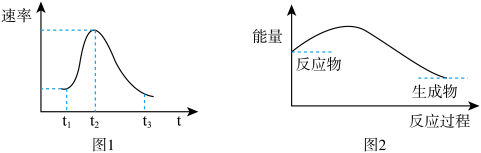

| A.图1中开始阶段产生气体速率较慢可能是因为Al条表面有氧化膜 |
| B.图1中影响t1~t2段速率变化的主要原因是反应放热导致溶液温度升高 |
| C.图1中影响t2~t3速率变化的主要因素是c(Cl-) |
| D.图2可以表示该反应过程的能量变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(p表示压强,T表示温度,n表示物质的量):根据以上规律判断,下列结论正确的是
反应Ⅰ:2A(s)+B(g) 2C(g)
2C(g)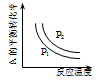 反应Ⅱ:2A(s)
反应Ⅱ:2A(s)  C(g)
C(g)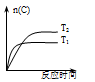
反应Ⅲ:3A(g)+B(g) 2C(g)
2C(g)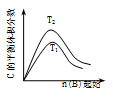 反应Ⅳ:A(g)+B(g)
反应Ⅳ:A(g)+B(g)  2C(g)
2C(g) 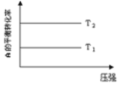
反应Ⅰ:2A(s)+B(g)
 2C(g)
2C(g) 反应Ⅱ:2A(s)
反应Ⅱ:2A(s)  C(g)
C(g)
反应Ⅲ:3A(g)+B(g)
 2C(g)
2C(g) 反应Ⅳ:A(g)+B(g)
反应Ⅳ:A(g)+B(g)  2C(g)
2C(g) 
| A.反应Ⅰ:ΔH>0,P2>P 1 |
| B.反应Ⅱ:ΔH<0,T1<T 2 |
| C.反应Ⅲ:ΔH>0,T 2>T 1;或ΔH<0,T 2<T 1 |
| D.反应Ⅳ:ΔH<0,T 2>T 1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一定温度下,在2L恒容密闭容器中充入8molN2O5,发生反应:2N2O5(g) 4NO2(g)+O2(g) △H>0,测得部分实验数据如表所示:
4NO2(g)+O2(g) △H>0,测得部分实验数据如表所示:
则下列说法错误的是
 4NO2(g)+O2(g) △H>0,测得部分实验数据如表所示:
4NO2(g)+O2(g) △H>0,测得部分实验数据如表所示:| 时间/s | 0 | 500 | 1000 | 1500 |
| n(N2O5)/mol | 8 | 5 | 4 | 4 |
| A.该温度下反应的平衡常数K=64 |
| B.反应达到平衡后,保持其他条件不变,升高体系温度,N2O5的转化率增大 |
| C.反应达到平衡后,保持其他条件不变,增大体系压强,平衡向逆反应方向移动,化学平衡常数不变 |
| D.反应达到平衡后,保持其他条件不变,向平衡体系中再充入适量N2O5气体,平衡向正反应方向移动,化学平衡常数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知反应:
(SCN)2性质与卤素单质相似,能与水或碱反应;CuOH沉淀显橙色; 。
。
进行如下实验:
i.将0.2mol·L-1CuSO4溶液与0.4mol·L-1KSCN溶液等体积混合,充分反应后过滤,测得滤液pH=2;
ⅱ.向滤液中滴加1滴稀NaOH溶液,出现白色沉淀;
ⅲ.继续滴加NaOH溶液,数滴后又出现蓝色沉淀,
下列说法不正确 的是

(SCN)2性质与卤素单质相似,能与水或碱反应;CuOH沉淀显橙色;
 。
。进行如下实验:
i.将0.2mol·L-1CuSO4溶液与0.4mol·L-1KSCN溶液等体积混合,充分反应后过滤,测得滤液pH=2;
ⅱ.向滤液中滴加1滴稀NaOH溶液,出现白色沉淀;
ⅲ.继续滴加NaOH溶液,数滴后又出现蓝色沉淀,
下列说法
| A.i充分反应后可观察到白色沉淀和黄绿色溶液 |
B.ⅱ中未生成蓝色沉淀,说明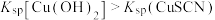 |
| C.ⅲ中出现蓝色沉淀时,该平衡可能发生逆向移动 |
D.无论ⅱ还是ⅲ,随着NaOH溶液的加入,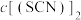 始终降低 始终降低 |
您最近一年使用:0次

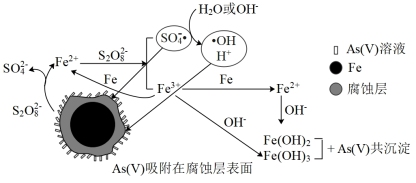
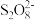 被还原
被还原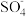 ·+OH-=
·+OH-=  +·OH
+·OH

