在t℃时,某体积可变的密闭容器内,加入适量反应物发生反应:mA(g)+nB(g) pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:
pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:
则下列有关说法中不正确的是()
 pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:
pC(g),已知通过逐渐改变容器的体积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:| 压强 | c(A) | 重新达到平衡所需时间 | |
| 第一次达到平衡 | 2×105Pa | 0.08mol/L | 4min |
| 第二次达到平衡 | 5×105Pa | 0.20mol/L | xmin |
| 第三次达到平衡 | 1×106Pa | 0.44mol/L | 0.8min |
| A.第二次平衡到第三次平衡中,A的平均反应速率为0.3mol/(L·min) |
| B.维持压强为2×105Pa,假设当反应达到平衡状态时体系中共有amol气体,再向体系中加入bmolB,则重新达到平衡时体系中共有(a+b)mol气体 |
C.当压强为1×106Pa时,此反应的平衡常数表达式为K=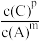 |
| D.m+n=p,x=0 |
19-20高三·浙江·阶段练习 查看更多[4]
(已下线)【浙江新东方】60(已下线)【南昌新东方】9.2020年11月江西南昌三中高三上学期期中化学浙江省杭州第二中学2020-2021学年高三上学期五校联考化学试题(已下线)专题七 化学反应速率与化学平衡 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)
更新时间:2020-12-08 10:29:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】向 刚性密闭容器中充入
刚性密闭容器中充入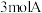 气体,发生反应
气体,发生反应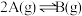 。不同温度下,反应达平衡,平衡体系中各物质的物质的量分数如下表:(已知A有颜色,B无色)
。不同温度下,反应达平衡,平衡体系中各物质的物质的量分数如下表:(已知A有颜色,B无色)
下列说法不正确的是
 刚性密闭容器中充入
刚性密闭容器中充入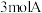 气体,发生反应
气体,发生反应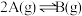 。不同温度下,反应达平衡,平衡体系中各物质的物质的量分数如下表:(已知A有颜色,B无色)
。不同温度下,反应达平衡,平衡体系中各物质的物质的量分数如下表:(已知A有颜色,B无色) ℃ ℃ | 25 | 40 | 50 | 60 |
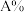 | 20 | 25 | 40 | 66 |
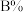 | 80 | 75 | 60 | 34 |
A.25℃,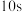 反应达平衡, 反应达平衡, 速率 速率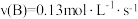 |
| B.室温时,将此容器放入冰水中,颜色变浅 |
| C.向40℃的平衡体系中再充入A,达新平衡时平均分子量减小 |
D.50℃达平衡时,A的转化率为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,在 恒容密闭容器中加入
恒容密闭容器中加入 A和
A和 B进行反应:
B进行反应: ,
, 达到平衡后,测得生成
达到平衡后,测得生成 C,且反应的前后压强之比为
C,且反应的前后压强之比为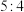 ,则下列说法
,则下列说法不正确 的是
 恒容密闭容器中加入
恒容密闭容器中加入 A和
A和 B进行反应:
B进行反应: ,
, 达到平衡后,测得生成
达到平衡后,测得生成 C,且反应的前后压强之比为
C,且反应的前后压强之比为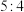 ,则下列说法
,则下列说法A.从开始至平衡时,B的平均速率为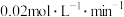 |
B.该反应的化学平衡常数表达式是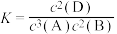 |
C.升高温度,体系压强增大,可知 减小 减小 |
| D.缓慢地再加入B,体系中D的体积分数先增大后减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】NO与CO是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应:
CO(g)+ NO(g)=CO2(g)+ N2(g) ΔH= -374.3 kJ·mol-1 K=2.5×1060, 反应速率较小。有关该反应的说法正确的是
N2(g) ΔH= -374.3 kJ·mol-1 K=2.5×1060, 反应速率较小。有关该反应的说法正确的是
CO(g)+ NO(g)=CO2(g)+
 N2(g) ΔH= -374.3 kJ·mol-1 K=2.5×1060, 反应速率较小。有关该反应的说法正确的是
N2(g) ΔH= -374.3 kJ·mol-1 K=2.5×1060, 反应速率较小。有关该反应的说法正确的是| A.K很大,NO与CO在排入大气之前就已反应完全 |
| B.增大压强,平衡将向右移动,K> 2.5×1060 |
| C.升高温度,既增大反应速率又增大K |
| D.选用适宜催化剂可达到尾气排放标准 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将CuBr2放入密闭的真空容器中,发生反应2CuBr2(s) 2CuBr(s)+Br2(g)达到平衡。保持温度不变,缩小容器体积,体系重新达到平衡,下列说法正确的是
2CuBr(s)+Br2(g)达到平衡。保持温度不变,缩小容器体积,体系重新达到平衡,下列说法正确的是
 2CuBr(s)+Br2(g)达到平衡。保持温度不变,缩小容器体积,体系重新达到平衡,下列说法正确的是
2CuBr(s)+Br2(g)达到平衡。保持温度不变,缩小容器体积,体系重新达到平衡,下列说法正确的是| A.平衡常数减小 | B.n(CuBr)不变 | C.c(Br2)不变 | D.气体密度增加 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
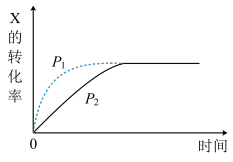
【推荐1】图中曲线分别表示相同温度下,压强为P1、P2条件下发生可逆反应:mX(g)+nY(g) 2Z(g)+W(s)的过程。下列说法不正确的是( )
2Z(g)+W(s)的过程。下列说法不正确的是( )
 2Z(g)+W(s)的过程。下列说法不正确的是( )
2Z(g)+W(s)的过程。下列说法不正确的是( )
| A.P1>P2 | B.m+n=2 |
| C.m+n=3 | D.P1、P2下平衡常数相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用传感技术可探究压强对反应 化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入适量
化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入适量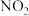 气体,当活塞位置不变时。分别在t1、t2s时快速移动注射器活塞并保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图所示。下列说法中错误的是
气体,当活塞位置不变时。分别在t1、t2s时快速移动注射器活塞并保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图所示。下列说法中错误的是
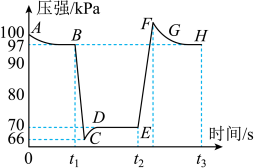
压强随时间变化的曲线
 化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入适量
化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入适量 气体,当活塞位置不变时。分别在t1、t2s时快速移动注射器活塞并保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图所示。下列说法中错误的是
气体,当活塞位置不变时。分别在t1、t2s时快速移动注射器活塞并保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图所示。下列说法中错误的是
压强随时间变化的曲线
| A.由B点到D点观察到注射器内气体颜色先变浅后逐渐变深 |
| B.E点的操作是压缩注射器 |
| C.B、H两点对应的正反应速率相等 |
D.该反应的 ,反应能自发进行的原因是 ,反应能自发进行的原因是 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列事实不能用勒夏特列原理(平衡移动原理)解释的是( )
①溴水中存在化学平衡:Br2+H2O⇌HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
②铁在潮湿的空气中易生锈
③二氧化氮与四氧化二氮的平衡体系,增大压强后颜色加深
④合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)⇌K(g)+NaCl(l)
⑥反应CO(g)+NO2(g)⇌CO2(g)+NO(g)(正反应为放热反应),达到化学平衡后,升高温度体系的颜色加深
①溴水中存在化学平衡:Br2+H2O⇌HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
②铁在潮湿的空气中易生锈
③二氧化氮与四氧化二氮的平衡体系,增大压强后颜色加深
④合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)⇌K(g)+NaCl(l)
⑥反应CO(g)+NO2(g)⇌CO2(g)+NO(g)(正反应为放热反应),达到化学平衡后,升高温度体系的颜色加深
| A.①④ | B.②③ | C.②⑥ | D.②③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度下2L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示.下列说法正确的是( )
| X | Y | W | |
| n(起始状态)/mol | 2 | 1 | 0 |
| n(平衡状态)/mol | 1 | 0.5 | 1.5 |
| A.该温度下,此反应的平衡常数K=6.75 |
| B.若升高温度,W的体积分数减小,则此反应△H>0 |
| C.增大压强,正、逆反应速率均增大,平衡向正反应方向移动 |
D.该温度下,此反应的平衡常数表达式是 K=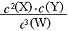 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】甲烷水蒸气催化重整是制备高纯氢的方法之一,反应为CH4(g)+H2O(g) CO(g)+3H2(g)。在不同温度下,向a、b两个恒温恒容的密闭容器中均通入1.1mol CH4(g)和1.1mol H2O(g),测得容器a中CO物质的量、容器b中H2物质的量随时间的变化曲线如图所示(已知容器a、b的体积为2L)。下列说法正确的是
CO(g)+3H2(g)。在不同温度下,向a、b两个恒温恒容的密闭容器中均通入1.1mol CH4(g)和1.1mol H2O(g),测得容器a中CO物质的量、容器b中H2物质的量随时间的变化曲线如图所示(已知容器a、b的体积为2L)。下列说法正确的是

 CO(g)+3H2(g)。在不同温度下,向a、b两个恒温恒容的密闭容器中均通入1.1mol CH4(g)和1.1mol H2O(g),测得容器a中CO物质的量、容器b中H2物质的量随时间的变化曲线如图所示(已知容器a、b的体积为2L)。下列说法正确的是
CO(g)+3H2(g)。在不同温度下,向a、b两个恒温恒容的密闭容器中均通入1.1mol CH4(g)和1.1mol H2O(g),测得容器a中CO物质的量、容器b中H2物质的量随时间的变化曲线如图所示(已知容器a、b的体积为2L)。下列说法正确的是
| A.该反应为放热反应 |
| B.两容器达到平衡时,b容器中CO的体积分数大于a容器 |
| C.a容器前4min用CH4表示的平均反应速率为0.25mol/(L∙min) |
| D.a容器达到平衡后,再充入1.1mol CH4(g)和1molCO(g),此时v正>v逆 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】向容积固定为2L的密闭容器中充入9.6molNO和4.8moLO2,发生反应:
①2NO(g)+O2(g) 2NO2(g) ΔH<0,
2NO2(g) ΔH<0,
②2NO2(g) N2O4(g) ΔH<0。
N2O4(g) ΔH<0。
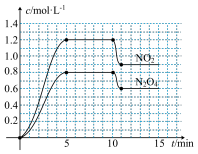
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T℃,10min时改变某一个反应条件,一段时间后再次平衡。下列说法正确的是( )
①2NO(g)+O2(g)
 2NO2(g) ΔH<0,
2NO2(g) ΔH<0,②2NO2(g)
 N2O4(g) ΔH<0。
N2O4(g) ΔH<0。测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T℃,10min时改变某一个反应条件,一段时间后再次平衡。下列说法正确的是( )

| A.前5min反应的平均速率v(O2)=0.28mol·L-1·min-1 |
| B.第一次平衡时NO的转化率约为25% |
| C.反应①的化学平衡常数:K(5-10min)=K(11-15min) |
| D.若起始时向该容器中充入3.6molNO2和3.0molN2O4,T℃达到平衡时,NO2的物质的量浓度大于图中5~10min的NO2的物质的量浓度 |
您最近一年使用:0次

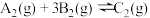 的化学反应速率,甲测得
的化学反应速率,甲测得 的物质的量浓度减小了0.5mol/L,乙测得
的物质的量浓度减小了0.5mol/L,乙测得 的物质的量浓度减小了1.5mol/L,则这两个学生测定的反应速率较大的是
的物质的量浓度减小了1.5mol/L,则这两个学生测定的反应速率较大的是

