回答下列有关问题
(1)KW的数学表达式是KW =__________ ,温度升高KW的变化情况是______ (选填“变大”“变小”或“不变”)。
(2)K通常表示化学平衡常数,K值越大表示该反应进行程度越________ ,对于反应2NO2(g)  N2O4(g),其化学平衡常数K的数学表达式为K=[N2O4]/[NO2]2,式中[NO2]2表示的意义是
N2O4(g),其化学平衡常数K的数学表达式为K=[N2O4]/[NO2]2,式中[NO2]2表示的意义是_______________ 。
(3)Kα通常表示弱酸的电离平衡常数,Kα值越大表示该弱酸的酸性_______ ,对于某一元弱酸,当用蒸馏水稀释该酸时,溶液越稀,Kα的变化情况是________ (选填“变大”“变小”或“不变”)
(4)Ksp表示难溶物的溶度积常数,该常数越大表示难溶物在水中的__________ 。
(5)实验室可用NaOH溶液吸收NO2 ,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1mol/L的CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-) 和c(CH3COO-) 由大到小的顺序为_____________ 。(已知HNO2的电离常数Ka=7.1×10−4 mol/L,CH3COOH的电离常数为:Ka=1.7×10−5 mol/L),可使溶液A和溶液B的pH相等的方法是_____________ 。
A.向溶液A中加适量水 B.向溶液A中加适量NaOH
C.向溶液B中加适量水 D.向溶液B中加适量NaOH.
(1)KW的数学表达式是KW =
(2)K通常表示化学平衡常数,K值越大表示该反应进行程度越
 N2O4(g),其化学平衡常数K的数学表达式为K=[N2O4]/[NO2]2,式中[NO2]2表示的意义是
N2O4(g),其化学平衡常数K的数学表达式为K=[N2O4]/[NO2]2,式中[NO2]2表示的意义是(3)Kα通常表示弱酸的电离平衡常数,Kα值越大表示该弱酸的酸性
(4)Ksp表示难溶物的溶度积常数,该常数越大表示难溶物在水中的
(5)实验室可用NaOH溶液吸收NO2 ,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1mol/L的CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-) 和c(CH3COO-) 由大到小的顺序为
A.向溶液A中加适量水 B.向溶液A中加适量NaOH
C.向溶液B中加适量水 D.向溶液B中加适量NaOH.
更新时间:2019-02-02 10:34:45
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】烟气(主要污染物SO2、NO、NO2)的大量排放造成严重的大气污染,国内较新研究成果是采用以尿素为还原剂的脱硫脱硝一体化技术。
(1)脱硫总反应:SO2(g)+CO(NH2)2(aq)+2H2O(l)+1/2O2(g)=(NH2)SO4(aq)+CO2(g),已知该反应能自发进行,则条件是____ (填“高温”、“低温”或“任何温度”)。
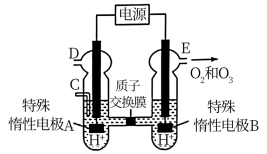
(2)电解稀硫酸制备O3(原理如图),则产生O3的电极反应式为______ 。

(3)室温下,往恒容的反应器中加入固定物质的量的SO2和NO,通入O3充分混合。反应相同时间后,各组分的物质的量随n(O3)∶n(NO)的变化见上图。
① n(NO2)随n(O3)∶n(NO)的变化先增加后减少,原因是____ 。
② 臭氧量对反应SO2(g)+O3(g)=SO3(g)+O2(g)的影响不大,试用过渡态理论解释可能原因__ 。
(4)通过控制变量法研究脱除效率的影响因素得到数据如下图所示,下列说法正确的是____ 。
A. 烟气在尿素溶液中的反应:v(脱硫)<v(脱硝)
B. 尿素溶液pH的变化对脱硝效率的影响大于对脱硫效率的影响
C. 强酸性条件下不利于尿素对氮氧化物的脱除
D. pH=7的尿素溶液脱硫效果最佳

(5)尿素的制备:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ΔH<0。一定条件下,往10 L恒容密闭容器中充入2 mol NH3和1 mol CO2。
CO(NH2)2(s)+H2O(g) ΔH<0。一定条件下,往10 L恒容密闭容器中充入2 mol NH3和1 mol CO2。
① 该反应10 min 后达到平衡,测得容器中气体密度为4.8 g·L-1,平衡常数K=__ 。
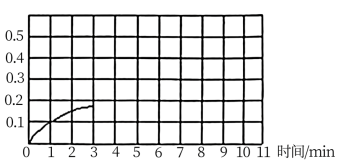
② 上图是该条件下,系统中尿素的物质的量随反应时间的变化趋势,当反应时间达到3min 时,迅速将体系升温,请在图中画出3~10 min 内容器中尿素的物质的量的变化趋势曲线__________ 。
(1)脱硫总反应:SO2(g)+CO(NH2)2(aq)+2H2O(l)+1/2O2(g)=(NH2)SO4(aq)+CO2(g),已知该反应能自发进行,则条件是
(2)电解稀硫酸制备O3(原理如图),则产生O3的电极反应式为


(3)室温下,往恒容的反应器中加入固定物质的量的SO2和NO,通入O3充分混合。反应相同时间后,各组分的物质的量随n(O3)∶n(NO)的变化见上图。
① n(NO2)随n(O3)∶n(NO)的变化先增加后减少,原因是
② 臭氧量对反应SO2(g)+O3(g)=SO3(g)+O2(g)的影响不大,试用过渡态理论解释可能原因
(4)通过控制变量法研究脱除效率的影响因素得到数据如下图所示,下列说法正确的是
A. 烟气在尿素溶液中的反应:v(脱硫)<v(脱硝)
B. 尿素溶液pH的变化对脱硝效率的影响大于对脱硫效率的影响
C. 强酸性条件下不利于尿素对氮氧化物的脱除
D. pH=7的尿素溶液脱硫效果最佳

(5)尿素的制备:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ΔH<0。一定条件下,往10 L恒容密闭容器中充入2 mol NH3和1 mol CO2。
CO(NH2)2(s)+H2O(g) ΔH<0。一定条件下,往10 L恒容密闭容器中充入2 mol NH3和1 mol CO2。① 该反应10 min 后达到平衡,测得容器中气体密度为4.8 g·L-1,平衡常数K=

② 上图是该条件下,系统中尿素的物质的量随反应时间的变化趋势,当反应时间达到3min 时,迅速将体系升温,请在图中画出3~10 min 内容器中尿素的物质的量的变化趋势曲线
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】汽车尾气主要含有CO2、CO、SO2、NO及汽油、柴油等物质,这种尾气越来越成为城市空气污染的主要来源,必须予以治理。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使汽油、柴油等物质充分燃烧及SO2的转化。
(1)汽车尾气中NO的来源是_________ 。
A.汽油、柴油中含氮,是其燃烧产物
B.是空气中的N2与汽油、柴油的反应产物
C.是空气中的N2与O2在汽车气缸内的高温环境下的反应产物
D.是汽车高温尾气导致了空气中N2与O2的化合反应
(2)写出CO与NO反应的化学方程式:_____________________________ 。
(3)“催化转化器”的缺点是在一定程度上提高了空气的酸度,其原因是______________
(4)控制或者减少城市汽车尾气污染的方法可以有___________ 。(多选)
A.开发氢能源 B.使用电动车 C.限制车辆行驶 D.使用乙醇汽油
(1)汽车尾气中NO的来源是
A.汽油、柴油中含氮,是其燃烧产物
B.是空气中的N2与汽油、柴油的反应产物
C.是空气中的N2与O2在汽车气缸内的高温环境下的反应产物
D.是汽车高温尾气导致了空气中N2与O2的化合反应
(2)写出CO与NO反应的化学方程式:
(3)“催化转化器”的缺点是在一定程度上提高了空气的酸度,其原因是
(4)控制或者减少城市汽车尾气污染的方法可以有
A.开发氢能源 B.使用电动车 C.限制车辆行驶 D.使用乙醇汽油
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是常温下,浓度为0.01mol/L的NaOH溶液与几种酸或盐混合后的情况:
回答下列问题:
(1)①组混合液中,HA、A-、Na+三种粒子浓度由大到小的顺序为________ ,若pH=8,则c(Na+)-c(A-)=________ mol/L(填具体数字)。
(2)由②组混合液pH=7可推知,V1____ V2。
(3)③组混合液中,pH>7的原因是______________________ 。
(4)0.01mol/LNaHD溶液中,水的电离度=_________ 。(已知:水的电离度=[已电离的水分子的个数/水分子总数]×100%)
(5)仅凭上述结果,一定能确定HA、HB、H2C、H2D四种酸中属于弱酸的是_________ 。
| 混合组别 | 混合前酸或盐的总浓度 | 混合比例及混合溶液性质 |
| ① | c(HA)=0.02mol/L | 等体积混合,pH>7 |
| ② | HB溶液的pH=2 | V1 mLNaOH溶液与V2mLHB溶液,pH=7 |
| ③ | c(H2C)=0.01mol/L | 等体积混合,pH>7 |
| ④ | c(NaHD)=0.01mol/L | 等体积混合,pH=7 |
(1)①组混合液中,HA、A-、Na+三种粒子浓度由大到小的顺序为
(2)由②组混合液pH=7可推知,V1
(3)③组混合液中,pH>7的原因是
(4)0.01mol/LNaHD溶液中,水的电离度=
(5)仅凭上述结果,一定能确定HA、HB、H2C、H2D四种酸中属于弱酸的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)已知NaHA水溶液呈碱性。
①用离子方程式表示NaHA水溶液呈碱性的原因:______________________________ 。
②在NaHA水溶液中各离子浓度的大小关系是:______________________________ 。
(2)25℃,两种酸的电离平衡常数如表.
①HSO3﹣的电离平衡常数表达式K=______ 。
②H 2SO3溶液和NaHCO3溶液反应的主要离子方程式为______ 。
①用离子方程式表示NaHA水溶液呈碱性的原因:
②在NaHA水溶液中各离子浓度的大小关系是:
(2)25℃,两种酸的电离平衡常数如表.
Ka1 | Ka2 | |
H2SO3 | 1.3×10﹣2 | 6.3×10﹣8 |
H2CO3 | 4.2×10﹣7 | 5.6×10﹣11 |
①HSO3﹣的电离平衡常数表达式K=
②H 2SO3溶液和NaHCO3溶液反应的主要离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知常温下部分弱电解质的电离常数如下表:
(1)常温下,pH相同的三种溶液:①NaF溶液;②NaClO溶液;③Na2CO3溶液,其物质的量浓度由大到小的顺序是 _______
(2)向NaClO 溶液中通入少量CO2,所发生反应的离子方程式为_______
(3)常温下,0.1mol·L-1HF与0.1mol·L-1NaF溶液等体积混合,判断混合溶液的酸碱性:_______
(4)常温下,将pH=5的盐酸与pH=9的NaOH溶液以体积比11:9混合后的pH为_______
(5)25℃时,碳酸氢钠溶液的水解平衡常数为_______
(6)泡沫灭火器反应原理的离子方程式_______
(7)工业制备TiO2·xH2O的化学方程式_______
| 化学式 | HF | HClO | H2CO3 | NH3·H2O |
| 电离常数 | Ka=6.8×10-4 | Ka=4.7×10-8 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Kb=1.7×10-5 |
(2)向NaClO 溶液中通入少量CO2,所发生反应的离子方程式为
(3)常温下,0.1mol·L-1HF与0.1mol·L-1NaF溶液等体积混合,判断混合溶液的酸碱性:
(4)常温下,将pH=5的盐酸与pH=9的NaOH溶液以体积比11:9混合后的pH为
(5)25℃时,碳酸氢钠溶液的水解平衡常数为
(6)泡沫灭火器反应原理的离子方程式
(7)工业制备TiO2·xH2O的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】草酸( ,二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用,常温下,
,二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用,常温下,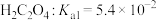 ,
,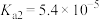 ;
;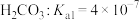 ,
,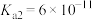 。
。
(1)写出草酸在水中的电离方程式_____ 。
(2)在 溶液稀释过程中,下列物理量始终增大的是_____。
溶液稀释过程中,下列物理量始终增大的是_____。
(3)常温下,0.18mol/L 溶液中第二步电离出来的
溶液中第二步电离出来的 ,则0.18mol/L
,则0.18mol/L 溶液中
溶液中 电离出来的
电离出来的
_____ amol/L(填“>”“<”或“=”)。
(4)常温下,向20mL0.1
 溶液中缓慢滴加pH=13的NaOH溶液,混合溶液的温度与滴加NaOH溶液体积的关系如图所示:
溶液中缓慢滴加pH=13的NaOH溶液,混合溶液的温度与滴加NaOH溶液体积的关系如图所示:
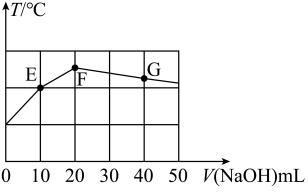
试分析图中E、F、G三点,水的电离程度最大的是点_____ 。
 ,二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用,常温下,
,二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用,常温下,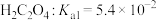 ,
,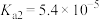 ;
;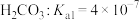 ,
,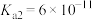 。
。(1)写出草酸在水中的电离方程式
(2)在
 溶液稀释过程中,下列物理量始终增大的是_____。
溶液稀释过程中,下列物理量始终增大的是_____。A. | B.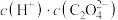 | C.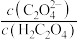 | D.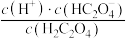 |
(3)常温下,0.18mol/L
 溶液中第二步电离出来的
溶液中第二步电离出来的 ,则0.18mol/L
,则0.18mol/L 溶液中
溶液中 电离出来的
电离出来的
(4)常温下,向20mL0.1

 溶液中缓慢滴加pH=13的NaOH溶液,混合溶液的温度与滴加NaOH溶液体积的关系如图所示:
溶液中缓慢滴加pH=13的NaOH溶液,混合溶液的温度与滴加NaOH溶液体积的关系如图所示:
试分析图中E、F、G三点,水的电离程度最大的是点
您最近一年使用:0次



