下列符号代表的粒子不影响水的电离平衡的是
A.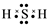 | B.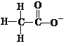 | C.Fe3+ | D.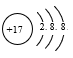 |
18-19高二上·湖北·期末 查看更多[4]
天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高二上学期第二次阶段检测(期中)化学试题(已下线)第三单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)辽宁省大连市2019-2020学年高二上学期期末考试化学试题【全国百强校】湖北省沙市中学2018-2019学年高二上学期期末考试化学试题
更新时间:2019-02-06 09:03:28
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】氢气和二氧化碳在催化剂作用下,在180-280℃温度下合成甲醇,该反应放热。催化过程可解释为“吸附-活化-解离”,催化反应机理如图所示。下列说法正确的是
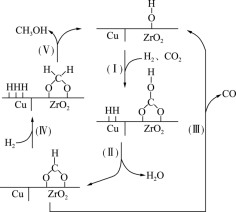
| A.反应过程中I-V步,C化合价不变 |
| B.单位时间内,生成水越多,甲醇产率越大 |
| C.增大催化剂的表面积,可以提高甲醇的平衡产率 |
| D.因为电负性O>C,所以CO2中的C与吸附在氧化锆晶格表面的OH上的O原子结合 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】关于下列各图的叙述错误的是


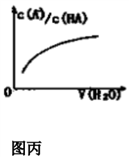



| A.已知1molCO燃烧放出的热为283kJ,2H2(g)+O2(g)=2H2O(g);ΔH= - 483.6kJ/mol则图甲表示CO和H2O(g)生成CO2和H2的能量变化 |
| B.常温下0.2 mol·L-1 HA溶液和0.1mol·L-1NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(A-)> c(Na+)>c(H+)>c(OH-) |
| C.常温下,X2(g)和H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐减小,且HX的还原性逐渐减弱 |
D.图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,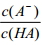 的变化情况 的变化情况 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】室温时,下列溶液中有关物质的量浓度关系正确的是
A.CH3COONa溶液的pH=8,则 |
| B.0.1 mol/LNa2CO3溶液中水电离出来的c(OH-)小于0.1 mol/LNaOH溶液中水电离出来的c(OH-) |
| C.0.1 mol/L NaHA溶液的pH=4,则有c(HA-)>c(H+)>c(H2A)>c(A2-) |
| D.纯水加热到100℃时,水的离子积变大、pH变小、呈中性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.分子晶体中,共价键键能越大,分子的熔、沸点越高 |
| B.pH=4的CH3COOH和NH4Cl溶液中,水的电离程度相同 |
| C.用pH试纸测定溶液pH的正确操作是,将一小条试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照 |
| D.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列有关电解质溶液的说法正确的是
A.向0.1mol•L-1CH3COOH溶液中加入少量水, 溶液减小 溶液减小 |
B.将CH3COONa溶液从20℃升温至30℃, 溶液中增大 溶液中增大 |
C.1mL0.5mol/LNH4Cl溶液与2mL0.25mol/LNH4Cl溶液含n(NH ),前者大于后者 ),前者大于后者 |
| D.将AlCl3溶液和Al2(SO4)3溶液分别蒸干后再灼烧,所得固体产物均为Al2O3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】短周期元素A、B、D、E的原子序数依次增大,B、E位于同主族,四种元素组成的一种化合物M的结构式为 。下列说法不正确的是
。下列说法不正确的是
 。下列说法不正确的是
。下列说法不正确的是| A.E的最简单氢化物的还原性比B的弱 | B.D与E形成的二元化合物的水溶液显碱性 |
| C.B与E形成的化合物不都是极性分子 | D.A与D形成的二元化合物中含有离子键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】Na2CrO4水溶液存在如下平衡:2H++2 (黄色)⇌2
(黄色)⇌2 ⇌
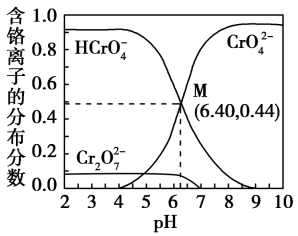
⇌ (橙色)+H2O,在1.00mol/L的铬酸钠(Na2CrO4)溶液中,各种含铬离子的分布分数与pH关系如图所示。下列说法错误的是
(橙色)+H2O,在1.00mol/L的铬酸钠(Na2CrO4)溶液中,各种含铬离子的分布分数与pH关系如图所示。下列说法错误的是
 (黄色)⇌2
(黄色)⇌2 ⇌
⇌ (橙色)+H2O,在1.00mol/L的铬酸钠(Na2CrO4)溶液中,各种含铬离子的分布分数与pH关系如图所示。下列说法错误的是
(橙色)+H2O,在1.00mol/L的铬酸钠(Na2CrO4)溶液中,各种含铬离子的分布分数与pH关系如图所示。下列说法错误的是
| A.Na2CrO4溶液中滴加硫酸,由黄色变为橙色 |
| B.铬酸(H2CrO4)的第二步电离常数Ka2=10-6.4 |
| C.要得到纯度较高的Na2CrO4溶液,应控制pH>9 |
D.pH=6时,Na2CrO4溶液中存在:c(Na+)=2c( )+2c( )+2c( )+2c( )+2c( ) ) |
您最近半年使用:0次

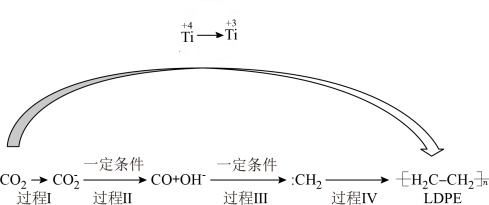
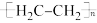 +4nH2O
+4nH2O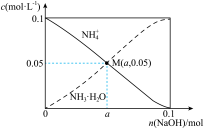
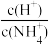 不断增大
不断增大

