已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.2mol·L-1HF溶液中加入1 L 0.2 mol·L-1CaCl2溶液,则下列说法中,正确的是 ( )
| A.25℃时,0.1 mol·L-1HF溶液中pH=1 |
| B.该体系中有CaF2沉淀产生 |
| C.Ksp(CaF2)随温度和浓度的变化而变化 |
| D.加入CaCl2溶液后体系中的c(H+)浓度不变 |
13-14高二下·内蒙古包头·期末 查看更多[4]
(已下线)2013-2014学年内蒙古包头一中高二下学期期末考试化学试卷2015-2016学年福建省漳州一中高二上学期期末化学试卷【全国百强校】河南省许昌市许昌高级中学2019届高三上学期第一次诊断考试化学试题天津市耀华中学2020-2021学年高二上学期第二次段考化学试题
更新时间:2019-03-01 14:17:19
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下某柠檬水溶液的pH是4,其中的 是
是
 是
是A.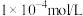 | B. | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知含硫元素的几种物质间具有如图转化关系。 表示阿伏加德罗常数值,下列说法正确的是
表示阿伏加德罗常数值,下列说法正确的是
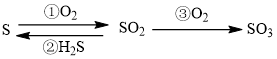
 表示阿伏加德罗常数值,下列说法正确的是
表示阿伏加德罗常数值,下列说法正确的是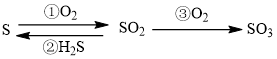
A.反应①中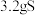 充分燃烧后生成 充分燃烧后生成 |
B.反应②中若转移 个电子,生成 个电子,生成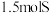 |
C. 个 个 分子与足量氧气经反应③可以制得 分子与足量氧气经反应③可以制得 个 个 分子 分子 |
D. 的二氧化硫水溶液中 的二氧化硫水溶液中 的物质的量为 的物质的量为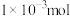 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,71gCl2通入1L水中,转移电子数为NA |
| B.1mo/L的NH4Cl溶液中,Cl-的数目为NA |
| C.标准状况下,5.6LCO2和O2混合气体中含有的氧原子数为0.5NA |
| D.1LpH=2的CH3COOH溶液中含有的H+数小于0.01NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.硬脂酸甘油酯在NaOH溶液中水解完全后,加入饱和食盐水,下层析出硬脂酸钠 |
B.乙酸的分子模型可表示为 |
| C.向浓度均为0.05mol·L−1的Na2CrO4、NaCl混合溶液中滴加少量AgNO3溶液时,先产生砖红色Ag2CrO4沉淀。(已知Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.12×10-12) |
| D.质量均为7.8gNa2S、Na2O2的固体中含有的阴离子数均为0.2NA |
您最近一年使用:0次
【推荐2】在t℃时,AgI在水中的沉淀溶解平衡曲线如图所示,又知t℃时AgBr的Ksp=5×10−13.下列说法不正确的是
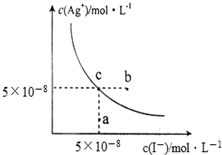

| A.在t℃时,AgI的Ksp=2.5×10−15 |
| B.图中b点有碘化银晶体析出 |
| C.向c点溶液中加入适量蒸馏水,可使溶液由c点到a点 |
| D.在t℃时,反应AgBr(s)+I−(aq)⇌AgI(s)+Br−(aq) 的平衡常数K=200 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知25℃物质的溶度积常数为:FeS:Ksp=6.3×10﹣18;CuS:Ksp=1.3×10﹣36;ZnS:Ksp=1.6×10﹣24。下列说法正确的是
| A.相同温度下,CuS的溶解度大于ZnS的溶解度 |
| B.除去工业废水中的Cu2+,可以选用FeS做沉淀剂 |
| C.足量CuSO4溶解在0.1mol/L的H2S溶液中,Cu2+能达到的最大浓度为1.3×10﹣35mol/L |
| D.在ZnS的饱和溶液中,加入FeCl2溶液,一定不产生FeS沉淀 |
您最近一年使用:0次
【推荐2】某工业废水中含有 等离子,现要用沉淀法除去
等离子,现要用沉淀法除去 ,并回收
,并回收 元素,上述金属阳离子在水中达到沉淀溶解平衡时的
元素,上述金属阳离子在水中达到沉淀溶解平衡时的 关系如图所示。下列说法不正确的是
关系如图所示。下列说法不正确的是
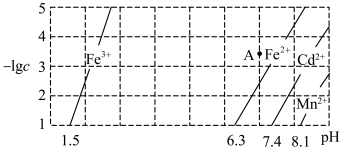
 等离子,现要用沉淀法除去
等离子,现要用沉淀法除去 ,并回收
,并回收 元素,上述金属阳离子在水中达到沉淀溶解平衡时的
元素,上述金属阳离子在水中达到沉淀溶解平衡时的 关系如图所示。下列说法不正确的是
关系如图所示。下列说法不正确的是
A.A点时 未沉淀 未沉淀 | B.分离 元素前需要加入氧化剂 元素前需要加入氧化剂 |
C.当 时, 时, | D. 沉淀完全时 沉淀完全时 也沉淀完全 也沉淀完全 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验目的对应的实验方案、现象和结论都正确的是
| 选项 | 实验目的 | 实验方案 | 现象和结论 |
| A | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入2~3mL蒸馏水 | 有气体生成,固体粉末为Na2O2 |
| B | 比较AgCl和AgI的Ksp相对大小 | 向等体积饱和AgCl溶液和饱和AgI溶液中分别滴加等量的浓AgNO3溶液(过量) | 得到沉淀n(AgCl)>n(AgI),则Ksp(AgCl)>Ksp(AgI) |
| C | 比较Cl2、Br2、I2的氧化性强弱 | 向KBr、KI混合溶液中依次加入少量新制氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色,证明氧化性:Cl2>Br2>I2 |
| D | 比较H2CO3与CH3COOH的酸性强弱 | 用pH计测定溶液pH:①NaHCO3溶液②CH3COONa溶液 | pH:①>②,证明H2CO3的酸性弱于CH3COOH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】根据下列图示所得出的结论不正确的是
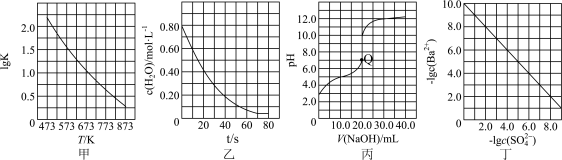

A.图甲是 的平衡常数与反应温度的关系曲线,说明该反应的 的平衡常数与反应温度的关系曲线,说明该反应的 |
B.图乙是室温下 催化分解放出氧气的反应中 催化分解放出氧气的反应中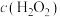 随反应时间变化的曲线,说明随着反应的进行 随反应时间变化的曲线,说明随着反应的进行 分解速率逐渐减小 分解速率逐渐减小 |
C.图丙是室温下用 溶液滴定 溶液滴定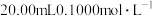 某一元酸HX的滴定曲线,说明HX是一元弱酸,Q点(pH=7): 某一元酸HX的滴定曲线,说明HX是一元弱酸,Q点(pH=7):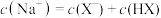 |
D.图丁是室温下用 除去溶液中 除去溶液中 达到沉淀溶解平衡时,溶液中 达到沉淀溶解平衡时,溶液中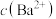 与 与 的关系曲线,说明室温下 的关系曲线,说明室温下 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某元素M的氢氧化物 在水中的溶解反应为:
在水中的溶解反应为:
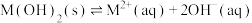

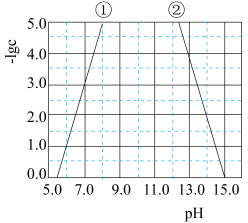
25℃,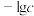 与pH的关系如图所示,c为
与pH的关系如图所示,c为 或
或 物质的量浓度的值。下列说法正确的是
物质的量浓度的值。下列说法正确的是
 在水中的溶解反应为:
在水中的溶解反应为: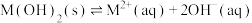


25℃,
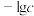 与pH的关系如图所示,c为
与pH的关系如图所示,c为 或
或 物质的量浓度的值。下列说法正确的是
物质的量浓度的值。下列说法正确的是A.曲线①代表 与pH的关系 与pH的关系 |
B. 的 的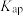 约为 约为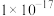 |
C.当溶液的pH达到15.0以上时, 才开始溶解 才开始溶解 |
D.向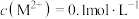 的溶液中加入NaOH溶液至 的溶液中加入NaOH溶液至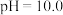 ,体系中元素M主要以 ,体系中元素M主要以 存在 存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知室温下溶度积常数:Ksp[Pb(OH)2]=2×10-15,Ksp[Fe(OH)2]=8×10-15。当溶液中金属离子浓度小于10-5mol•L-1视为沉淀完全。向20mL含0.10mol•L-1Pb2+和0.10mol•L-1Fe2+的混合溶液中滴加0.10mol•L-1NaOH溶液,金属阳离子浓度与滴入NaOH溶液体积的关系曲线如图所示,则下列说法正确的是( )


| A.曲线A表示c(Pb2+)的曲线 |
| B.当溶液pH=8时,Fe2+开始沉淀,Pb2+沉淀完全 |
| C.滴入NaOH溶液体积大于30mL时,溶液中c(Fe2+)=4c(Pb2+) |
D.室温下,滴加NaOH溶液过程中,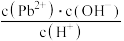 比值不断增大 比值不断增大 |
您最近一年使用:0次



