下列关于难溶电解质溶解平衡的说法正确的是
| A.可直接根据Ksp的数值大小比较难溶电解质在水中的溶解度大小 |
| B.在AgCl的饱和溶液中,加入蒸馏水,Ksp(AgCl)不变 |
| C.难溶电解质的溶解平衡过程是可逆的,且在平衡状态时,v溶解=v沉淀=0 |
| D.25℃时,Ksp(AgCl)>Ksp(AgI),向 AgCl 的饱和溶液中加入少量KI固体,一定有黄色沉淀 |
更新时间:2019-03-20 16:36:17
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知 时,
时,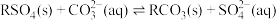 的平衡常数
的平衡常数 ,
,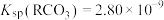 ,下列叙述中正确的是
,下列叙述中正确的是
 时,
时,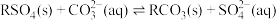 的平衡常数
的平衡常数 ,
,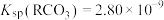 ,下列叙述中正确的是
,下列叙述中正确的是A. 时, 时, 的 的 的为 的为 |
B.将浓度均为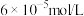 的 的 、 、 溶液等体积混合后可得到 溶液等体积混合后可得到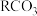 沉淀 沉淀 |
C.向 的混合液中滴加 的混合液中滴加 溶液,首先析出 溶液,首先析出 沉淀 沉淀 |
D.相同温度下,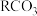 在水中的 在水中的 大于在 大于在 溶液中的 溶液中的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知CaCO3的Ksp=2.8×10-9,现将浓度为2×10-4mol·L-1的Na2CO3溶液与CaCl2溶液等体积混合,下列说法正确的是
| A.CaCO3难溶于稀硫酸,却能溶于醋酸,说明醋酸酸性比硫酸强 |
| B.CaCO3与水形成饱和溶液,再加CaCO3固体,平衡向溶解方向移动,Ksp将增大 |
| C.若要产生沉淀,则所用CaCl2溶液的浓度至少应为1.4×10-5mol·L-1 |
| D.若要产生沉淀,则所用CaCl2溶液的浓度至少应为5.6×10-5mol·L-1 |
您最近一年使用:0次
【推荐1】下列实验操作能达到实验目的的是
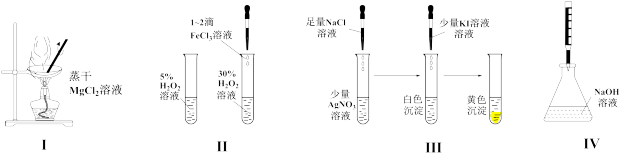

| A.装置I:从MgCl2溶液中提取MgCl2·6H2O固体 |
| B.装置II:探究催化剂对化学反应速率的影响 |
| C.装置III:验证AgCl和AgI的Ksp大小 |
| D.装置IV:用标准盐酸溶液滴定NaOH溶液的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.向AgI沉淀中加入饱和KCl溶液,有白色沉淀生成,说明AgCl比AgI更难溶 |
B.向浓度均为 的 的 和 和 混合溶液中逐滴加入氨水,若先生成蓝色 混合溶液中逐滴加入氨水,若先生成蓝色 沉淀,则 沉淀,则 |
C.向 饱和溶液中加入饱和 饱和溶液中加入饱和 溶液,有白色沉淀产生,说明 溶液,有白色沉淀产生,说明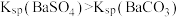 |
D.向1mL 的NaOH溶液中滴入1mL 的NaOH溶液中滴入1mL 的 的 溶液,产生白色沉淀后,再滴加2滴 溶液,产生白色沉淀后,再滴加2滴 的 的 溶液,又生成红褐色沉淀,说明在相同温度下的溶解度: 溶液,又生成红褐色沉淀,说明在相同温度下的溶解度: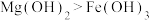 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3。某化学兴趣小组用某浓度的Na2CO3溶液处理一定量的CaSO4固体,测得所加Na2CO3溶液体积与溶液中-lgc(CO32-)的关系如下。
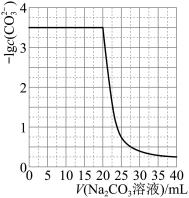
已知Ksp(CaSO4)=9×10-6,Ksp(CaCO3)=3×10-9,lg3=0.5,下列说法不正确的是( )

已知Ksp(CaSO4)=9×10-6,Ksp(CaCO3)=3×10-9,lg3=0.5,下列说法不正确的是( )
| A.曲线上各点的溶液满足关系式:c(Ca2+)·c(SO42-)=Ksp(CaSO4) |
B.CaSO4(s)+CO32-(aq) CaCO3(s)+SO42-(aq) K=3×103 CaCO3(s)+SO42-(aq) K=3×103 |
| C.该Na2CO3溶液的浓度为1mol/L |
| D.相同实验条件下,若将Na2CO3溶液的浓度改为原浓度的2倍,则上图曲线整体向上平移1个单位即可 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定温度下,AgCl(s) Ag+(aq)+Cl-(aq)体系中,
Ag+(aq)+Cl-(aq)体系中, 和
和 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 Ag+(aq)+Cl-(aq)体系中,
Ag+(aq)+Cl-(aq)体系中, 和
和 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
| A.a、b、c三点溶解度相同 |
| B.d点的溶液为AgCl的不饱和溶液 |
| C.向该平衡体系中加入NaCl固体,AgCl的溶解度不变 |
D.a、b、c三点对应的 相等 相等 |
您最近一年使用:0次
【推荐2】某小组为了探究 的性质,设计了实验[已知:
的性质,设计了实验[已知: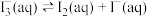 ]:
]:
下列推断正确的是
 的性质,设计了实验[已知:
的性质,设计了实验[已知: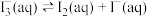 ]:
]:| 操作 | 试剂X( ) ) | 现象 |
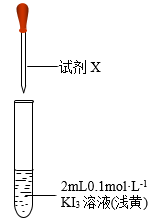 | Ⅰ. 溶液和淀粉溶液 溶液和淀粉溶液 | 溶液变为蓝色 |
Ⅱ. 溶液 溶液 | 产生黄色沉淀 | |
Ⅲ.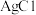 浊液 浊液 | 产生黄色沉淀 | |
Ⅳ. 溶液 溶液 | 溶液变为无色 |
A.由实验Ⅰ知,还原性: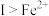 |
B.由实验Ⅱ知:加入 溶液时,发生了氧化还原反应 溶液时,发生了氧化还原反应 |
C.由实验Ⅲ知: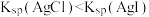 |
D.由实验Ⅳ知: 具有氧化性 具有氧化性 |
您最近一年使用:0次

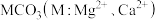 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。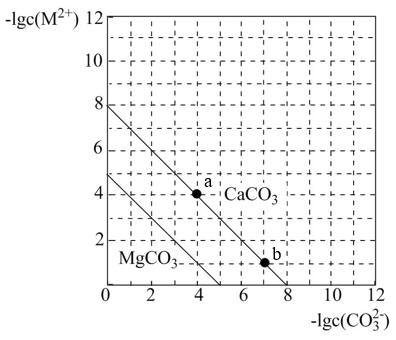
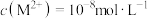 时,
时,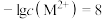 ;
;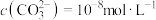 时。
时。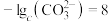
 的
的

 固体
固体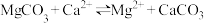 ,正向转化比逆向转化更难实现
,正向转化比逆向转化更难实现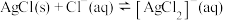
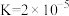 ,
, 的
的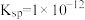 。下列说法不正确的是
。下列说法不正确的是 NaCl溶液中AgCl溶解的质量约为
NaCl溶液中AgCl溶解的质量约为