题型:解答题-结构与性质
难度:0.65
引用次数:233
题号:7851841
铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。请回答下列问题:
(1)铁元素基态原子的电子排布式为_________ ,3d能级上的未成对电子数为_________ ,能量最高能级的电子云形状为_________ 。
(2)Fe3+可用KSCN溶液检验,形成的配合物颜色为_________ ,写出一个与SCN-具有相同空间构型的分子:_________ 。
(3)氮元素的最简单氢化物为氨,氨的沸点_________ (填“高于”或“低于”)膦(PH3),原因是_________ 。氮元素另一种氢化物联氨(N2H4)是_________ (填“极性”或“非极性”)分子,其中心原子的轨道杂化类型为_________ 。
(4)铁的第三电离能(I3),第四电离能(I4)分别为2957kJ/mol,5290kJ/mol,I4远大于I3的原因是_________ 。
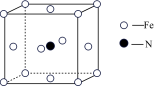
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:_________ 。若两个最近的Fe原子间的距离为a cm,则该晶体的密度是_________ g/cm3(设阿伏伽德罗常数的值为NA)。
(1)铁元素基态原子的电子排布式为
(2)Fe3+可用KSCN溶液检验,形成的配合物颜色为
(3)氮元素的最简单氢化物为氨,氨的沸点
(4)铁的第三电离能(I3),第四电离能(I4)分别为2957kJ/mol,5290kJ/mol,I4远大于I3的原因是
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:

更新时间:2019/04/01 17:57:00
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)基态碳原子的核外电子排布式为______ 。非金属元素 的第一电离能大于
的第一电离能大于 的第一电离能,原因是
的第一电离能,原因是______ 。
(2)下表是第三周期部分元素的电离能[单位:[ (电子伏特)]数据。
(电子伏特)]数据。
下列说法正确的是______ (填序号)。
A.甲的金属性比乙强
B.乙有 价
价
C.丙不可能为非金属元素
D.丁一定为金属元素
(3) 、
、 均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
锰元素位于第四周期第ⅦB族。请写出基态 的价电子排布式:
的价电子排布式:______ ,比较两元素的I2、I3可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是______ 。
(4)卤族元素 、
、 、
、 、
、 的电负性由小到大的顺序是
的电负性由小到大的顺序是______ 。
(5)基态 原子的电子排布式为
原子的电子排布式为______ ; 和
和 相比,电负性较大的是
相比,电负性较大的是______ ; 中
中 元素的化合价为
元素的化合价为______ 。
(1)基态碳原子的核外电子排布式为
 的第一电离能大于
的第一电离能大于 的第一电离能,原因是
的第一电离能,原因是(2)下表是第三周期部分元素的电离能[单位:[
 (电子伏特)]数据。
(电子伏特)]数据。| 元素 |  | 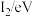 | 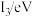 |
| 甲 | 5.7 | 47.4 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
下列说法正确的是
A.甲的金属性比乙强
B.乙有
 价
价C.丙不可能为非金属元素
D.丁一定为金属元素
(3)
 、
、 均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:| 元素 |  |  | |
电离能/(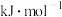 ) ) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
锰元素位于第四周期第ⅦB族。请写出基态
 的价电子排布式:
的价电子排布式: 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是(4)卤族元素
 、
、 、
、 、
、 的电负性由小到大的顺序是
的电负性由小到大的顺序是(5)基态
 原子的电子排布式为
原子的电子排布式为 和
和 相比,电负性较大的是
相比,电负性较大的是 中
中 元素的化合价为
元素的化合价为
您最近一年使用:0次
【推荐2】下表为元素周期表前三周期的一部分:
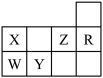
(1)判断X__________ Y __________ Z __________ W__________ R ________ (写元素符号)。
(2)写出X的氢化物的化学式;__________ ,W的氢化物的化学式__________ ,其沸点比较:__________ >________ (填化学式)
(3)下图是X的基态原子的电子排布图,其中有一个是错误的,它不能作为基态原子的电子排布图是因为它不符合________ 。
①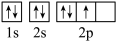
②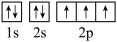
(4)以上五种元素中,________ (填元素符号)元素第一电离能最大。__________ 元素电负性最大,Y的基态原子的电子排布式为__________

(1)判断X
(2)写出X的氢化物的化学式;
(3)下图是X的基态原子的电子排布图,其中有一个是错误的,它不能作为基态原子的电子排布图是因为它不符合
①

②

(4)以上五种元素中,
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】非金属氮化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态N原子核外电子的运动状态有___________ 种,其核外电子占据能量最高的能级电子云轮廓图形状为___________ 。
(2)氟化硝酰(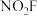 )可用作火箭推进剂中的氧化剂,上述所涉及元素中,电负性由大到小顺序为
)可用作火箭推进剂中的氧化剂,上述所涉及元素中,电负性由大到小顺序为___________ ;第一电离能由大到小顺序为_________ 。
(3)气态 的分子结构为
的分子结构为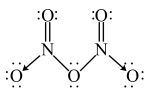 ,而固态
,而固态 则由
则由 与
与 构成。
构成。 的空间构型为
的空间构型为_________ , 中N的杂化方式为
中N的杂化方式为___________ 。
(4)一种新型的氮碳化合物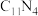 的晶体属于四方晶系,其沿着y轴的投影如图1所示,晶胞参数及侧视图如图2所示。
的晶体属于四方晶系,其沿着y轴的投影如图1所示,晶胞参数及侧视图如图2所示。______ 。
(5)已知某氮化铁的晶胞结构如图所示,则氮化铁的化学式为___________ ,若该晶体的密度是 ,则晶胞中两个最近的Fe的核间距离为
,则晶胞中两个最近的Fe的核间距离为___________ cm(用含 、
、 的代数式表示)。
的代数式表示)。
(1)基态N原子核外电子的运动状态有
(2)氟化硝酰(
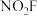 )可用作火箭推进剂中的氧化剂,上述所涉及元素中,电负性由大到小顺序为
)可用作火箭推进剂中的氧化剂,上述所涉及元素中,电负性由大到小顺序为(3)气态
 的分子结构为
的分子结构为 ,而固态
,而固态 则由
则由 与
与 构成。
构成。 的空间构型为
的空间构型为 中N的杂化方式为
中N的杂化方式为(4)一种新型的氮碳化合物
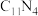 的晶体属于四方晶系,其沿着y轴的投影如图1所示,晶胞参数及侧视图如图2所示。
的晶体属于四方晶系,其沿着y轴的投影如图1所示,晶胞参数及侧视图如图2所示。
(5)已知某氮化铁的晶胞结构如图所示,则氮化铁的化学式为
 ,则晶胞中两个最近的Fe的核间距离为
,则晶胞中两个最近的Fe的核间距离为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)H2O的键角小于NH3的,分析原因_______ 。
(2)磷酸根离子的空间构型为_______ 。
(3)常温常压下SnCl4为无色液体,SnCl4空间构型为_______ 。
(4)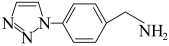 是一种叠氮炔基Husigen环加成反应产物,该分子中N原子的杂化方式为
是一种叠氮炔基Husigen环加成反应产物,该分子中N原子的杂化方式为_______ 。
(5)过渡元素铜的配合物在物质制备、尖端技术、医药科学、催化反应、材料化学等领域有着广泛的应用。请回答下列问题:
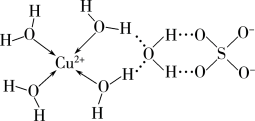
①科学家推测胆矾(CuSO4∙5H2O)的结构示意图可简单表示如图: 的空间结构为
的空间结构为_______ ,其中硫原子的轨道杂化方式为_______ 。
②Cu能与(SCN)2反应生成Cu(SCN)2。1mol(SCN)2中含有的π键数目为_______ ;(SCN)2对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),其中异硫氰酸的沸点较高,原因是_______ 。
(1)H2O的键角小于NH3的,分析原因
(2)磷酸根离子的空间构型为
(3)常温常压下SnCl4为无色液体,SnCl4空间构型为
(4)
 是一种叠氮炔基Husigen环加成反应产物,该分子中N原子的杂化方式为
是一种叠氮炔基Husigen环加成反应产物,该分子中N原子的杂化方式为(5)过渡元素铜的配合物在物质制备、尖端技术、医药科学、催化反应、材料化学等领域有着广泛的应用。请回答下列问题:
①科学家推测胆矾(CuSO4∙5H2O)的结构示意图可简单表示如图:
 的空间结构为
的空间结构为②Cu能与(SCN)2反应生成Cu(SCN)2。1mol(SCN)2中含有的π键数目为
您最近一年使用:0次
【推荐2】铝、铁在生活、生产中有着广泛的用途,请回答下列问题。
(1) Fe2+的最外层电子排布式____________ 。元素Fe与Mn的第三电离能分别为I3(Fe)、I3(Mn),则I3(Fe)______ I3(Mn)(填“>”、“<”)。
(2)气态氯化铝的分子组成为(AlCl3)2,其中Al、Cl均达8e-稳定结构,Al原子的杂化方式为__________ 。根据等电子原理,AlO2-的空间构型为_____ 。
(3) Fe(CO)5的熔点为-20 ℃,沸点为103 ℃,易溶于乙醚,其晶体类型为______ ,
(4)科学家们发现某些含铁的物质可催化尿素合成肼(N2H4),沸点:N2H4>C2H6的主要原因为______________________ 。
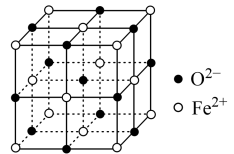
(5) FeO晶体的晶胞如图所示,已知:FeO晶体的密度为ρ g/cm3,NA代表阿伏加 德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____ ;Fe2+与O2-最短核间距为______ pm(用ρ和NA表示)。
(1) Fe2+的最外层电子排布式
(2)气态氯化铝的分子组成为(AlCl3)2,其中Al、Cl均达8e-稳定结构,Al原子的杂化方式为
(3) Fe(CO)5的熔点为-20 ℃,沸点为103 ℃,易溶于乙醚,其晶体类型为
(4)科学家们发现某些含铁的物质可催化尿素合成肼(N2H4),沸点:N2H4>C2H6的主要原因为
(5) FeO晶体的晶胞如图所示,已知:FeO晶体的密度为ρ g/cm3,NA代表阿伏加 德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】填空。
(1)OF2分子构型为___________ ,其中氧原子的杂化方式为___________ 。
(2)①V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是___________ 对,分子的立体构型为___________ ;SO3气态为单分子,该分子中S原子的杂化轨道类型为___________ ;SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为___________ ;该结构中S—O键长有两类,一类键长约140pm,另一类键长约160pm,较短的键为___________ (填图1中字母),该分子中含有___________ 个σ键。

②V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为___________ ;也可以得到偏钒酸钠,其阴离子呈如图所示的无限链状结构,则偏钒酸钠的化学式为___________ 。

(3)①碳在形成化合物时,其键型以共价键为主,原因是___________ 。
②CS2分子中,共价键的类型有___________ ,C原子的杂化轨道类型是___________ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子___________ 。
(1)OF2分子构型为
(2)①V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是

②V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为

(3)①碳在形成化合物时,其键型以共价键为主,原因是
②CS2分子中,共价键的类型有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】研究笼形包合物结构和性质具有重要意义。化学式为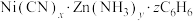 的笼形包合物四方晶胞结构如下图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数
的笼形包合物四方晶胞结构如下图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数 ,
, 。
。
(1)①基态 的核外电子排布式为
的核外电子排布式为___________ 。
② 的电子式为
的电子式为___________ 。
③ 的空间结构名称为
的空间结构名称为___________ 。
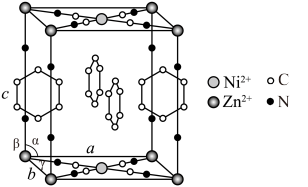
(2)已知晶胞中N原子均参与形成配位键,则 与
与 的配位数之比为
的配位数之比为___________ ;x:y:z=___________ 。
(3)吡啶(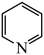 )替代苯也可形成类似的笼形包合物。吡啶在水中的溶解度远大于苯,主要原因是:
)替代苯也可形成类似的笼形包合物。吡啶在水中的溶解度远大于苯,主要原因是:
①___________ ;②___________ 。
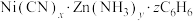 的笼形包合物四方晶胞结构如下图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数
的笼形包合物四方晶胞结构如下图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数 ,
, 。
。
(1)①基态
 的核外电子排布式为
的核外电子排布式为②
 的电子式为
的电子式为③
 的空间结构名称为
的空间结构名称为(2)已知晶胞中N原子均参与形成配位键,则
 与
与 的配位数之比为
的配位数之比为(3)吡啶(
 )替代苯也可形成类似的笼形包合物。吡啶在水中的溶解度远大于苯,主要原因是:
)替代苯也可形成类似的笼形包合物。吡啶在水中的溶解度远大于苯,主要原因是:①
您最近一年使用:0次
【推荐2】A~G是前四周期除稀有气体之外原子序数依次增大的七种元素。A与其他元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题:
(1)写出元素名称:B_______ ,G_______ 。
(2)写出F的价电子排布图:_______ 。
(3)写出化合物BC的结构式:__________________ 。
(4)由A、C、F三元素形成的离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是________________ 。
(5)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是______________________ 。
(6)E的一种晶体结构如图甲,则其一个晶胞中含有_______ 个E;G与D形成的化合物的晶胞结构如图乙,若晶体密度为ag/cm3,则G与D最近的距离为____ pm
(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)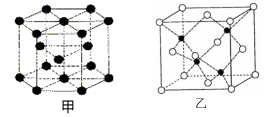
(1)写出元素名称:B
(2)写出F的价电子排布图:
(3)写出化合物BC的结构式:
(4)由A、C、F三元素形成的离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是
(5)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是
(6)E的一种晶体结构如图甲,则其一个晶胞中含有
(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】I.配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(1)Ni2+可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2+、丁二酮肟镍分子(见图)等。_____ (填“大“或“小”)。
②丁二酮肟镍分子内含有的作用力有_____ (填字母)。
a.配位键 b.离子键 c.氢键 d.金属键
(2)关于[Ti(NH3)5Cl]Cl2的说法中错误的是______ 。
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol[Ti(NH3)5Cl]Cl2的的水济液中加入足量AgNO3溶液,产生3mol白色沉淀
(3)已知[Co(NH3)6]3+立体结构如图,其中1~6处的小圆圈表示NH3分子,且各相邻的NH3分子间的距离相等(图中虚线长度相等)。Co3+位于正八面体的中心,岩其中两个NH3被Cl-取代,所形成的[Co(NH3)4Cl2]+的结构的数目为___________ 。_______ 。
a.σ键 b.极性键 c.作极性键 d.离子键 e.范德华力
(5)有机物吡啶(C5H5N),结构简式为 ,其中N的杂化方式为
,其中N的杂化方式为__________ 。吡啶在水中的溶解度远大于在苯中的溶解度,可能原因是:
①吡啶和水均为极性分子,相似相溶,而苯为非极性分子;
②__________ 。
(1)Ni2+可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2+、丁二酮肟镍分子(见图)等。

②丁二酮肟镍分子内含有的作用力有
a.配位键 b.离子键 c.氢键 d.金属键
(2)关于[Ti(NH3)5Cl]Cl2的说法中错误的是
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol[Ti(NH3)5Cl]Cl2的的水济液中加入足量AgNO3溶液,产生3mol白色沉淀
(3)已知[Co(NH3)6]3+立体结构如图,其中1~6处的小圆圈表示NH3分子,且各相邻的NH3分子间的距离相等(图中虚线长度相等)。Co3+位于正八面体的中心,岩其中两个NH3被Cl-取代,所形成的[Co(NH3)4Cl2]+的结构的数目为


a.σ键 b.极性键 c.作极性键 d.离子键 e.范德华力
(5)有机物吡啶(C5H5N),结构简式为
 ,其中N的杂化方式为
,其中N的杂化方式为①吡啶和水均为极性分子,相似相溶,而苯为非极性分子;
②
您最近一年使用:0次



