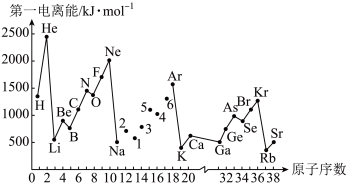
第一电离能I1是指气态电中性原子X(g)处于基态时,失去一个电子成为气态基态正离子X+(g)所需的最低能量。如图所示是部分元素原子的第一电离能I1随原子序数变化的关系图。
请回答下列问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na~Ar之间六种元素用短线连接起来,构成完整的图象___________ 。 第1、2、4、6号元素简单离子半径的大小关系是________ (用离子符号表示)。
(2)从题图分析可知,同主族元素原子的第一电离能I1变化规律是________ 。
(3)题图中5号元素在周期表中的位置是________ ;处于______ 区。
(4)题图中4、5、6号三种元素的最简单气态氢化物的沸点均比同主族上一周期元素的最简单气态氢化物的沸点低,原因是____________ 。

请回答下列问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na~Ar之间六种元素用短线连接起来,构成完整的图象
(2)从题图分析可知,同主族元素原子的第一电离能I1变化规律是
(3)题图中5号元素在周期表中的位置是
(4)题图中4、5、6号三种元素的最简单气态氢化物的沸点均比同主族上一周期元素的最简单气态氢化物的沸点低,原因是
2019高二下·全国·专题练习 查看更多[1]
(已下线)2019年4月14日 《每日一题》选修3-每周一测
更新时间:2019-04-10 16:59:17
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】I.从下列物质中选出合适组号填写在对应空格上。
A.红磷与白磷 B.蔗糖与麦芽糖 C.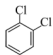 与
与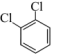
D.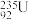 与
与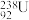 E.环氧乙烷(
E.环氧乙烷(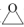 )与乙醛
)与乙醛
F. 与
与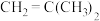
G.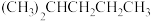 与
与
(1)同位素___________ 。
(2)同系物___________ 。
(3)同分异构体___________ 。
(4)同一物质___________ 。
II.已知:a是元素周期表中半径最小的元素,b是短周期中金属性最强的元素:下图是部分短周期元素在周期表中的位置,且g元素的最高正价与最低负价之和为4。
(1)c处于周期表的第___________ 周期___________ 族;g的简单阴离子的结构示意图为___________ 。
(2)a、d、h形成的常见离子化合物的电子式为___________ 。
(3)用电子式表示b、h形成化合物的过程___________ 。
(4)d、e、h元素对应的简单离子半径由小到大的顺序是___________ (用离子符号表示)。
(5)d的简单氢化物比f的简单氢化物的沸点高,原因是___________ 。
(6)写出e的单质与b的最高价氧化物对应的水化物反应的离子方程式___________ 。
A.红磷与白磷 B.蔗糖与麦芽糖 C.
 与
与
D.
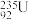 与
与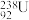 E.环氧乙烷(
E.环氧乙烷( )与乙醛
)与乙醛F.
 与
与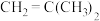
G.
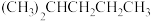 与
与
(1)同位素
(2)同系物
(3)同分异构体
(4)同一物质
II.已知:a是元素周期表中半径最小的元素,b是短周期中金属性最强的元素:下图是部分短周期元素在周期表中的位置,且g元素的最高正价与最低负价之和为4。
| c | d | |||
| e | f | g | h |
(2)a、d、h形成的常见离子化合物的电子式为
(3)用电子式表示b、h形成化合物的过程
(4)d、e、h元素对应的简单离子半径由小到大的顺序是
(5)d的简单氢化物比f的简单氢化物的沸点高,原因是
(6)写出e的单质与b的最高价氧化物对应的水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】1869年门捷列夫制得世界上第一张元素周期表,它反映了元素之间的内在联系。元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是现代长式元素周期表的一部分,数字①~⑩代表十种元素,请按题目要求回答下列问题(以下问题均用相应的化学符号表达):
(1)元素周期表中元素种类最多的族是_______ 。
(2)元素⑤的一种核素可以用来考古断代,该核素的符号为_______ 。
(3)在这10种元素中,金属性最强的元素对应的单质与水反应的化学方程式为_______ 。
(4)元素③④⑦⑩的简单离子半径的由大到小的顺序为_______ ;比较元素⑨⑩的简单氢化物的还原性:_______ >_______ 。
(5)元素②的最高价氧化物对应的水化物的电子式为_______ ,其与元素⑧的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(6)由元素①⑥⑩三种元素形成的盐中所含化学键的类型有_______ 。
| ① | |||||||||||||||||
| ⑤ | ⑥ | ⑦ | |||||||||||||||
| ② | ③ | ⑧ | ⑨ | ⑩ | |||||||||||||
| ④ | |||||||||||||||||
(2)元素⑤的一种核素可以用来考古断代,该核素的符号为
(3)在这10种元素中,金属性最强的元素对应的单质与水反应的化学方程式为
(4)元素③④⑦⑩的简单离子半径的由大到小的顺序为
(5)元素②的最高价氧化物对应的水化物的电子式为
(6)由元素①⑥⑩三种元素形成的盐中所含化学键的类型有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】W、X、Y、Z、M、G、H七种短周期元素,原子序数依次增大。W、Z同主族,可形成离子化合物ZW;Y、G同主族,可形成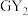 、
、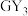 两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
(1)Y在元素周期表中的位置为_______ 。
(2)X的气态氢化物的电子式为_____ ,工业合成X的气态氢化物的化学方程式为______ 。
(3)Y、Z、G三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(4)Z、M最高价氧化物对应的水化物相互反应的离子方程式为_______ ,G的最高价氧化物对应的水化物的浓溶液与金属铜反应的化学方程式为_______ 。
(5)G的非金属性_______ (填“>”或“<”)H的非金属性,下列表述可以作为验证的证据的是_______ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易程度
C.G和H单质分别与Fe反应生成FeG、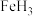
D.比较这两种元素单质与酸或碱反应的难易程度
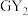 、
、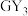 两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
两种分子;X的气态氢化物与其最高价氧化物对应的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:(1)Y在元素周期表中的位置为
(2)X的气态氢化物的电子式为
(3)Y、Z、G三种元素原子半径由大到小的顺序是
(4)Z、M最高价氧化物对应的水化物相互反应的离子方程式为
(5)G的非金属性
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易程度
C.G和H单质分别与Fe反应生成FeG、
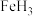
D.比较这两种元素单质与酸或碱反应的难易程度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】原子序数依次增大的短周期元素A、B、C、D、E,周期表中A与B、C与E相邻;A与E的最外层电子数之比2:3,B的最外层电子数比C的最外层电子数少1个;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红。
(1)E的元素名称是___________ ,该元素在周期表中的位置为___________
(2)C、D、E的原子半径由大到小的顺序是___________ (用元素符号表示)
(3)A、B、C的简单氢化物稳定性由弱到强的顺序为___________ (用分子式表示)
(4)C的简单氢化物与E的简单氢化物,沸点较高的是___________ (填化学式),理由是___________
(5)B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z中所含化学键的类型为___________
(6)B、C可形成10电子的微粒,其中①和②为分子,①溶于②后可电离出阳离子③和阴离子④,写出下列四种微粒的化学式①___________ ;②___________ ;③___________ ;④___________
(7)用电子式表示D2C2的形成过程为___________ ,D2C2与水反应的离子方程式为___________
(1)E的元素名称是
(2)C、D、E的原子半径由大到小的顺序是
(3)A、B、C的简单氢化物稳定性由弱到强的顺序为
(4)C的简单氢化物与E的简单氢化物,沸点较高的是
(5)B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z中所含化学键的类型为
(6)B、C可形成10电子的微粒,其中①和②为分子,①溶于②后可电离出阳离子③和阴离子④,写出下列四种微粒的化学式①
(7)用电子式表示D2C2的形成过程为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】镍及其化合物是重要的合金材料和催化剂。请回答下列问题:
(1)基态镍原子的价层电子排布式为______ ,排布时最高能层的电子所占的原子轨道有______ 种伸展方向。
(2)镍能形成多种配合物如正四面体形的 、正方形的
、正方形的 和正八面体形的
和正八面体形的 等。下列说法不正确的有
等。下列说法不正确的有______ 。
A. 分子内σ键和π键个数之比为1:2
分子内σ键和π键个数之比为1:2
B. 的空间结构为平面三角形
的空间结构为平面三角形
C. 在形成配合物时,其配位数可能为4或6
在形成配合物时,其配位数可能为4或6
D. 中,镍元素是
中,镍元素是 杂化
杂化
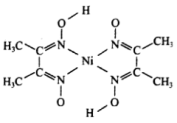
(3)丁二酮肟常用于检验 :在稀氨水中,丁二酮肟与
:在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用“…”表示出氢键
反应生成鲜红色沉淀,其结构如图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用“…”表示出氢键______ 。
(4) 的晶体结构类型与氯化钠的相同,相关离子半径如下表:
的晶体结构类型与氯化钠的相同,相关离子半径如下表:
 熔点比
熔点比 高的原因是
高的原因是______ 。
(1)基态镍原子的价层电子排布式为
(2)镍能形成多种配合物如正四面体形的
 、正方形的
、正方形的 和正八面体形的
和正八面体形的 等。下列说法不正确的有
等。下列说法不正确的有A.
 分子内σ键和π键个数之比为1:2
分子内σ键和π键个数之比为1:2B.
 的空间结构为平面三角形
的空间结构为平面三角形C.
 在形成配合物时,其配位数可能为4或6
在形成配合物时,其配位数可能为4或6D.
 中,镍元素是
中,镍元素是 杂化
杂化(3)丁二酮肟常用于检验
 :在稀氨水中,丁二酮肟与
:在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用“…”表示出氢键
反应生成鲜红色沉淀,其结构如图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用“…”表示出氢键
(4)
 的晶体结构类型与氯化钠的相同,相关离子半径如下表:
的晶体结构类型与氯化钠的相同,相关离子半径如下表: | 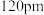 |  | 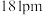 |
 | 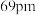 |  |  |
 熔点比
熔点比 高的原因是
高的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、Q、E五种元素中,X原子核外M层中只有两对成对电子,Y原子核外L层电子数是K层两倍,Z是地壳内含量(质量分数)最高元素,Q核电荷数是X与Z核电荷数之和,E电负性最大。
(1)相同条件下XZ2与YZ2分子在水中溶解度较大是 ,理由是
;
(2)Q的外围电子排布为 ,在形成化合物时它的最高化合价为 ;
(3)在测定E的气态氢化物的相对分子质量时,实验测得的值一般高于理论值的主要原因是: 。
(1)相同条件下XZ2与YZ2分子在水中溶解度较大是 ,理由是
;
(2)Q的外围电子排布为 ,在形成化合物时它的最高化合价为 ;
(3)在测定E的气态氢化物的相对分子质量时,实验测得的值一般高于理论值的主要原因是: 。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氯化氰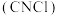 ,又名氯甲氰,是重要的化工中间体,在农药、医药、化工助剂等方面有着广泛的应用。某小组制备氯化氰并探究其性质,装置如图所示。回答下列问题:
,又名氯甲氰,是重要的化工中间体,在农药、医药、化工助剂等方面有着广泛的应用。某小组制备氯化氰并探究其性质,装置如图所示。回答下列问题:

已知部分信息如下:
①CNCl的熔点为-6.5℃,沸点为13.1℃,可溶于水并与水反应; 具有较强的还原性。
具有较强的还原性。
②合成原理:在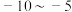 ℃条件下,
℃条件下,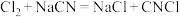 。
。
(1) 所含元素中第一电离能最大的是
所含元素中第一电离能最大的是___________ (填元素符号),B的作用是___________ 。
(2)F中干冰和丙酮的作用是降低温度,此时干冰___________ (填“升华”或“凝华”)。
(3)实验中,先向D中通入___________ (填“ ”或“
”或“ ”)。
”)。
(4)D中温度高于-5℃时,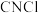 与
与 反应只生成
反应只生成 和气体X(纯净物,其结构中不含环状结构),X的电子式为
和气体X(纯净物,其结构中不含环状结构),X的电子式为___________ 。当G中___________ (填实验现象)时,停止通入 。
。
(5)本实验在通风橱中进行且操作者佩戴防毒面具,原因是___________ 。向盛有 溶液的试管中通入少量
溶液的试管中通入少量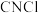 ,然后滴加一滴
,然后滴加一滴 溶液,溶液立即变为红色,
溶液,溶液立即变为红色, 和
和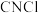 反应的离子方程式为
反应的离子方程式为___________ 。
(6)上述实验中, 完全反应时收集到
完全反应时收集到
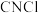 ,产率为
,产率为___________ %(结果保留整数)。
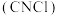 ,又名氯甲氰,是重要的化工中间体,在农药、医药、化工助剂等方面有着广泛的应用。某小组制备氯化氰并探究其性质,装置如图所示。回答下列问题:
,又名氯甲氰,是重要的化工中间体,在农药、医药、化工助剂等方面有着广泛的应用。某小组制备氯化氰并探究其性质,装置如图所示。回答下列问题:
已知部分信息如下:
①CNCl的熔点为-6.5℃,沸点为13.1℃,可溶于水并与水反应;
 具有较强的还原性。
具有较强的还原性。②合成原理:在
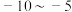 ℃条件下,
℃条件下,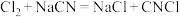 。
。(1)
 所含元素中第一电离能最大的是
所含元素中第一电离能最大的是(2)F中干冰和丙酮的作用是降低温度,此时干冰
(3)实验中,先向D中通入
 ”或“
”或“ ”)。
”)。(4)D中温度高于-5℃时,
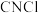 与
与 反应只生成
反应只生成 和气体X(纯净物,其结构中不含环状结构),X的电子式为
和气体X(纯净物,其结构中不含环状结构),X的电子式为 。
。(5)本实验在通风橱中进行且操作者佩戴防毒面具,原因是
 溶液的试管中通入少量
溶液的试管中通入少量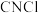 ,然后滴加一滴
,然后滴加一滴 溶液,溶液立即变为红色,
溶液,溶液立即变为红色, 和
和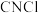 反应的离子方程式为
反应的离子方程式为(6)上述实验中,
 完全反应时收集到
完全反应时收集到
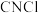 ,产率为
,产率为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】氮、铜及其化合物以及乙醇、氯化钠的用途广泛。回答下列问题:
(1)C、N、O、F四种元素的第一电离能由小到大的顺序为___________ 。
(2)N价层电子的轨道表达式(电子排布图)为___________ 。CuO在高温下能分解生成Cu2O,其原因是___________ 。
(3)在加热和Cu的催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中碳原子的杂化方式是___________ ,乙醛分子中H−C=O的键角___________ (填“大于”“等于”或“小于”)乙醇分子中的H−C−O的键角。
(4)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl−取代后有两种不同的结构,其中[Cu( H2O)2(Cl)2]是非极性分子的结构式为___________ 。
(5)如图所示为NaCl晶体的晶胞结构图和晶胞截面图(截面图中的大球为Cl−,小球为Na+);

①晶胞中距离1个Na+最近的Cl−有___________ 个,这些C1−围成的图形是___________ 。
②若晶体密度为ρg∙cm−3,阿伏伽德罗常数的值用NA表示,则Na+的离子半径为___________ pm(列出计算表达式)。
(1)C、N、O、F四种元素的第一电离能由小到大的顺序为
(2)N价层电子的轨道表达式(电子排布图)为
(3)在加热和Cu的催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中碳原子的杂化方式是
(4)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl−取代后有两种不同的结构,其中[Cu( H2O)2(Cl)2]是非极性分子的结构式为
(5)如图所示为NaCl晶体的晶胞结构图和晶胞截面图(截面图中的大球为Cl−,小球为Na+);

①晶胞中距离1个Na+最近的Cl−有
②若晶体密度为ρg∙cm−3,阿伏伽德罗常数的值用NA表示,则Na+的离子半径为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】碳族元素(Carbongroup)是位于元素周期表IVA族的元素,包括碳(C)、硅(Si)、锗(Ge),锡(Sn)、铅(Pb)、鈇(Fl)六种。请回答:
(1)鈇(Fl),其命名是为了纪念苏联原子物理学家乔治弗洛伊洛夫,是一种人工合成的放射性化学元素,它的化学符号是Uuq,它的原子序数是_______ , 属于弱金属之一。
(2)基态锡原子价电子的轨道表示式为_______ ;与Ge同周期且未成对电子数相同的元素还有_______ 种。
(3)碱金属元素是位于元素周期表第IA族(除氢外)的元素。第一电离能(I1)的变化趋势是自上而下依次减小,其原因是_______ 。
(4)石英玻璃(非晶态二氧化硅)和水晶(晶态二氧化硅)外观很相似,可通过_______ 法进行科学区分。
(5)金刚石和石墨是碳元素形成的常见单质,下列关于这两种单质的对比叙述中正确的有_______ 。
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C
c.晶体的熔点:金刚石>石墨
d. 晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力
f. 金刚石和石墨的熔点都很高,所以金刚石和石墨都是共价晶体
g. 在金刚石和石墨的结构中, 由共价键形成的最小碳环均是六元环
(6)三氯甲烷(CHCl3)常温下为无色透明液体。有特殊气味,味甜,低毒,有麻醉性,有致癌可能性。三氯甲烷的是_______ 分子(选填“极性”或“非极性”), 碳元素的化合价是_______ 。
(1)鈇(Fl),其命名是为了纪念苏联原子物理学家乔治弗洛伊洛夫,是一种人工合成的放射性化学元素,它的化学符号是Uuq,它的原子序数是
(2)基态锡原子价电子的轨道表示式为
(3)碱金属元素是位于元素周期表第IA族(除氢外)的元素。第一电离能(I1)的变化趋势是自上而下依次减小,其原因是
(4)石英玻璃(非晶态二氧化硅)和水晶(晶态二氧化硅)外观很相似,可通过
(5)金刚石和石墨是碳元素形成的常见单质,下列关于这两种单质的对比叙述中正确的有
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化
b.晶体中共价键的键长:金刚石中C-C<石墨中C-C
c.晶体的熔点:金刚石>石墨
d. 晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力
f. 金刚石和石墨的熔点都很高,所以金刚石和石墨都是共价晶体
g. 在金刚石和石墨的结构中, 由共价键形成的最小碳环均是六元环
(6)三氯甲烷(CHCl3)常温下为无色透明液体。有特殊气味,味甜,低毒,有麻醉性,有致癌可能性。三氯甲烷的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】锌及其化合物在工业、农业方面用途广泛。
(1)基态Zn原子的价电子排布式为_______ 。
(2)Zn原子能形成多种配位化合物。一种锌的配合物结构如图:_______ ,结构中参与sp3杂化原子有_______ 个。
②配位键①和②相比。较稳定的是_______ ;键角③_______ 键角④(填“>”、“<”、“=”)。
(3)(CH3COO)2Zn和ZnC2O4中阴离子对应的酸中沸点较高的是_______ (写结构简式),原因是_______ 。
(4)ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,下图为这两种晶体的局部结构。_______ 。
②闪锌矿型中Zn2+填入O2-所形成的“正四面体”空隙中,闪锌矿晶胞中含有_______ 个“正四面体”空隙。
③图b闪锌矿型晶胞密度为ρg/cm3.则Zn2+与O2-的距离为_______ nm。(设NA为阿伏加德罗常数的值)
(1)基态Zn原子的价电子排布式为
(2)Zn原子能形成多种配位化合物。一种锌的配合物结构如图:

②配位键①和②相比。较稳定的是
(3)(CH3COO)2Zn和ZnC2O4中阴离子对应的酸中沸点较高的是
(4)ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,下图为这两种晶体的局部结构。

②闪锌矿型中Zn2+填入O2-所形成的“正四面体”空隙中,闪锌矿晶胞中含有
③图b闪锌矿型晶胞密度为ρg/cm3.则Zn2+与O2-的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题(凡涉及的物质均用化学式表示):
(1)基态硫原子的价电子排布图为___________ 。第一电离能介于Al、P之间的第三周期元素有___________ 种。a的氢化物的分子构型为___________ ,中心原子的杂化形式为___________ ;d的最高价氧化物的分子构型为___________ ,中心原子的杂化形式为___________ ,该分子是___________ (填“极性”或“非极性”)分子。
(2)b、d、e三种元素的氢化物中的沸点最高的是___________ ,原因是_____________ 。de2的电子式___________ ,它在常温下呈液态,形成晶体时属于___________ 晶体。
(3)将g的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,写出该配合离子的结构简式___________ (必须将配位键表示出来)。
(4)f(NH3)5BrSO4可形成两种配合物 ,已知f3+的配位数是6,为确定f的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,第二种配合物的化学式为___________ ,该配合物的配体是___________ 、___________ ;
(5)SO2中S的杂化类型为___________ ,SO2的立体构型为___________ 。
(6)c单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
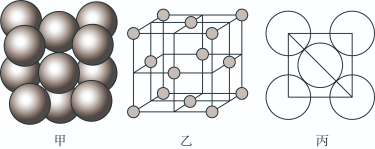
若已知c的原子半径为r,NA代表阿伏加德罗常数,c的相对原子质量为M。该晶体的密度为___________ (用字母表示)。

试回答下列问题(凡涉及的物质均用化学式表示):
(1)基态硫原子的价电子排布图为
(2)b、d、e三种元素的氢化物中的沸点最高的是
(3)将g的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,写出该配合离子的结构简式
(4)f(NH3)5BrSO4可形成两种配合物 ,已知f3+的配位数是6,为确定f的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,第二种配合物的化学式为
(5)SO2中S的杂化类型为
(6)c单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

若已知c的原子半径为r,NA代表阿伏加德罗常数,c的相对原子质量为M。该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。
(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
(2)第三周期元素的原子中,未成对电子不可能有_______。
(3)基态F原子的轨道表示式为_______ ,四氟乙烯的电子式为_______ 。
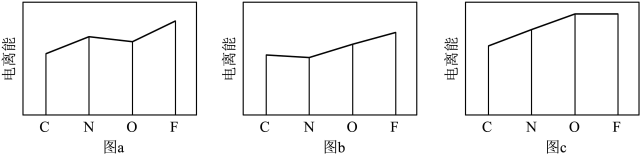
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填字母),第三电离能的变化图是_______ (填字母)。
(5) 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为_______ 和_______ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(6)比较甲醚和乙醇的沸点高低,并说明理由_______ 。
 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
| A.原子与原子之间 | B.分子与分子之间 | C.离子与离子之间 | D.离子与电子之间 |
(2)第三周期元素的原子中,未成对电子不可能有_______。
| A.4个 | B.3个 | C.2个 | D.1个 |
(3)基态F原子的轨道表示式为
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(5)
 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为(6)比较甲醚和乙醇的沸点高低,并说明理由
您最近一年使用:0次



