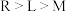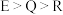依据下列说法来判断相应元素的金属性、非金属性强弱,不合理的是
| A.非金属气态氢化物的稳定性 |
| B.非金属氧化物对应水化物酸性的强弱或单质间的置换反应 |
| C.金属单质与氧气,水或酸反应的剧烈程度 |
| D.等量Na、Mg、Al分别与足量盐酸反应时失电子的难易程度 |
更新时间:2019-04-16 15:51:48
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是电子层数的3倍,Z的焰色反应呈黄色。常温下,Z和W形成化合物的水溶液的pH=7。下列说法正确的是
| A.X与W属于不同周期、不同主族元素 |
| B.简单离子半径:X<Z |
| C.简单氢化物的沸点:Y>W>Z |
| D.Z和W形成的化合物的水溶液与Y单质反应,能置换出W |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】短周期元素R、X、Y、Z、M原子序数依次递增,原子最外层电子数存在关系:3Z+M=X+Y,其中元素R、X、Y、M形成的化合物(结构式)具有如图所示的转化关系。下列说法正确的是
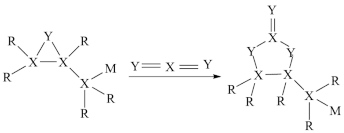

| A.原子半径:Z>M>Y>X>R |
| B.氧化物对应水化物的酸性:M>X |
| C.Y与Z形成的化合物只含共价键 |
| D.R与X形成的化合物可能会使酸性高锰酸钾溶液褪色 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列叙述正确的是
| A.A和B是元素周期表中同主族的金属元素,A在B的下方,则A肯定比B的金属性强 |
| B.1molA与酸反应转移3mol电子,1molB与酸反应转移2mol电子,可以证明A比B的金属性强 |
C. 比 比 的酸性弱,证明C比S的非金属性强 的酸性弱,证明C比S的非金属性强 |
| D.元素简单氢化物的沸点X比元素Y的熔沸点高,能证明元素X比元素Y的非金属性弱 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是其最内层电子数的3倍。下列说法正确的是
| A.原子半径:Z>W>R>X |
| B.对应气态氢化物的热稳定性:W>R>Y |
| C.W与Y、Z与R形成的化合物微粒组成比相同 |
| D.W与R的氧化物对应的水化物是强酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列性质的比较,不能用元素周期律解释的是
A.原子半径: > > | B.还原性: > > |
C.热稳定性: > > | D.酸性: > > |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列实验操作、现象和结论都正确的是
| 实验操作 | 现象 | 结论 | |
| A | 用玻璃棒蘸取某样品进行焰色试验 | 产生黄色火焰 | 该样品含钠元素 |
| B | 向0.5 g淀粉中加入4 mL2 mo/LH2SO4溶液,加热,冷却后加入少量新制Cu(OH)2并加热 | 未出现砖红色沉淀 | 淀粉没有发生水解 |
| C | 分别向Mg(OH)2沉淀和Al(OH)3沉淀中加入NaOH溶液 | Mg(OH)2不溶解,Al(OH)3溶解 | Mg金属性强于Al |
| D | SO2气体通入紫色石磊试液中 | 溶液先变红后褪色 | H2SO3具有酸性和漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列条件下的离子方程式正确的有个
①向硫酸铜溶液中滴加氢氧化钡溶液:Cu2++2OH-=Cu(OH)2↓
②用FeCl3溶液腐蚀印刷电路板:Cu+Fe3+=Cu2++Fe2+
③向NaOH溶液中通入过量的CO2:CO2+2OH-=CO +H2O
+H2O
④将一小块钠用铝箔包裹,扎好小孔后,用镊子夹住按入水下,并用试管收集氢气,只发生了:2Na+2H2O=2Na++2OH-+H2↑
⑤向AlCl3溶液中滴加氨水至过量制备Al(OH)3:Al3++3OH-=Al(OH)3↓
⑥除去FeCl3中的FeCl2:Cl2+2Fe2+=2Cl-+2Fe3+
⑦证明元素非金属性Cl>C:CaCO3+2HCl=CaCl2+H2O+CO2↑
⑧证明元素金属性Na>Al:Al(OH)3+OH-= [Al(OH)4]-
①向硫酸铜溶液中滴加氢氧化钡溶液:Cu2++2OH-=Cu(OH)2↓
②用FeCl3溶液腐蚀印刷电路板:Cu+Fe3+=Cu2++Fe2+
③向NaOH溶液中通入过量的CO2:CO2+2OH-=CO
 +H2O
+H2O④将一小块钠用铝箔包裹,扎好小孔后,用镊子夹住按入水下,并用试管收集氢气,只发生了:2Na+2H2O=2Na++2OH-+H2↑
⑤向AlCl3溶液中滴加氨水至过量制备Al(OH)3:Al3++3OH-=Al(OH)3↓
⑥除去FeCl3中的FeCl2:Cl2+2Fe2+=2Cl-+2Fe3+
⑦证明元素非金属性Cl>C:CaCO3+2HCl=CaCl2+H2O+CO2↑
⑧证明元素金属性Na>Al:Al(OH)3+OH-= [Al(OH)4]-
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示。若Z原子的最外层电子数是K层电子数的3倍,下列说法中正确的是
| X | Y | |
| Z | W |
| A.X元素的最常见气态氢化物的水溶液显酸性 |
| B.W的氧化物对应水化物的酸性比Z强 |
| C.Z的单质与氢气反应比Y单质与氢气反应更容易发生 |
| D.Y的气态氢化物比Z的气态氢化物更稳定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】能说明氯的非金属性比硫强的事实是
①氯和硫单质与铜反应生成化合物中铜的化合价
②酸性:HClO4>H2SO4
③沸点:HCl<H2S
④酸性:HCl>H2S
①氯和硫单质与铜反应生成化合物中铜的化合价
②酸性:HClO4>H2SO4
③沸点:HCl<H2S
④酸性:HCl>H2S
| A.①②③ | B.①②④ | C.①② | D.③④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列结论正确 的是
①微粒半径:S2->K+>Al3+
②氢化物的稳定性:HF>HCl>SiH4
③离子的还原性: Cl->Br->I-
④氧化性:F2>S>Se
⑤酸性:HClO>H2SO4>H3PO4
⑥非金属性:O>N>Si
⑦金属性:Be>Ca>K
⑧碱性:NaOH>Be(OH)2>LiOH
①微粒半径:S2->K+>Al3+
②氢化物的稳定性:HF>HCl>SiH4
③离子的还原性: Cl->Br->I-
④氧化性:F2>S>Se
⑤酸性:HClO>H2SO4>H3PO4
⑥非金属性:O>N>Si
⑦金属性:Be>Ca>K
⑧碱性:NaOH>Be(OH)2>LiOH
| A.①②④⑥ | B.①③④⑥ | C.①③⑥⑧ | D.②⑤⑥⑧ |
您最近一年使用:0次