氮、铬及其相关化合物用途非常广泛。回答下列问题:
(1)基态N原子的核外电子排布式为___ ,Cr位于元素周期表第四周期___ 族。
(2) Cr与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为___ ;Crcl3的熔点(83℃)比CrF3的熔点(1100℃)低得多,这是因为___ 。
(3) Cr的一种配合物结构如图所示:
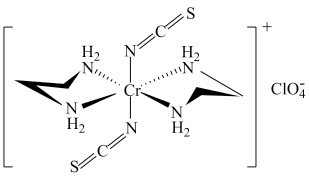
①阴离子C1O4-的空间构型为___ 形。
②配离子中,中心离子的配位数为___ ,N与中心原子形成的化学键称为___ 键。
③配体H2 NCH2 CH2 NH2(乙二胺)中碳原子的杂化方式是______ ,分子中三种元素电负性从大到小的顺序为___
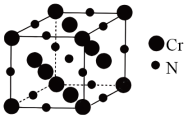
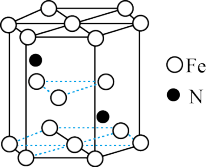
(4)氮化铬的熔点为1770℃,它的一种晶体的晶胞结构如图所示,其密度为5. 9 g·cm -3,氮化铬的晶胞边长为___ (列出计算式)nm.
(1)基态N原子的核外电子排布式为
(2) Cr与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为
(3) Cr的一种配合物结构如图所示:

①阴离子C1O4-的空间构型为
②配离子中,中心离子的配位数为
③配体H2 NCH2 CH2 NH2(乙二胺)中碳原子的杂化方式是
(4)氮化铬的熔点为1770℃,它的一种晶体的晶胞结构如图所示,其密度为5. 9 g·cm -3,氮化铬的晶胞边长为

更新时间:2019-04-18 16:48:09
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】中国海军航母建设正在有计划、有步骤向前推进。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢抗腐蚀性能强,Ni2+基态原子的核外电子排布为_______________________ .
(2)航母甲板涂有一层耐高温的材料聚硅氧烷结构如图所示,其中C原子杂化方式为______ 杂化,在有机物中C原子间可以形成双键,而硅烷中Si原子间难以形成双键的原因是_____________ .

(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是_________ (填元素符号)
②根据价层电子对互斥理论,预测ClO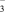 的空间构型为
的空间构型为___________ 形,写出一个ClO 的等电子体的化学符号
的等电子体的化学符号___________ .
(4)海底金属软泥是在洋海底蕴藏着大量的资源,含有硅、铁、锰、锌等。某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为________________ ,若晶胞底边长为a nm,高为c nm,则这种磁性氮化铁的晶体密度为________ g·cm−3(用含a、c和NA的式子表示)
(1)镍铬钢抗腐蚀性能强,Ni2+基态原子的核外电子排布为
(2)航母甲板涂有一层耐高温的材料聚硅氧烷结构如图所示,其中C原子杂化方式为

(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
 的空间构型为
的空间构型为 的等电子体的化学符号
的等电子体的化学符号(4)海底金属软泥是在洋海底蕴藏着大量的资源,含有硅、铁、锰、锌等。某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硫及其化合物有许多用途,相关物质的物理常数如表所示:
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为____ 。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是___ 。
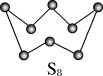
(3)如图为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为____ 。S原子的杂化轨道类型为___ 。
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为___ 形,固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为____ 。

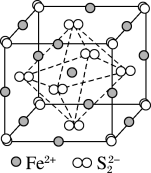
(5)FeS2晶体的晶胞如图所示,晶胞边长为anm,FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为____ g•cm-3;晶胞中Fe2+位于S 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为___ nm。
| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(3)如图为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为

(5)FeS2晶体的晶胞如图所示,晶胞边长为anm,FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为
 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】钛及其化合物被广泛应用于飞机、火箭、卫星、舰艇、医疗等领域。
(1)基态Ti原子的价电子轨道表示式是______ 。
(2) 与
与 互为等电子体,
互为等电子体, 与
与 甲基咪唑
甲基咪唑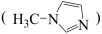 反应可以得到
反应可以得到
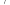 其结构如下图所示。
其结构如下图所示。
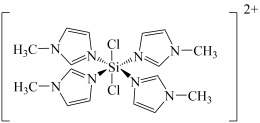
① 分子的空间构型为
分子的空间构型为______ 。
② 甲基咪唑分子中碳原子的杂化轨道类型为
甲基咪唑分子中碳原子的杂化轨道类型为______ ,C、N、Si的电负性由大到小的顺序为______ ,1个 中含有
中含有______ 个σ键。
③ 稳定性比
稳定性比 差,试从化学键角度分析原因:
差,试从化学键角度分析原因:______ 。
(3) 属于四方晶系,晶胞棱边夹角均为90°。研究表明,
属于四方晶系,晶胞棱边夹角均为90°。研究表明, 通过氮掺杂反应可生成
通过氮掺杂反应可生成 ,能使
,能使 对可见光具有活性,反应如图所示。
对可见光具有活性,反应如图所示。
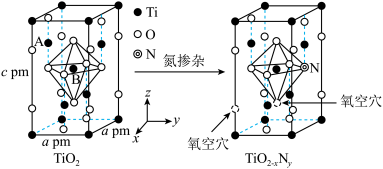
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。已知上述晶胞中所有 键键长为rpm,B点钛原子分数坐标为
键键长为rpm,B点钛原子分数坐标为 ,占据氧原子围成的八面体空隙,则A点钛原子的分数坐标为(
,占据氧原子围成的八面体空隙,则A点钛原子的分数坐标为( ,0,
,0,______ )。若 晶体密度为
晶体密度为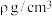 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
______ 。
② 晶体中
晶体中
______ 。
(1)基态Ti原子的价电子轨道表示式是
(2)
 与
与 互为等电子体,
互为等电子体, 与
与 甲基咪唑
甲基咪唑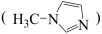 反应可以得到
反应可以得到
 其结构如下图所示。
其结构如下图所示。
①
 分子的空间构型为
分子的空间构型为②
 甲基咪唑分子中碳原子的杂化轨道类型为
甲基咪唑分子中碳原子的杂化轨道类型为 中含有
中含有③
 稳定性比
稳定性比 差,试从化学键角度分析原因:
差,试从化学键角度分析原因:(3)
 属于四方晶系,晶胞棱边夹角均为90°。研究表明,
属于四方晶系,晶胞棱边夹角均为90°。研究表明, 通过氮掺杂反应可生成
通过氮掺杂反应可生成 ,能使
,能使 对可见光具有活性,反应如图所示。
对可见光具有活性,反应如图所示。
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。已知上述晶胞中所有
 键键长为rpm,B点钛原子分数坐标为
键键长为rpm,B点钛原子分数坐标为 ,占据氧原子围成的八面体空隙,则A点钛原子的分数坐标为(
,占据氧原子围成的八面体空隙,则A点钛原子的分数坐标为( ,0,
,0, 晶体密度为
晶体密度为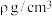 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
②
 晶体中
晶体中
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有属于前四周期的 A、B、C、D、E、F、G 七种元素,原子序数依次增大。A 元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能_______ (填“<”“>”或“=”)B元素的第一电离能,A、B、C三种元素的电负性由小到大的顺序为_______ (用元素符号表示)。
(2)C元素的电子排布图为_______ ;E3+的离子符号为_______ 。
(3)F元素位于元素周期表的_______ 区,其基态原子的电子排布式为_______
(4)G元素可能的性质_______ 。
A.其单质可作为半导体材料 B.其电负性大于磷
C.其原子半径大于锗 D.其第一电离能小于硒
(5)活泼性:D_____ (填“>”或“<”,下同)Al,I1(Mg)_____ I1(Al),其原因是____ 。
 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)A元素的第一电离能
(2)C元素的电子排布图为
(3)F元素位于元素周期表的
(4)G元素可能的性质
A.其单质可作为半导体材料 B.其电负性大于磷
C.其原子半径大于锗 D.其第一电离能小于硒
(5)活泼性:D
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】光伏材料是能将太阳能直接转换成电能的材料,又称太阳能材料,只有半导体材料具有这种功能。可做太阳能电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。请回答下列问题:
(1)已知Ga与B同主族,基态Ga原子的原子结构示意图为________ 。Ga失去电子的逐级电离能(单位:kJ⋅mol⁻¹)的数值依次为577、1984.5、2961.8、6192。由此可推知镓的主要化合价为________ 和+3。
(2)Cd为第48号元素,Cd在元素周期表中的位置为_______ ,电子占据的最高能级的原子轨道的电子云轮廓图为_______ 。
(3)下列事实能说明硫的非金属性比磷强的是_______ (填字母);
A.沸点:PH3<H2S B.稳定性:PH3<H2S C.酸性:H3PO4<H2SO4
从原子结构角度解释硫的非金属性比磷强的原因:_______ 。
(4)与Al在元素周期表中处于对角线的铍,在性质上与Al具有相似性,写出铍的氧化物与氢氧化钠溶液反应生成Na2BeO2的离子方程式________ 。
(5)GaN、GaP、GaAs熔融状态均不导电,它们的晶体结构与金刚石相似,其熔点如下表所示,试分析GaN、GaP、GaAs的熔点依次降低的原因:_______ 。
(1)已知Ga与B同主族,基态Ga原子的原子结构示意图为
(2)Cd为第48号元素,Cd在元素周期表中的位置为
(3)下列事实能说明硫的非金属性比磷强的是
A.沸点:PH3<H2S B.稳定性:PH3<H2S C.酸性:H3PO4<H2SO4
从原子结构角度解释硫的非金属性比磷强的原因:
(4)与Al在元素周期表中处于对角线的铍,在性质上与Al具有相似性,写出铍的氧化物与氢氧化钠溶液反应生成Na2BeO2的离子方程式
(5)GaN、GaP、GaAs熔融状态均不导电,它们的晶体结构与金刚石相似,其熔点如下表所示,试分析GaN、GaP、GaAs的熔点依次降低的原因:
| 物质 | GaN | GaP | GaAs |
| 熔点/℃ | 1700 | 1480 | 1238 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、W、Q、R均为前四周期元素,且原子序数依次增大,其相关信息如下表所示,回答下列问题:
(1)R基态原子的价电子排布图为___________________ ,R在周期表中位于________ 区。
(2)X、Y、Z的第一电离能由大到小的顺序为________ (用元素符号表示)。
(3)Q单质形成的晶体的堆积模型为____________ ,配位数是______ 。
(4)光谱证实单质W与强碱溶液反应有[W(OH)4]-生成,则[W(OH)4]-中存在________ (填字母)。
a.极性共价键 b.非极性共价键 c.配位键 d.σ键 e.π键
| X的基态原子中电子分布在三个不同的能级中且每个能级中电子总数相同 |
| Y元素的气态氢化物与其最高价氧化物对应的水化物能发生化合反应 |
| Z元素的族序数是周期数的三倍 |
| W原子的第一至第六电离能分别为: I1=578 kJ·mol-1 I2=1 817 kJ·mol-1 I3=2 745 kJ·mol-1 I4=11 575 kJ·mol-1 I5=14 830 kJ·mol-1 I6=18 376 kJ·mol-1 |
| Q为前四周期中电负性最小的元素 |
| R位于周期表中的第11列 |
(1)R基态原子的价电子排布图为
(2)X、Y、Z的第一电离能由大到小的顺序为
(3)Q单质形成的晶体的堆积模型为
(4)光谱证实单质W与强碱溶液反应有[W(OH)4]-生成,则[W(OH)4]-中存在
a.极性共价键 b.非极性共价键 c.配位键 d.σ键 e.π键
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表中的六种元素A、B、C、D、E、F,原子序数依次增大。
(1)写出E的基态原子的电子排布式:___________ 。
(2) A、B形成的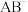 常作为配位化合物中的配体。在
常作为配位化合物中的配体。在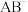 中,元素A的原子采取sp杂化,则A与B形成的化学键中含有的
中,元素A的原子采取sp杂化,则A与B形成的化学键中含有的 键与
键与 键的数目之比为
键的数目之比为___________ 。
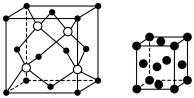
(3)D与E形成的化合物晶体的晶胞如图左所示。在该晶胞中,E离子的数目为___________ ;该化合物的化学式为___________ 。___________ ,F原子的配位数为___________ 。
(5)C的氢化物( )在乙醇中的溶解度大于
)在乙醇中的溶解度大于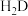 ,其原因是
,其原因是___________ 。
(6)D与C形成的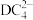 的空间结构为
的空间结构为___________ (用文字描述)。
(7)E、F均能与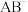 形成配离子,已知
形成配离子,已知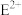 与
与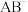 形成配离子时,配位数为4;
形成配离子时,配位数为4;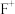 与
与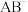 形成配离子时,配位数为2.工业上常用
形成配离子时,配位数为2.工业上常用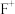 与
与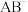 形成的配离子与单质E反应,生成
形成的配离子与单质E反应,生成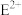 与
与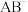 形成的配离子和E单质来提取F,写出上述反应的离子方程式:
形成的配离子和E单质来提取F,写出上述反应的离子方程式:___________ 。
A的基态原子价电子排布为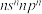 |
| B的基态原子2p能级有3个单电子 |
| C的原子最外层电子数是其内层的3倍 |
| D的基态原子3p轨道上有4个电子 |
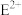 的d轨道中有10个电子 的d轨道中有10个电子 |
| F单质在金属活动性顺序中排在最末位 |
(1)写出E的基态原子的电子排布式:
(2) A、B形成的
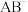 常作为配位化合物中的配体。在
常作为配位化合物中的配体。在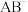 中,元素A的原子采取sp杂化,则A与B形成的化学键中含有的
中,元素A的原子采取sp杂化,则A与B形成的化学键中含有的 键与
键与 键的数目之比为
键的数目之比为(3)D与E形成的化合物晶体的晶胞如图左所示。在该晶胞中,E离子的数目为
(5)C的氢化物(
 )在乙醇中的溶解度大于
)在乙醇中的溶解度大于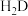 ,其原因是
,其原因是(6)D与C形成的
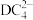 的空间结构为
的空间结构为(7)E、F均能与
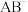 形成配离子,已知
形成配离子,已知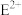 与
与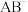 形成配离子时,配位数为4;
形成配离子时,配位数为4;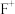 与
与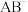 形成配离子时,配位数为2.工业上常用
形成配离子时,配位数为2.工业上常用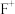 与
与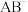 形成的配离子与单质E反应,生成
形成的配离子与单质E反应,生成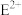 与
与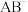 形成的配离子和E单质来提取F,写出上述反应的离子方程式:
形成的配离子和E单质来提取F,写出上述反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硼及其化合物在结构上的复杂性和键型上的多样性,极大地丰富和扩展了现有的共价键理论,因此ⅢA族元素及其化合物在无机化学发展中占有独特的地位。回答:
(1)某同学写出了铝原子的4种不同状态的电子排布图,其中能量最低的是___________ (填字母代号),电子由状态C到状态B所得原子光谱为___________ 光谱(填“发射”或“吸收”)。
A.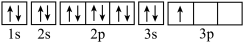 B.
B.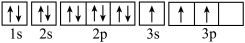
C.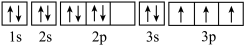 D.
D.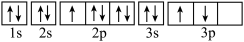
(2)BF3、NF3、CH4的键角由大到小的顺序为___________ 。
(3)BF3可与HF形成HBF4(四氟硼酸),在水中可以部分电离产生H+和BF ,与BF
,与BF 互为等电子体的分子有
互为等电子体的分子有___________ (写一个)。
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:

在Xm-中,硼原子轨道的杂化类型有___________ ;配位键存在于___________ 原子之间(填原子的数字标号);m=___________ (填数字)。
(5)砷化镓属于第三代半导体,晶胞结构与金刚石相似,如图所示。
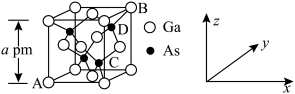
①晶胞中原子坐标参数A为 ,B为
,B为 ,
,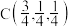 ,则D为
,则D为___________ 。
②阿伏伽德罗常数的值为 ,砷化镓的密度为
,砷化镓的密度为___________  (列出计算式)。
(列出计算式)。
(1)某同学写出了铝原子的4种不同状态的电子排布图,其中能量最低的是
A.
 B.
B.
C.
 D.
D.
(2)BF3、NF3、CH4的键角由大到小的顺序为
(3)BF3可与HF形成HBF4(四氟硼酸),在水中可以部分电离产生H+和BF
 ,与BF
,与BF 互为等电子体的分子有
互为等电子体的分子有(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:

在Xm-中,硼原子轨道的杂化类型有
(5)砷化镓属于第三代半导体,晶胞结构与金刚石相似,如图所示。

①晶胞中原子坐标参数A为
 ,B为
,B为 ,
, ,则D为
,则D为②阿伏伽德罗常数的值为
 ,砷化镓的密度为
,砷化镓的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】铬、钛、钴都属于过渡元素。
(1)铬元素属于周期表的___________ 区,基态Cr原子有___________ 个未成对电子。同周期的基态原子中,与Cr最高能层电子数相同的还有___________ (写元素符号)。
(2)钛元素形成的钛酸钡晶体的晶胞结构如图所示,该晶体经X射线分析得出,重复单元为立方体,顶点位置被Ti4+所占据,体心位置被Ba2+所占据,棱心位置被O2-所占据。___________ 。
②若将Ti4+置于晶胞的体心,Ba2+置于晶胞顶点,则O2-处于立方体的___________ 位置。
③Ti4+的氧配位数和Ba2+的氧配位数分别为___________ 。
(3)钴的某种配合物的化学式为[Co(H2O)6]F2,该配合物的立方晶胞如图所示,其晶胞参数为apm。___________ 个。
②设阿伏加德罗常数的值为NA,则[Co(H2O)6]F2晶体的密度为___________ g·cm-3。
(1)铬元素属于周期表的
(2)钛元素形成的钛酸钡晶体的晶胞结构如图所示,该晶体经X射线分析得出,重复单元为立方体,顶点位置被Ti4+所占据,体心位置被Ba2+所占据,棱心位置被O2-所占据。
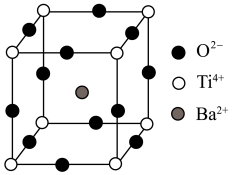
②若将Ti4+置于晶胞的体心,Ba2+置于晶胞顶点,则O2-处于立方体的
③Ti4+的氧配位数和Ba2+的氧配位数分别为
(3)钴的某种配合物的化学式为[Co(H2O)6]F2,该配合物的立方晶胞如图所示,其晶胞参数为apm。
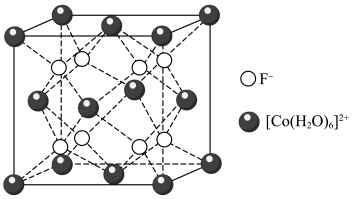
②设阿伏加德罗常数的值为NA,则[Co(H2O)6]F2晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氮的相关化合物在材料等方面有重要用途。回答下列问题:
(1)基态N原子的核外电子排布式为_______ ,第一电离能: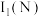
_______ 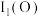 (填“大于”或“小于”)。
(填“大于”或“小于”)。
(2)N及其同族的P、As均可形成类似的氢化物, 、
、 ,
, 的沸点由高到低的顺序为
的沸点由高到低的顺序为_______ (填化学式)。
(3)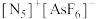 是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为
是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为_______ 。 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有_______ 个,其中提供孤对电子的原子为_______ (写元素符号)。 ,则C点的原子坐标参数为
,则C点的原子坐标参数为_______ 。
②已知晶胞参数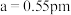 ,则该晶体的密度为
,则该晶体的密度为_______  (用
(用 表示阿伏加德罗常数,只列出计算表达式即可。)
表示阿伏加德罗常数,只列出计算表达式即可。)
(1)基态N原子的核外电子排布式为
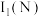
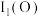 (填“大于”或“小于”)。
(填“大于”或“小于”)。(2)N及其同族的P、As均可形成类似的氢化物,
 、
、 ,
, 的沸点由高到低的顺序为
的沸点由高到低的顺序为(3)
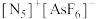 是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为
是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为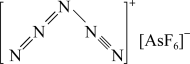
 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有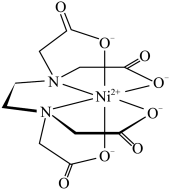

 ,则C点的原子坐标参数为
,则C点的原子坐标参数为②已知晶胞参数
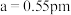 ,则该晶体的密度为
,则该晶体的密度为 (用
(用 表示阿伏加德罗常数,只列出计算表达式即可。)
表示阿伏加德罗常数,只列出计算表达式即可。)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】铜、锌为ds区元素,它们的单质及化合物在工业生产中具有重要的用途。回答下列问题:
(1)基态锌原子占据最高能级的电子云轮廓图为______ 形,基态铜原子的价层电子排布图为______ ,与铜同周期且与铜具有相同未成对电子数目的元素有______ (填元素符号)。
(2)铜的第二电离能______ (填“>”“<”或=”)锌的第二电离能,其主要原因是______ 。
(3)某含铜(Ⅱ)配合物的结构式如图:
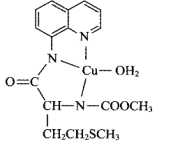
 该配合物中含有
该配合物中含有______  配位键,N原子的杂化方式为
配位键,N原子的杂化方式为______ ,N、O、S中原子半径最大的是______ , 键的共价键类型为
键的共价键类型为 键,则
键,则 键的共价键类型为
键的共价键类型为______ 。
(4)锌单质的晶胞采用六方最密堆积,其晶胞结构如图所示:
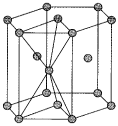
若距离最近的两个Zn原子的核间距为anm,阿伏加德罗常数的值为 ,则Zn晶体的密度为
,则Zn晶体的密度为______  。
。
(1)基态锌原子占据最高能级的电子云轮廓图为
(2)铜的第二电离能
(3)某含铜(Ⅱ)配合物的结构式如图:

 该配合物中含有
该配合物中含有 配位键,N原子的杂化方式为
配位键,N原子的杂化方式为 键的共价键类型为
键的共价键类型为 键,则
键,则 键的共价键类型为
键的共价键类型为(4)锌单质的晶胞采用六方最密堆积,其晶胞结构如图所示:

若距离最近的两个Zn原子的核间距为anm,阿伏加德罗常数的值为
 ,则Zn晶体的密度为
,则Zn晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】[化学一选修3:物质结构与性质]A、B、C、D、E五种元素是周期表中前四周期的元素。只有A、B、C为金属且同周期,原子序数A<B<C。A、C核外均没有未成对电子;B原子核外有二个未成对电子和三个空轨道。D原子最外层电子数是其周期序数的三倍。E能与D形成化合物ED2,可用于自来水的消毒。
(1)C的基态原子的价层电子排布式为_____ ;D和E的电负性大小关系为____ (用元素符号表示)。
(2)化合物E2D分子的空间构型为____________________ ,中心原子采用_____________ 杂化。E与D还可形成三角锥结构的阴离子,该离子的化学式为_______ ,任意写出一种它的等电子体的化学式为____________ 。
(3)B与E能形成一种化合物BE4,其熔点:-25℃,沸点:l 36.4℃。则该化合物属于____ 晶体,晶体内含有的作用力类型有__________ 。
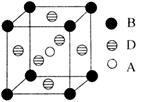
(4)A、B、D三种元素形成的某晶体的晶胞结构如图,则晶体的化学式为______ 。若最近的B与D的原子距离为a cm,该物质的摩尔质量为M g/mol,阿伏加德罗常数的数值为NA,则该晶体的密度为_________ g/cm3。
(1)C的基态原子的价层电子排布式为
(2)化合物E2D分子的空间构型为
(3)B与E能形成一种化合物BE4,其熔点:-25℃,沸点:l 36.4℃。则该化合物属于
(4)A、B、D三种元素形成的某晶体的晶胞结构如图,则晶体的化学式为

您最近一年使用:0次



