I、钢铁中加入少量镍铬等元素可制成不锈钢,东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是______________________ 。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为_________ ,提供孤电子对的成键原子是________ 。
(2)铁元素有变价,试根据原子核外电子排布所遵循的原理解释Fe2+具有较强的还原性,易被氧化为Fe3+的原因______________________________ 。
(3)普鲁士蓝(Prussian Blue),即亚铁氰化铁,化学式Fe4[Fe(CN)6]3是一种配合物,其中含有的化学键有____________________ ;
a.共价键 b.离子键 c.配位键 d.金属键 e.氢键
II、钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为2Mn2++5S2O82−+8H2O=2MnO4−+10SO42−+16H+
(4)写出基态锰原子的价电子排布的轨道表示式:________________ 。
(5)已知H2S2O8的结构如图:

①H2S2O8硫原子的轨道杂化方式为________________ 。
②上述反应每生成2 mol MnO4−,S2O82−断裂的共价键数目为_________ 。
③上述反应中被还原的元素为________________ 。
(1)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为
(2)铁元素有变价,试根据原子核外电子排布所遵循的原理解释Fe2+具有较强的还原性,易被氧化为Fe3+的原因
(3)普鲁士蓝(Prussian Blue),即亚铁氰化铁,化学式Fe4[Fe(CN)6]3是一种配合物,其中含有的化学键有
a.共价键 b.离子键 c.配位键 d.金属键 e.氢键
II、钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为2Mn2++5S2O82−+8H2O=2MnO4−+10SO42−+16H+
(4)写出基态锰原子的价电子排布的轨道表示式:
(5)已知H2S2O8的结构如图:

①H2S2O8硫原子的轨道杂化方式为
②上述反应每生成2 mol MnO4−,S2O82−断裂的共价键数目为
③上述反应中被还原的元素为
更新时间:2019-04-25 14:32:38
|
相似题推荐
【推荐1】碳是形成化合物种类最多的元素。
(1)CH2=CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为________ (填最简整数比),写出该分子中所有碳原子的杂化方式:________________ 。
(2)乙醇(CH3CH2OH)和二甲醚(CH3OCH3)的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是_______________________________ 。
(3)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为________________ 。
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。如图所示为碳化硅的晶胞(其中 为碳原子,
为碳原子, 为硅原子)。
为硅原子)。
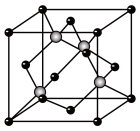
每个碳原子周围与其距离最近的硅原子有________ 个。
(5)写出下列物质的的电子式:①NaOH_____________ ②CO2___________
(1)CH2=CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为
(2)乙醇(CH3CH2OH)和二甲醚(CH3OCH3)的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是
(3)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。如图所示为碳化硅的晶胞(其中
 为碳原子,
为碳原子, 为硅原子)。
为硅原子)。
每个碳原子周围与其距离最近的硅原子有
(5)写出下列物质的的电子式:①NaOH
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】化合物G属于黄酮醋酸类化合物,具有保肝的作用。一种合成化合物G的路线如下:
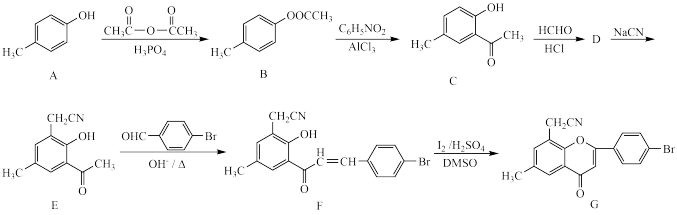
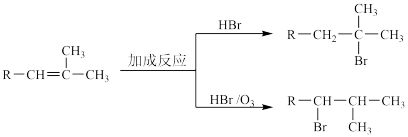
已知:烯烃与HBr发生加成时,不同的条件下有不同的反应方式:
(1)1 mol B分子中含有的σ键数目为_______ 。
(2)E→F分两步进行,反应类型依次为_______ 、_______ 。
(3)D的分子是C10H11O2Cl,D的结构简式为_______ 。
(4)E的一种同分异构体X同时符合下列条件。写出X的结构简式:_______ 。
Ⅰ.能使溴的CCl4溶液褪色,且消耗2 mol Br2
Ⅱ.分子中含3种化学环境不同的氢
(5)设计由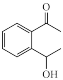 为原料,制备
为原料,制备 的合成路线(无机试剂和有机溶剂任选)
的合成路线(无机试剂和有机溶剂任选) _______ 。

已知:烯烃与HBr发生加成时,不同的条件下有不同的反应方式:

(1)1 mol B分子中含有的σ键数目为
(2)E→F分两步进行,反应类型依次为
(3)D的分子是C10H11O2Cl,D的结构简式为
(4)E的一种同分异构体X同时符合下列条件。写出X的结构简式:
Ⅰ.能使溴的CCl4溶液褪色,且消耗2 mol Br2
Ⅱ.分子中含3种化学环境不同的氢
(5)设计由
 为原料,制备
为原料,制备 的合成路线(无机试剂和有机溶剂任选)
的合成路线(无机试剂和有机溶剂任选)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】元素Fe、Ni、C等形成的各种合金在工业、生活、国防中有很大的作用。
(1)Ni在元素周期表中的位置为________ 。
(2)元素铜与镍的第二电离能:ICu_____ (填“> ”或“< ”)INi,原因是_______ 。
(3)二茂铁是种含铁的有机化合物,其化学式为Fe(C5H5)2,可看作是Fe2+与两个正五边形的环戊二烯负离子(C5H )配体形成的夹心型分子(如图所示),熔点为173℃ (在100 ℃时开始升华),沸点为249 ℃。
)配体形成的夹心型分子(如图所示),熔点为173℃ (在100 ℃时开始升华),沸点为249 ℃。
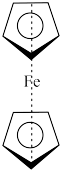
①二茂铁的晶体类型是____ ;1 mol环戊二烯( )分子中含
)分子中含______ molσ键。
②结合二茂铁的结构,预测二茂铁在水中的溶解性并说明理由:________ 。
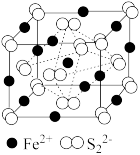
(4)FeS2晶体的晶胞结构如图所示,设晶胞边长为a nm,FeS2的相对分子质量为M,阿伏加 德罗常数的值为NA,则其晶体密度的计算表达式为____________ g·cm-3。
(1)Ni在元素周期表中的位置为
(2)元素铜与镍的第二电离能:ICu
(3)二茂铁是种含铁的有机化合物,其化学式为Fe(C5H5)2,可看作是Fe2+与两个正五边形的环戊二烯负离子(C5H
 )配体形成的夹心型分子(如图所示),熔点为173℃ (在100 ℃时开始升华),沸点为249 ℃。
)配体形成的夹心型分子(如图所示),熔点为173℃ (在100 ℃时开始升华),沸点为249 ℃。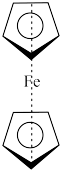
①二茂铁的晶体类型是
 )分子中含
)分子中含②结合二茂铁的结构,预测二茂铁在水中的溶解性并说明理由:
(4)FeS2晶体的晶胞结构如图所示,设晶胞边长为a nm,FeS2的相对分子质量为M,阿伏加 德罗常数的值为NA,则其晶体密度的计算表达式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】物质结构与性质]单质铁、锂、砷及它们的化合物广泛应用于超导体材料等领域,回答下列问题:
(1)Fe原子的核外电子排布式为[Ar]_______ ,Li原子核外占据最高能层电子的电子云轮廓图形状为_______ 。
(2)As 的卤化物的熔点如下:
表中卤化物熔点差异的原因是_______ ,AsCl3分子的立体构型为_______ 。
(3)铁、锂、砷形成的化合物LiFeAs是一种超导体,其晶胞结构如图1所示,已知立方晶胞参数acm,则该晶体的密度是_______ g/cm3(用含a、NA的式子表示)。
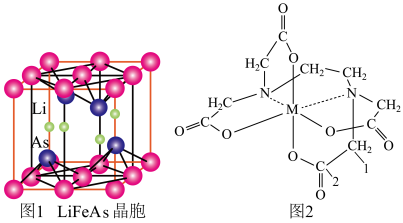
(4)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图2所示,图中M代表Fe3+。则1号碳原子有_______ 个σ键,2号碳原子采取_______ 杂化方式;Fe3+与氮原子之间形成的化学键是_______ ,Fe3+的配位数为_______ ;该配合物中,第二周期的三种元素的第一电离能由大到小的顺序为_______ 。
(1)Fe原子的核外电子排布式为[Ar]
(2)As 的卤化物的熔点如下:
AsCl3 | AsBr3 | AsI3 | |
熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是
(3)铁、锂、砷形成的化合物LiFeAs是一种超导体,其晶胞结构如图1所示,已知立方晶胞参数acm,则该晶体的密度是

(4)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图2所示,图中M代表Fe3+。则1号碳原子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)分子中含有两个或两个以上中心原子(离子)的配合物称为多核配合物,如图为Co (II)双核配合物的内界。

①元素Co位于元素周期表中_______ 区,其基态原子次外层电子的运动状态有_______
种。
②下列状态的钴中,失去一个电子所需能量最大的是_______ (填序号)。
A.[Ar]3d74s2 B.[Ar]3d74s1 C.[Ar]3d74s14p1 D.[Ar]3d74p1
③配合物中每个中心离子的配位数为_______ 。
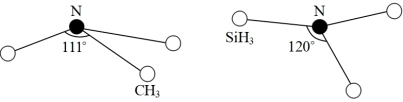
④由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物结构和性质存在较大差异。化合物N(CH3)3(三角锥形)和N(SiH3)3 (平面形)的结构如图所示,则N(SiH3)3中N的杂化方式为_______ ,更易形成配合物的是_______ 。
(2)①有机物甲醛是居室中常见的污染物之一,其结构为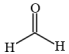 ,其中H—C—H间的键角略小于120°,原因是
,其中H—C—H间的键角略小于120°,原因是_______ 。
②离子化合物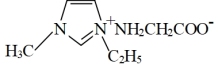 常温下为液态而非固态,原因是
常温下为液态而非固态,原因是_______ 。
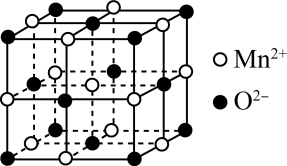
(3)一氧化锰在医药、冶炼上应用广泛,其立方晶胞如图所示,晶胞中距离最近的两个O2-之间的距离为a pm, MnO晶体的密度为ρg·cm-3,则阿伏加德罗常数的值为_______ (用含a和ρ的代数式表示)。
(1)分子中含有两个或两个以上中心原子(离子)的配合物称为多核配合物,如图为Co (II)双核配合物的内界。

①元素Co位于元素周期表中
种。
②下列状态的钴中,失去一个电子所需能量最大的是
A.[Ar]3d74s2 B.[Ar]3d74s1 C.[Ar]3d74s14p1 D.[Ar]3d74p1
③配合物中每个中心离子的配位数为
④由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物结构和性质存在较大差异。化合物N(CH3)3(三角锥形)和N(SiH3)3 (平面形)的结构如图所示,则N(SiH3)3中N的杂化方式为

(2)①有机物甲醛是居室中常见的污染物之一,其结构为
 ,其中H—C—H间的键角略小于120°,原因是
,其中H—C—H间的键角略小于120°,原因是②离子化合物
 常温下为液态而非固态,原因是
常温下为液态而非固态,原因是(3)一氧化锰在医药、冶炼上应用广泛,其立方晶胞如图所示,晶胞中距离最近的两个O2-之间的距离为a pm, MnO晶体的密度为ρg·cm-3,则阿伏加德罗常数的值为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】材料是生物医疗、国防军事以及航空航天等领域发展提供支撑。
(1)磷酸亚铁锂( )常用作锂离子电池正极材料,周期表中与Li的化学性质最相似的邻族元素是
)常用作锂离子电池正极材料,周期表中与Li的化学性质最相似的邻族元素是_______ (填元素符号),该元素基态原子核外M层电子自旋状态_______ (填“相同”或“相反”);
(2)苯胺(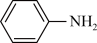 )常作为合成原料,与甲苯(
)常作为合成原料,与甲苯(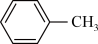 )相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ ;
(3)反应 的产物分子中采取
的产物分子中采取 杂化的原子是
杂化的原子是_______ (填元素名称):
(4) 是制备氟磺酸类化合物的常用原料,分子结构如图所示:
是制备氟磺酸类化合物的常用原料,分子结构如图所示:
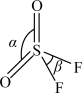
已知键角α为124°,β为96°,则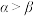 的原因主要是
的原因主要是_______ ;
(5)第三代硅太阳能电池以铜钢镓硒CiGs(CIS中掺入Ga)等化合物为主要材料。Cu晶体的晶胞如图,其配位数为_______ ;
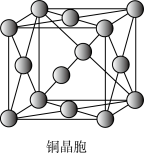
往 溶液中加入过量氨水,可生成
溶液中加入过量氨水,可生成 ,下列说法正确的是
,下列说法正确的是_______ ;
A. 中所含的化学键有离子键、极性键和配位键
中所含的化学键有离子键、极性键和配位键
B.在 中
中 给出孤电子对,
给出孤电子对, 提供空轨道
提供空轨道
C. 组成元素中第一电离能最大的是氧元素
组成元素中第一电离能最大的是氧元素
D. 与
与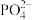 互为等电子体,空间构型均为正四面体形
互为等电子体,空间构型均为正四面体形
(6) 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
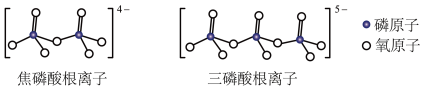
这类磷酸根离子的化学式可用通式表示为_______ (用n代表P原子数)。
(1)磷酸亚铁锂(
 )常用作锂离子电池正极材料,周期表中与Li的化学性质最相似的邻族元素是
)常用作锂离子电池正极材料,周期表中与Li的化学性质最相似的邻族元素是(2)苯胺(
 )常作为合成原料,与甲苯(
)常作为合成原料,与甲苯( )相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(3)反应
 的产物分子中采取
的产物分子中采取 杂化的原子是
杂化的原子是(4)
 是制备氟磺酸类化合物的常用原料,分子结构如图所示:
是制备氟磺酸类化合物的常用原料,分子结构如图所示:
已知键角α为124°,β为96°,则
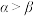 的原因主要是
的原因主要是(5)第三代硅太阳能电池以铜钢镓硒CiGs(CIS中掺入Ga)等化合物为主要材料。Cu晶体的晶胞如图,其配位数为

往
 溶液中加入过量氨水,可生成
溶液中加入过量氨水,可生成 ,下列说法正确的是
,下列说法正确的是A.
 中所含的化学键有离子键、极性键和配位键
中所含的化学键有离子键、极性键和配位键B.在
 中
中 给出孤电子对,
给出孤电子对, 提供空轨道
提供空轨道C.
 组成元素中第一电离能最大的是氧元素
组成元素中第一电离能最大的是氧元素D.
 与
与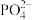 互为等电子体,空间构型均为正四面体形
互为等电子体,空间构型均为正四面体形(6)
 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
这类磷酸根离子的化学式可用通式表示为
您最近一年使用:0次
【推荐1】钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为___________ ;K、F、Zn的电负性从大到小的顺序为___________ 。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是_______________ 。
(3)OF2分子的几何构型为___________ ,中心原子的杂化类型为___________ 。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在___________ ;与O3-互为等电子体的分子为___________ (任 写一种 )。
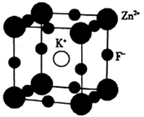
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。
①晶胞中Zn2+的配位数为___________ 个。
②晶胞中紧邻的两个F-间的距离为_______________________ (列出算式即可)nm。
③该晶体的密度为___________ (列出算式即可,用NA表示阿伏伽德罗常数的数值)g·cm-3。
(1)基态锌原子的价电子排布式为
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是
(3)OF2分子的几何构型为
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。

①晶胞中Zn2+的配位数为
②晶胞中紧邻的两个F-间的距离为
③该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】S、Se 、N、Fe等元素及其化合物在科学研究和工业生产中具有重要的作用。
(1)臭鼬排放的臭气主要成分为3﹣MBT,键线式如图所示:

0.1mol 3﹣MBT中含有σ键数目为___________ (NA为阿伏加德罗常数的值)。3﹣MBT的沸点低于(CH3)2C=CHCH2OH,主要原因是___________ 。
(2)2020年12月17日,采撷月壤的嫦娥五号荣耀归来。嫦娥五号探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质。硒为第四周期第VIA族元素,其氧化物有SeO2和SeO3两种,SeO3分子的立体构型为___________ ,与其互为等电子体的阴离子为 ___________ (举一例)。
(3)铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业,其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
①K3[Fe(CN)6]中所涉及的各元素的第一电离能由大到小的顺序为___________ 。
②(CN)2分子中存在碳碳键,C原子的杂化轨道类型为___________ 。
③下列选项是部分同学画的基态氮原子的核外电子排布图,其中违背泡利原理的是___________ (填序号,下同),违背洪特规则的是___________ 。
A.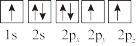 B.
B. 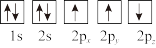 C.
C. 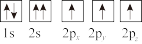
(4)如图是金属铁晶体中的一个晶胞。
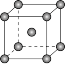
①该晶体中原子总体积占晶体体积的比值为___________ (用含π的最简代数式表示)。
②铁原子的半径为rpm,其晶体密度为___________ g•cm﹣3(用含有r、NA的最简代数式表示)。
(1)臭鼬排放的臭气主要成分为3﹣MBT,键线式如图所示:

0.1mol 3﹣MBT中含有σ键数目为
(2)2020年12月17日,采撷月壤的嫦娥五号荣耀归来。嫦娥五号探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质。硒为第四周期第VIA族元素,其氧化物有SeO2和SeO3两种,SeO3分子的立体构型为
(3)铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业,其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
①K3[Fe(CN)6]中所涉及的各元素的第一电离能由大到小的顺序为
②(CN)2分子中存在碳碳键,C原子的杂化轨道类型为
③下列选项是部分同学画的基态氮原子的核外电子排布图,其中违背泡利原理的是
A.
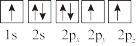 B.
B. 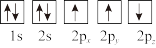 C.
C. 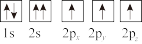
(4)如图是金属铁晶体中的一个晶胞。

①该晶体中原子总体积占晶体体积的比值为
②铁原子的半径为rpm,其晶体密度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】柠檬酸亚铁(FeC6H6O7)是一种易被人体吸收的高效铁制剂,医疗上可以用来治疗缺铁性贫血。某课题组以硫铁矿烧渣(含Fe2O3、SiO2、少量Al2O3等)为原料,先制备碳酸亚铁,再与柠檬酸反应可以制得柠檬酸亚铁。其工艺流程如下:
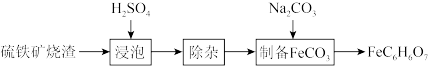
已知:相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算):
(1)“浸泡”时加入过量硫酸的目的:___________ 。
(2)“除杂”时有同学提出下列两种途径,请选择较合理的途径并说明理由___________ 。
途径一:
途径二: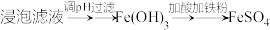
(3)“制备FeCO3”时,Na2CO3溶液的浓度对沉淀中铁元素的质量分数以及FeCO3产率的影响如下图:
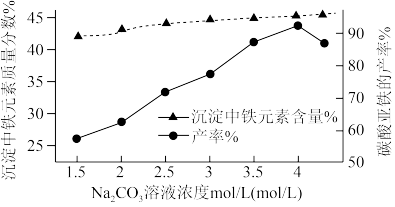
Na2CO3溶液的浓度大于4mol/L时,FeCO3的产率有所下降,而沉淀中铁元素质量分数仍在上升的原因是:___________ 。
(4)在水溶液里,铁氰化钾K3[Fe(CN)6]与FeSO4生成蓝色沉淀,常用于Fe2+的检验。
①HCN分子、SO 离子的空间构型分别为
离子的空间构型分别为___________ 、___________ 。
②基态Fe3+的价电子排布图为___________ 。
③组成K3[Fe(CN)6]的各元素电负性由大到小的次序是___________ 。
④1mol铁氰化钾中σ键的数目为___________ mol。
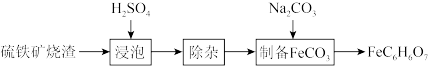
已知:相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算):
| 金属离子 | 沉淀开始pH | 沉淀完全pH |
| Al3+ | 3.1 | 5.1 |
| Fe2+ | 5.9 | 6.9 |
| Fe3+ | 1.2 | 3.2 |
(2)“除杂”时有同学提出下列两种途径,请选择较合理的途径并说明理由
途径一:

途径二:
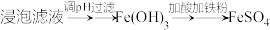
(3)“制备FeCO3”时,Na2CO3溶液的浓度对沉淀中铁元素的质量分数以及FeCO3产率的影响如下图:

Na2CO3溶液的浓度大于4mol/L时,FeCO3的产率有所下降,而沉淀中铁元素质量分数仍在上升的原因是:
(4)在水溶液里,铁氰化钾K3[Fe(CN)6]与FeSO4生成蓝色沉淀,常用于Fe2+的检验。
①HCN分子、SO
 离子的空间构型分别为
离子的空间构型分别为②基态Fe3+的价电子排布图为
③组成K3[Fe(CN)6]的各元素电负性由大到小的次序是
④1mol铁氰化钾中σ键的数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钠和氯及其相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素钠的焰色反应呈黄色,其中黄色对应的辐射波长为_______ nm(填标号)。
A.404.4 B.550.5 C.588.8 D.600.6 E.720.5
(2)基态Na原子中,核外电子占据的最高能层的符号是_________ ,占据该能层电子的电子云轮廓图形状为___________ ,钠元素基态原子的电子排布式为___________ 。Na和Al属于同一周期,但金属Na的熔点、沸点等都比金属Al低,原因是___________________________ 。
(3)氯、硫、磷的电负性由大到小顺序为______ (用元素符号表示);COCl2分子的空间构型为______ 。
(4) 的中心氯原子的杂化轨道类型为
的中心氯原子的杂化轨道类型为_________ ,写出 一种等电子体的化学式
一种等电子体的化学式_________ 。
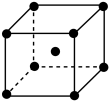
(5)钠单质的晶体结构为体心立方堆积,假设晶胞的棱长为a cm,钠的密度为ρ g/cm3,阿伏伽德罗常数为NA,则晶胞中距离最近的两个钠原子之间的距离为_______ cm(用ρ和NA表示)。
(1)元素钠的焰色反应呈黄色,其中黄色对应的辐射波长为
A.404.4 B.550.5 C.588.8 D.600.6 E.720.5
(2)基态Na原子中,核外电子占据的最高能层的符号是
(3)氯、硫、磷的电负性由大到小顺序为
(4)
 的中心氯原子的杂化轨道类型为
的中心氯原子的杂化轨道类型为 一种等电子体的化学式
一种等电子体的化学式(5)钠单质的晶体结构为体心立方堆积,假设晶胞的棱长为a cm,钠的密度为ρ g/cm3,阿伏伽德罗常数为NA,则晶胞中距离最近的两个钠原子之间的距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,请回答下列问题
(1)基态B原子的电子排布式为_________ ;B和N相比,电负性较大的是_________ ,BN中B元素的化合价为_________ ;
(2)在BF3分子中,F-B-F的键角是_______ ,B原子的杂化轨道类型为_______ ,BF3和过量NaF作用可生成NaBF4,BF4-的立体结构为_______ ;
(3)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________ ,层间作用力为________ ;
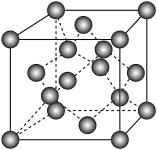
(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有______ 各氮原子、________ 各硼原子,立方氮化硼的密度是_______ g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
(1)基态B原子的电子排布式为
(2)在BF3分子中,F-B-F的键角是
(3)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为
(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】铜是人类知道最早的金属之一,也是广泛使用的第一种金属。回答下列问题:
(1)镍白铜(铜镍合金)可用于制作仿银饰品。第二电离能I2(Cu)___________ (填“>”或“<”)I2(Ni),其原因为___________ 。
(2)向[Cu(NH3)2]Cl溶液中通入乙炔(C2H2)气体,可生成红棕色沉淀Cu2C2。
①C2H2分子中σ键与π键的数目之比为___________ ;碳原子的杂化方式为___________ ;
②写出与Cu2C2中阴离子C 互为等电子体的一种分子:
互为等电子体的一种分子:___________ 。
(3)乙二胺(H2N-CH2CH2-NH2)易与Cu2+形成络合物,用于Cu2+的定量测定。
①形成的络合物中提供孤对电子的原子为___________ (填元素符号)。
②乙二胺中所含元素的电负性由大到小的顺序为___________ 。
(4)铜与氧构成的某种化合物的立方晶胞如图甲所示,图乙是沿晶胞对角面取得的截图,晶胞中所有原子均在对角面上。氧原子的配位数为___________ ,若Cu原子之间最短距离为dpm,阿伏加德罗常数的值为NA,该晶体的密度为___________ g•cm-3(列出计算式即可)。

(1)镍白铜(铜镍合金)可用于制作仿银饰品。第二电离能I2(Cu)
(2)向[Cu(NH3)2]Cl溶液中通入乙炔(C2H2)气体,可生成红棕色沉淀Cu2C2。
①C2H2分子中σ键与π键的数目之比为
②写出与Cu2C2中阴离子C
 互为等电子体的一种分子:
互为等电子体的一种分子:(3)乙二胺(H2N-CH2CH2-NH2)易与Cu2+形成络合物,用于Cu2+的定量测定。
①形成的络合物中提供孤对电子的原子为
②乙二胺中所含元素的电负性由大到小的顺序为
(4)铜与氧构成的某种化合物的立方晶胞如图甲所示,图乙是沿晶胞对角面取得的截图,晶胞中所有原子均在对角面上。氧原子的配位数为

您最近一年使用:0次



