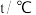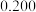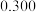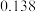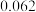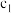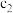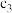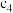可逆反应:2NO2(g) 2NO(g)+O2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是
2NO(g)+O2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是___
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态 ⑦混合气体的平均相对分子质量不再改变的状态
 2NO(g)+O2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是
2NO(g)+O2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态 ⑦混合气体的平均相对分子质量不再改变的状态
更新时间:2019-04-29 17:05:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=___________ 。平衡时H2的转化率为___________ %。
(2)平衡后,若提高H2的转化率,可以采取的措施有___________。
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)  2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
①试比较K1、K2的大小,K1___________ K2(填“<”“>”或“=”);
②400℃时,反应2NH3(g) N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为___________ 。当测得NH3、N2和H2物质的量分别为3mol、2mol和1mol时,则该反应的v(N2)正___________ v(N2)逆(填“<”“>”或“=”)。
③下列可用于判断N2(g)+3H2(g) 2NH3(g)反应达到平衡状态的依据是
2NH3(g)反应达到平衡状态的依据是___________ 。
A.容器中气体压强不再变化
B.容器中气体的密度不再变化
C.容器中气体平均摩尔质量不再变化
D.3v(H2) 正=2v(NH3) 逆
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g)
 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=(2)平衡后,若提高H2的转化率,可以采取的措施有___________。
| A.加了催化剂 | B.增大容器体积 |
| C.降低反应体系的温度 | D.加入一定量N2 |
 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1
②400℃时,反应2NH3(g)
 N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为③下列可用于判断N2(g)+3H2(g)
 2NH3(g)反应达到平衡状态的依据是
2NH3(g)反应达到平衡状态的依据是A.容器中气体压强不再变化
B.容器中气体的密度不再变化
C.容器中气体平均摩尔质量不再变化
D.3v(H2) 正=2v(NH3) 逆
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】一定温度下,在容积为1L的密闭容器内放入2molN2O4和8molNO2,发生如下反应:2NO2(红棕色) N2O4(无色)( ΔH<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
N2O4(无色)( ΔH<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:

(1)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率:___________ mol·L-1·s-1
(2)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:___________
(3)t1时,正反应速率___________ (填“>”、“<”或“=”)逆反应速率
(4)维持容器的温度不变,若缩小容器的体积,则平衡向___________ 移动(填“正反应方向”、“逆反应方向”或“不移动”)
(5)维持容器的体积不变,升高温度,达到新平衡时体系的颜色___________ (填“变深”、“变浅”或“不变”)
 N2O4(无色)( ΔH<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
N2O4(无色)( ΔH<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
(1)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率:
(2)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:
(3)t1时,正反应速率
(4)维持容器的温度不变,若缩小容器的体积,则平衡向
(5)维持容器的体积不变,升高温度,达到新平衡时体系的颜色
您最近一年使用:0次
【推荐3】在1.0 L真空密闭容器中充入4.0 mol A(g)和4.0 mol B(g),在一定温度下进行反应:A(g)+B(g) C(g) ΔH,测得不同时刻该容器内物质的物质的量如下表,回答下列问题:
C(g) ΔH,测得不同时刻该容器内物质的物质的量如下表,回答下列问题:
(1)随着温度的升高,该反应的化学平衡常数减小,则 ΔH______ (填“>”“<”或“=”)0,反应从起始到20 min内C的平均反应速率是_______ 。
(2)该温度下,上述反应的化学平衡常数为________ 。
(3)下列选项中能说明该反应在一定温度和恒容条件下达到平衡状态的是________ 。
A.反应速率:vA(正)+vB(正)=vC(逆) B.A的质量不再改变
C.B的转化率不再改变 D.密度不再改变
(4)若反应C(g) A(g)+B(g)进行时需加入稀释剂X气体(不参与反应),则C的平衡转化率与体系的温度、压强、X的物质的量的关系如图1、图2所示。
A(g)+B(g)进行时需加入稀释剂X气体(不参与反应),则C的平衡转化率与体系的温度、压强、X的物质的量的关系如图1、图2所示。

①由图1可知,T1____ T2(填“>”“<”或“=”)。
②由图2可知,当其他条件不变时,增大X的物质的量,C的平衡转化率将______ (填“增大”“减小”或“不变”)。
 C(g) ΔH,测得不同时刻该容器内物质的物质的量如下表,回答下列问题:
C(g) ΔH,测得不同时刻该容器内物质的物质的量如下表,回答下列问题:| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(A)/mol | 4.0 | 2.5 | 1.5 | n2 | n3 |
| n(C)/mol | 0 | 1.5 | n1 | 3 | 3 |
(2)该温度下,上述反应的化学平衡常数为
(3)下列选项中能说明该反应在一定温度和恒容条件下达到平衡状态的是
A.反应速率:vA(正)+vB(正)=vC(逆) B.A的质量不再改变
C.B的转化率不再改变 D.密度不再改变
(4)若反应C(g)
 A(g)+B(g)进行时需加入稀释剂X气体(不参与反应),则C的平衡转化率与体系的温度、压强、X的物质的量的关系如图1、图2所示。
A(g)+B(g)进行时需加入稀释剂X气体(不参与反应),则C的平衡转化率与体系的温度、压强、X的物质的量的关系如图1、图2所示。
①由图1可知,T1
②由图2可知,当其他条件不变时,增大X的物质的量,C的平衡转化率将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硅是重要的半导体材料,是构成现代电子工业的基础。硅及其化合物在工业中应用广泛,在工业上,高纯硅可以通过下列流程制取:
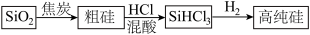
完成下列填空:
(1)氯原子核外有_______ 种不同能量的电子,硅原子的核外电子排布式是_______________ 。
(2)碳与硅属于同主族元素,熔沸点SiO2________ CO2 (填写“>”、“<”或“=”),其原因是_____________________________________________________ 。
(3)流程中由SiO2制粗硅的反应不能说明碳的非金属性强于硅,原因是_________________ ;请写出一个能说明碳的非金属性强于硅的化学方程式______________________________ 。
(4)SiHCl3(g) + H2(g) Si(s) + 3HCl(g) -Q (Q>0)
Si(s) + 3HCl(g) -Q (Q>0)
①上述反应的平衡常数表达式K=_____________ ;能使K增大的措施是_______________ 。
②一定条件下,在固定容积的密闭容器中,能表示上述反应达到平衡状态的是________ (选填编号)。
a.3v逆(SiHCl3)=v正(HCl) b.混合气体的压强不变
c.K保持不变 d.c(SiHCl3)∶c(H2)∶c(HCl)=1∶1∶3
③一定温度下,在2L密闭容器中进行上述反应,5min后达到平衡,此过程中固体质量增加0.28g,此时HCl的化学反应速率为________________ 。

完成下列填空:
(1)氯原子核外有
(2)碳与硅属于同主族元素,熔沸点SiO2
(3)流程中由SiO2制粗硅的反应不能说明碳的非金属性强于硅,原因是
(4)SiHCl3(g) + H2(g)
 Si(s) + 3HCl(g) -Q (Q>0)
Si(s) + 3HCl(g) -Q (Q>0)①上述反应的平衡常数表达式K=
②一定条件下,在固定容积的密闭容器中,能表示上述反应达到平衡状态的是
a.3v逆(SiHCl3)=v正(HCl) b.混合气体的压强不变
c.K保持不变 d.c(SiHCl3)∶c(H2)∶c(HCl)=1∶1∶3
③一定温度下,在2L密闭容器中进行上述反应,5min后达到平衡,此过程中固体质量增加0.28g,此时HCl的化学反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是( ) (填序号)
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。
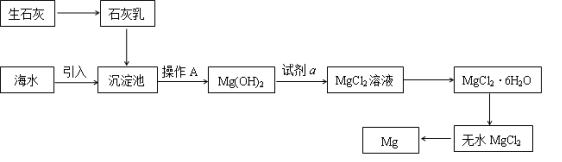
①操作A是_______________________ 。
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为____________________________ 。
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?_____________________________________________ 。
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是( ) (填序号)
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式________________________________ 。
③用CCl4提取碘时除了用CCl4还可以选用的试剂是( ) (填字母序号)
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:________ 。
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为__________________ 。
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
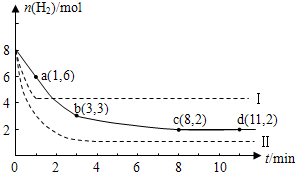
①a点正反应速率_________ (填“大于、等于或小于”)a点逆反应速率。
②平衡时CO2的物质的量浓度是___________ mol/L。
③能够说明该反应达到化学平衡状态的标志是_______ (双选)。
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
(1)无需经过化学变化就能从海水中获得的物质是
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。

①操作A是
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
③用CCl4提取碘时除了用CCl4还可以选用的试剂是
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
①a点正反应速率
②平衡时CO2的物质的量浓度是
③能够说明该反应达到化学平衡状态的标志是
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
您最近一年使用:0次
【推荐3】在一个固定容积的密闭容器中,有如下反应: △H=QkJ/mol,其化学平衡常数K和温度t的关系如下
△H=QkJ/mol,其化学平衡常数K和温度t的关系如下
(1)下列各项能判断该反应已达到化学平衡状态的是______ 。
a.容器中压强不变 b.△H不变 c.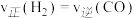 d.CO的质量分数不变
d.CO的质量分数不变
(2)在 时,可逆反应
时,可逆反应 在固定容积的密闭容器中进行,容器内各物质的浓度
在固定容积的密闭容器中进行,容器内各物质的浓度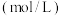 变化如下表:
变化如下表:
 计算:
计算: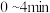 时,
时, 的转化率
的转化率
_____ 。
 表中
表中 之间数值发生变化,可能的原因是
之间数值发生变化,可能的原因是______ 。
(3)在723K时,将 和
和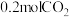 通入抽空的1L恒容密闭容器中,发生如下反应:
通入抽空的1L恒容密闭容器中,发生如下反应:  ,反应达平衡后,水的物质的量分数为
,反应达平衡后,水的物质的量分数为 。
。
 的平衡转化率等于
的平衡转化率等于_______ ,反应平衡常数K等于_____  保留两位有效数字
保留两位有效数字 。
。
 再向容器中加入过量的
再向容器中加入过量的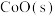 和
和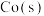 ,则容器中又会增加如下平衡:
,则容器中又会增加如下平衡: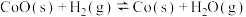 K1,
K1,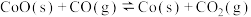 K2,最后反应达平衡时,容器中水的物质的量分数为
K2,最后反应达平衡时,容器中水的物质的量分数为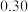 ,则K1等于
,则K1等于______ 。
 △H=QkJ/mol,其化学平衡常数K和温度t的关系如下
△H=QkJ/mol,其化学平衡常数K和温度t的关系如下
| 700 | 800 | 850 | 1000 | 1200 |
K | 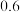 |  |  | 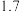 |  |
(1)下列各项能判断该反应已达到化学平衡状态的是
a.容器中压强不变 b.△H不变 c.
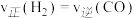 d.CO的质量分数不变
d.CO的质量分数不变(2)在
 时,可逆反应
时,可逆反应 在固定容积的密闭容器中进行,容器内各物质的浓度
在固定容积的密闭容器中进行,容器内各物质的浓度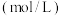 变化如下表:
变化如下表:时间 | CO |
|
|
|
0 |
|
| 0 | 0 |
2 |
|
|
|
|
3 |
|
|
|
|
4 |
|
|
|
|
5 |
|
|
| |
6 |
|
|
|
 计算:
计算: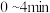 时,
时, 的转化率
的转化率
 表中
表中 之间数值发生变化,可能的原因是
之间数值发生变化,可能的原因是(3)在723K时,将
 和
和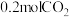 通入抽空的1L恒容密闭容器中,发生如下反应:
通入抽空的1L恒容密闭容器中,发生如下反应:  ,反应达平衡后,水的物质的量分数为
,反应达平衡后,水的物质的量分数为 。
。 的平衡转化率等于
的平衡转化率等于 保留两位有效数字
保留两位有效数字 。
。 再向容器中加入过量的
再向容器中加入过量的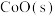 和
和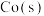 ,则容器中又会增加如下平衡:
,则容器中又会增加如下平衡: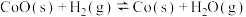 K1,
K1,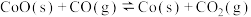 K2,最后反应达平衡时,容器中水的物质的量分数为
K2,最后反应达平衡时,容器中水的物质的量分数为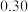 ,则K1等于
,则K1等于
您最近一年使用:0次