原子序数小于36的X、Y、Z、R、W五种元素,其中X是周期表中原子半径最小的元素,Y是形成化合物种类最多的元素,Z原子基态时2p原子轨道上有3个未成对的电子,R单质占空气体积的 ;W的原子序数为29。回答下列问题:
;W的原子序数为29。回答下列问题:
(1)Y2X4分子中Y原子轨道的杂化类型为________ ,1mol Z2X4含有σ键的数目为 ________ 。
(2)化合物ZX3与化合物X2R的VSEPR构型相同,但立体构型不同,ZX3的立体构型为________ ,两种化合物分子中化学键的键角较小的是________ (用分子式表示,下同)。
(3)与R同主族的三种非金属元素与X可形成结构相似的三种物质,试推测三者的稳定性由大到小的顺序________ ,理由是 ________ ;三者的沸点由高到低的顺序是 ________ ,解释原因________ 。
(4)元素Y的一种氧化物与元素Z的单质互为等电子体,元素Y的这种氧化物的分子式是________ 。
(5)W元素有________ 个运动状态不同的电子,其基态原子的价电子排布式为________ 。
 ;W的原子序数为29。回答下列问题:
;W的原子序数为29。回答下列问题:(1)Y2X4分子中Y原子轨道的杂化类型为
(2)化合物ZX3与化合物X2R的VSEPR构型相同,但立体构型不同,ZX3的立体构型为
(3)与R同主族的三种非金属元素与X可形成结构相似的三种物质,试推测三者的稳定性由大到小的顺序
(4)元素Y的一种氧化物与元素Z的单质互为等电子体,元素Y的这种氧化物的分子式是
(5)W元素有
18-19高二下·吉林辽源·期中 查看更多[3]
吉林省辽源市田家炳高级中学2018-2019学年高二下学期期中考试化学试题四川省宜宾市第四中学2018-2019学年高二下学期期中考试化学试题(已下线)2019年6月16日 《每日一题》选修3-每周一测
更新时间:2019-05-06 17:49:08
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】化合物G属于黄酮醋酸类化合物,具有保肝的作用。一种合成化合物G的路线如下:
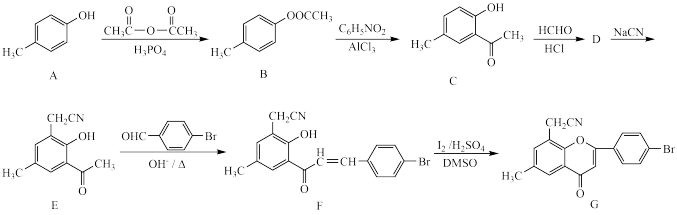
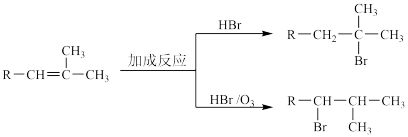
已知:烯烃与HBr发生加成时,不同的条件下有不同的反应方式:
(1)1 mol B分子中含有的σ键数目为_______ 。
(2)E→F分两步进行,反应类型依次为_______ 、_______ 。
(3)D的分子是C10H11O2Cl,D的结构简式为_______ 。
(4)E的一种同分异构体X同时符合下列条件。写出X的结构简式:_______ 。
Ⅰ.能使溴的CCl4溶液褪色,且消耗2 mol Br2
Ⅱ.分子中含3种化学环境不同的氢
(5)设计由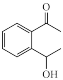 为原料,制备
为原料,制备 的合成路线(无机试剂和有机溶剂任选)
的合成路线(无机试剂和有机溶剂任选) _______ 。

已知:烯烃与HBr发生加成时,不同的条件下有不同的反应方式:

(1)1 mol B分子中含有的σ键数目为
(2)E→F分两步进行,反应类型依次为
(3)D的分子是C10H11O2Cl,D的结构简式为
(4)E的一种同分异构体X同时符合下列条件。写出X的结构简式:
Ⅰ.能使溴的CCl4溶液褪色,且消耗2 mol Br2
Ⅱ.分子中含3种化学环境不同的氢
(5)设计由
 为原料,制备
为原料,制备 的合成路线(无机试剂和有机溶剂任选)
的合成路线(无机试剂和有机溶剂任选)
您最近一年使用:0次
【推荐2】Hg-Ba-Cu-O 高温超导晶体A属四方晶系,正当晶胞如图所示:晶胞参 数a= 388.8 pm, c= 954.6 pm。

(1)铜离子易形成配合物。请说明[Cu(NH3)6]2+和[Fe(CN)6]4-的空间构型________ 。写出不变形配离子的全部轴次最高的旋转轴(方向及位置) ________ 。
(2)写出A的周期性重复的最小单位________ 。
(3)写出A晶胞中Ba离子的分数坐标(两个Ba离子之间的距离为z)________ 。
(4)通过掺杂X离子可以获得具有更高临界转变温度的超导材料B. B也属于四方晶系,晶胞参数a= 385.9pm, c= 1269.7 pm,正当晶胞的组成为HgBa2XCu2O6.部分离子坐标为: X(0.5, 0.5, y), Ba (0.5, 0.5, 0.2202),Cu(0, 0, 0.3771),O(1)(0, 0.5, 0.3771), O(2) (0, 0, 0.1556), O(3) (0.5,0, 0.3771)。B的全部宏观对称元素与A相同,画出以Hg为顶点的B的正当晶胞________ ,并指出y的数值_______ 。
(5)写出A、B二晶体中Cu原子的氧配位数________ 。
(6)已知B晶体理论密度为6.49 g·cm-3, 通过计算说明X是何种元素________ 。

(1)铜离子易形成配合物。请说明[Cu(NH3)6]2+和[Fe(CN)6]4-的空间构型
(2)写出A的周期性重复的最小单位
(3)写出A晶胞中Ba离子的分数坐标(两个Ba离子之间的距离为z)
(4)通过掺杂X离子可以获得具有更高临界转变温度的超导材料B. B也属于四方晶系,晶胞参数a= 385.9pm, c= 1269.7 pm,正当晶胞的组成为HgBa2XCu2O6.部分离子坐标为: X(0.5, 0.5, y), Ba (0.5, 0.5, 0.2202),Cu(0, 0, 0.3771),O(1)(0, 0.5, 0.3771), O(2) (0, 0, 0.1556), O(3) (0.5,0, 0.3771)。B的全部宏观对称元素与A相同,画出以Hg为顶点的B的正当晶胞
(5)写出A、B二晶体中Cu原子的氧配位数
(6)已知B晶体理论密度为6.49 g·cm-3, 通过计算说明X是何种元素
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,其中的字母编号代表对应的元素。试回答问题:
(1)元素⑦的原子结构示意图为_______ ,元素⑨价电子的轨道表示式为 _______ 。
(2)元素④基态原子核外共有_______ 种不同运动状态的电子,未成对电子数共有_______ 个。
(3)元素③的最简单氢化物分子的空间构型为_______ ,该氢化物含有_______ (填“极性”或“非极性”)键。
(4)③④⑤三种元素的原子电负性由小到大的顺序是_______ (用元素符号表示)。
(5)⑤⑥⑧三种元素的原子半径由大到小的顺序是_______ (用元素符号表示)。
(6)由元素⑩形成的1mol晶体中,含有的共价键为_______ mol。
| ① | ② | ③ | ④ | ⑤ | |||||||||||||
| ⑥ | ⑦ | ⑩ | ⑧ | ||||||||||||||
| ⑨ | |||||||||||||||||
(2)元素④基态原子核外共有
(3)元素③的最简单氢化物分子的空间构型为
(4)③④⑤三种元素的原子电负性由小到大的顺序是
(5)⑤⑥⑧三种元素的原子半径由大到小的顺序是
(6)由元素⑩形成的1mol晶体中,含有的共价键为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】配合物Fe(CO)5的熔点-20℃,沸点103℃,Fe(CO)5的结构式如图。可用于制备纯铁。

(1)基态Fe2+的价电子排布图为___________ ;基态Fe原子中有___________ 种能量不同的电子,有___________ 种运动状态不同的电子。
(2)C、O、Fe的电负性由大到小的顺序为___________ 。
(3)写出与CO互为等电子体的一种阴离子的电子式___________ 。
(4)关于Fe(CO)5,下列说法正确的是___________ 。
A.Fe(CO)5中Fe原子以sp3杂化,C原子sp杂化
B.Fe(CO)5是非极性分子,CO是极性分子
C.反应Fe(CO)5=Fe+5CO中没有新化学键生成
D.Fe(CO)5晶体属于分子晶体
(5)金属铁单质在不同温度下有两种堆积方式,其晶胞分别如图所示。

①体心立方晶胞中原子的空间利用率为___________ (用含π的代数式表示)。
②体心立方晶胞和面心立方晶胞中铁原子的配位数之比为___________ 。
③假设晶体中最近的原子都相切,忽略温度对原子半径的影响,则面心立方晶胞和体心立方晶胞的密度之比为___________ 。

(1)基态Fe2+的价电子排布图为
(2)C、O、Fe的电负性由大到小的顺序为
(3)写出与CO互为等电子体的一种阴离子的电子式
(4)关于Fe(CO)5,下列说法正确的是
A.Fe(CO)5中Fe原子以sp3杂化,C原子sp杂化
B.Fe(CO)5是非极性分子,CO是极性分子
C.反应Fe(CO)5=Fe+5CO中没有新化学键生成
D.Fe(CO)5晶体属于分子晶体
(5)金属铁单质在不同温度下有两种堆积方式,其晶胞分别如图所示。

①体心立方晶胞中原子的空间利用率为
②体心立方晶胞和面心立方晶胞中铁原子的配位数之比为
③假设晶体中最近的原子都相切,忽略温度对原子半径的影响,则面心立方晶胞和体心立方晶胞的密度之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】过渡金属元素种类众多,具有重要的用途,回答下列问题:
(1)Fe元素能形成化学式为[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁( III)]的络合物,其中基态Fe3+的核外电子排布式为___________ ,尿素中C原子的杂化方式是___________ ,Fe3+比Fe2+稳定的原因是___________ 。
(2)Ti广泛应用于航空航天行业,络合物[Ti(OH)2(H2O)4]2+中含有的化学键有___________
a.离子键 b.σ键 c.配位键 d.氢键
对比分析H2O、H2S、H2Se,沸点最低的是___________ ,键角最小的是___________ 热稳定性最强的是___________ : 钛酸亚铁(FeTiO3)与80%的硫酸反应可生成TiOSO4,写出与SO 互为等电子体的一种分子的化学式:
互为等电子体的一种分子的化学式:___________ 。
(3)Mn 、Sn元素形成的一种磁性材料的单晶胞结构如图所示。

该晶胞中碳原子的原子坐标为___________ ,该晶体的化学式为___________ 该晶体中距离Sn最近的Mn原子有___________ 个 。
(1)Fe元素能形成化学式为[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁( III)]的络合物,其中基态Fe3+的核外电子排布式为
(2)Ti广泛应用于航空航天行业,络合物[Ti(OH)2(H2O)4]2+中含有的化学键有
a.离子键 b.σ键 c.配位键 d.氢键
对比分析H2O、H2S、H2Se,沸点最低的是
 互为等电子体的一种分子的化学式:
互为等电子体的一种分子的化学式:(3)Mn 、Sn元素形成的一种磁性材料的单晶胞结构如图所示。

该晶胞中碳原子的原子坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】金属材料及其化合物应用十分广泛。回答下列问题:
(1)基态Mn原子核外未成对电子有___________ 个。
(2)NH3可以和很多过渡金属离子形成配合物,NH3的空间构型为___________ ,其中N原子的杂化轨道类型为___________ 。
(3)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为___________ ,其配位数为___________ 。
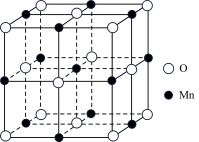
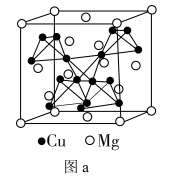
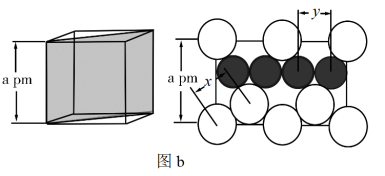
(4)图a是MgCu2的结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图b是沿立方格子对角面取得的截图。可见,Mg原子之间最短距离x=___________ pm,Cu原子之间最短距离y=___________ pm,。设阿伏加德罗常数的值为NA,则MgCu2的密度是___________ g·cm-3(列出计算表达式)。
(1)基态Mn原子核外未成对电子有
(2)NH3可以和很多过渡金属离子形成配合物,NH3的空间构型为
(3)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为

(4)图a是MgCu2的结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图b是沿立方格子对角面取得的截图。可见,Mg原子之间最短距离x=


您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】二甲基亚砜( )是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:
)是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:
(1)铬和锰基态原子核外未成对电子数之比为_______ 。
(2)已知:二甲基亚砜能够与水和丙酮( )分别以任意比互溶。二甲基亚砜分子中硫原子的杂化类型为
)分别以任意比互溶。二甲基亚砜分子中硫原子的杂化类型为_______ 。丙酮分子中各原子电负性由大到小的顺序为_______ 。二甲基亚砜能够与水以任意比互溶的原因为_______ 。
(3)CrCl3·6H2O的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3:2:1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为_______ 。
(4)已知硫化锰(MnS)晶胞如图所示,该晶胞参数α=120°,β=γ=90°。

①晶体中锰原子的配位数为_______ 。
②已知锰和硫的原子半径分别r1nm和r2nm,该晶体中原子的空间利用率为_______ (列出计算式即可)。
 )是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:
)是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:(1)铬和锰基态原子核外未成对电子数之比为
(2)已知:二甲基亚砜能够与水和丙酮(
 )分别以任意比互溶。二甲基亚砜分子中硫原子的杂化类型为
)分别以任意比互溶。二甲基亚砜分子中硫原子的杂化类型为(3)CrCl3·6H2O的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3:2:1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为
(4)已知硫化锰(MnS)晶胞如图所示,该晶胞参数α=120°,β=γ=90°。

①晶体中锰原子的配位数为
②已知锰和硫的原子半径分别r1nm和r2nm,该晶体中原子的空间利用率为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如右图所示。
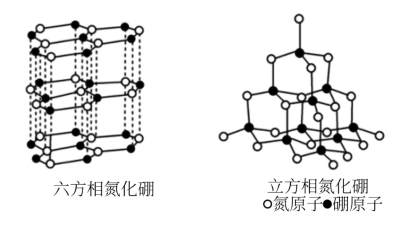
⑴基态硼原子的电子排布式为______________________________ 。
⑵关于这两种晶体的说法,正确的是_________________ (填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键d.两种晶体均为分子晶体
⑶六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为________ ,其结构与石墨相似却不导电,原因是______________________________ 。
⑷立方相氮化硼晶体中,硼原子的杂化轨道类型为___________________ 。该晶体的天然矿物在青藏高原在下约300Km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是____________________________ 。
⑸NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1mo NH4BF4含有_____________ mol配位键。

⑴基态硼原子的电子排布式为
⑵关于这两种晶体的说法,正确的是
a.立方相氮化硼含有σ键和π键,所以硬度大b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键d.两种晶体均为分子晶体
⑶六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为
⑷立方相氮化硼晶体中,硼原子的杂化轨道类型为
⑸NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1mo NH4BF4含有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】铁和钴是两种重要的过渡元素。
(1)钴位于元素周期表得第_____________ 族,其基态原子中未成对电子的个数为______ 。
(2)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为________ ,所含非金属元素的第一电离能由大到小的顺序是_________ 。
(3)尿素分子中碳原子为________ 杂化,分子中σ键与π键的数目之比为_____ 。
(4)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=___ 。Fe(CO)x常温下呈液态,熔点为-20 .5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于_______ (填晶体类型)。
(5)血红素是吡咯(C4H5N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如图所示。
吡咯 血红素
血红素
①1 mol吡咯分子中所含的σ键总数为____ 个。(用NA表示阿伏伽德罗常数的值)分子中的大π键可用 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为____ 。
②血液中的O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过____ 键相结合。
③血红素中N的杂化方式为______________ ,请画出血红素中N与Fe的配位键_______ 。
(1)钴位于元素周期表得第
(2)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为
(3)尿素分子中碳原子为
(4)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=
(5)血红素是吡咯(C4H5N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如图所示。
吡咯
 血红素
血红素
①1 mol吡咯分子中所含的σ键总数为
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为②血液中的O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过
③血红素中N的杂化方式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】我国科学家研发的全球首套千吨级太阳能燃料合成项目,为实现“碳中和”目标作出了重大贡献。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。
(1)钙钛矿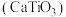 型化合物是一类可用于生产太阳能电池的功能材料,
型化合物是一类可用于生产太阳能电池的功能材料, 的晶胞如图所示。
的晶胞如图所示。

①基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
② 组成元素的电负性大小顺序是
组成元素的电负性大小顺序是_______ ; 的配位数是
的配位数是_______ 。
(2)单晶硅是生产太阳能电池板的主要原料, 是生产单晶硅的前驱体,可发生水解反应,机理如图:
是生产单晶硅的前驱体,可发生水解反应,机理如图:

注:含s、p、d轨道的杂化类型有: 、
、 、
、 。
。
在 水解为中间体
水解为中间体 的过程中,
的过程中, 原子的杂化类型由
原子的杂化类型由_______ 变为_______ 。
(3)甲醇的沸点 介于水
介于水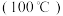 和甲硫醇
和甲硫醇 之间,其原因是
之间,其原因是_______ 。
(4)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为 固溶体。在
固溶体。在 中掺杂少量
中掺杂少量 后形成的催化剂,化学式可表示为
后形成的催化剂,化学式可表示为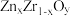 ,则
,则
_______ (用含x的表达式)。
(1)钙钛矿
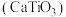 型化合物是一类可用于生产太阳能电池的功能材料,
型化合物是一类可用于生产太阳能电池的功能材料, 的晶胞如图所示。
的晶胞如图所示。
①基态
 原子的核外电子排布式为
原子的核外电子排布式为②
 组成元素的电负性大小顺序是
组成元素的电负性大小顺序是 的配位数是
的配位数是(2)单晶硅是生产太阳能电池板的主要原料,
 是生产单晶硅的前驱体,可发生水解反应,机理如图:
是生产单晶硅的前驱体,可发生水解反应,机理如图:
注:含s、p、d轨道的杂化类型有:
 、
、 、
、 。
。在
 水解为中间体
水解为中间体 的过程中,
的过程中, 原子的杂化类型由
原子的杂化类型由(3)甲醇的沸点
 介于水
介于水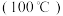 和甲硫醇
和甲硫醇 之间,其原因是
之间,其原因是(4)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为
 固溶体。在
固溶体。在 中掺杂少量
中掺杂少量 后形成的催化剂,化学式可表示为
后形成的催化剂,化学式可表示为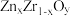 ,则
,则
您最近一年使用:0次
【推荐2】金属冶炼过程中一种用有机化合物从水溶液中提取Cu2+的流程如下所示:

(1)有机化合物W的结构简式为:
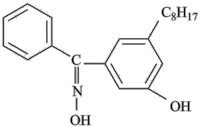
①该分子中与氮原子相连的氧原子的杂化轨道类型为___________ 。
②关于W的说法正确的是___________ 。
a.能发生取代、加成、还原反应
b.可与碳酸钠反应产生气体
c.含有氨基官能团
(2)W可与Cu2+形成化合物Q,其结构如下图所示。

①解释氢键形成的原因___________ 。
②氢键对Q在水中溶解性的影响是___________ (填“增大”或“减小”)。
③Cu2+与氮原子之间形成的化学键的类型是___________ 。

(1)有机化合物W的结构简式为:

①该分子中与氮原子相连的氧原子的杂化轨道类型为
②关于W的说法正确的是
a.能发生取代、加成、还原反应
b.可与碳酸钠反应产生气体
c.含有氨基官能团
(2)W可与Cu2+形成化合物Q,其结构如下图所示。

①解释氢键形成的原因
②氢键对Q在水中溶解性的影响是
③Cu2+与氮原子之间形成的化学键的类型是
您最近一年使用:0次




 化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有
化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有

