我国具有丰富的铜矿资源,请回答下列有关铜及其化合物的问题:
(1)请写出基态Cu原子的价电子排布式_________ 。焰火中的绿色是铜的焰色,基态铜原子在灼烧时价电子发生了_________ 而变为激发态。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Il(Zn)______ Il(Cu)(填“大于”或“小于”),原因是___________ 。
(3)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式:
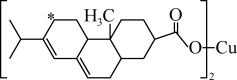
请分析1个松脂酸铜中π键的个数___________ 加“*”碳原子的杂化方式为_____________ 。
(4)硫酸铜溶于氨水形成 4深蓝色溶液。
4深蓝色溶液。
① 中阴离子的立体构型是
中阴离子的立体构型是_______ 。
②在 中
中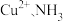 之间形成的化学键称为
之间形成的化学键称为_____ ,提供孤电子对的成键原子是_______________________ 。
③氨的沸点_________________ (填“高于”或“低于”)膦;
(5)黄铜合金可以表示为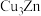 ,为面心立方晶胞,晶体密度为8.5
,为面心立方晶胞,晶体密度为8.5 ,求晶胞的边长
,求晶胞的边长___________ (只写计算式,不求结果)
(1)请写出基态Cu原子的价电子排布式
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Il(Zn)
(3)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式:

请分析1个松脂酸铜中π键的个数
(4)硫酸铜溶于氨水形成
 4深蓝色溶液。
4深蓝色溶液。 ①
 中阴离子的立体构型是
中阴离子的立体构型是②在
 中
中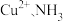 之间形成的化学键称为
之间形成的化学键称为③氨的沸点
(5)黄铜合金可以表示为
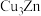 ,为面心立方晶胞,晶体密度为8.5
,为面心立方晶胞,晶体密度为8.5 ,求晶胞的边长
,求晶胞的边长
更新时间:2019-05-07 10:42:32
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】SiC又叫金刚砂,是砂轮的主要成分,可看作是金刚石里一半碳原子被硅原子替换的产物。
(1)工业上用焦炭和石英在高温下反应制得SiC:3C+SiO2 SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为
SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为________ 。
(2)SiC晶体中有两个含五个原子的基本结构单元,分别是__________ 和_________ 。
(3)SiC晶体中最小的原子环是____ 元环,该环独立有___ 个Si原子,_____ 个C原子。
(4)1molSiC晶体中含____ mol Si-C键。
(5)金刚石、SiC晶体、晶体Si 熔点由高到低的顺序_____________ 。
(1)工业上用焦炭和石英在高温下反应制得SiC:3C+SiO2
 SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为
SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为(2)SiC晶体中有两个含五个原子的基本结构单元,分别是
(3)SiC晶体中最小的原子环是
(4)1molSiC晶体中含
(5)金刚石、SiC晶体、晶体Si 熔点由高到低的顺序

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1。在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,原理为:2XCl+2CO+ 2H2O==X2Cl2·2CO·2H2O
(1)X原子基态核外电子排布式为_________ ;
(2)C、H、O三种元素的电负性由大到小的顺序为________ ;
(3)H2O中氧原子的轨道杂化类型为__________ ;
(4)X2Cl2·2CO·2H2O是一种配合物,结构如图所示,每个X原子能与其他原子形成3个配位键,在图中用“→"标出相应的配位键__ 。CO与N2分子的结构相似,则1molX2Cl2·2CO·2H2O含有δ键的数目为__ 。
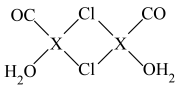
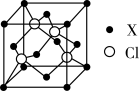
(5)化合物XCl晶体的晶胞如图所示,距离每个X离子最近的Cl的个数为________ 。
(1)X原子基态核外电子排布式为
(2)C、H、O三种元素的电负性由大到小的顺序为
(3)H2O中氧原子的轨道杂化类型为
(4)X2Cl2·2CO·2H2O是一种配合物,结构如图所示,每个X原子能与其他原子形成3个配位键,在图中用“→"标出相应的配位键

(5)化合物XCl晶体的晶胞如图所示,距离每个X离子最近的Cl的个数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】在电解冶炼铝的过程中加入冰晶石,可起到降低 Al2O3熔融温度的作用。冰晶石的生产 原理为 2Al(OH)3+12HF+3Na2CO3===2Na3AlF6+3CO2↑+9H2O。根据题意填空:
(1)冰晶石的晶体不导电,但熔融时能导电,则在冰晶石晶体中存在_____ (填序号)。
a.离子键 b.极性键 c.配位键 d.范德华力
(2)CO2 分子的空间构型为___ ,中心原子的杂化方式为__ ,和 CO2互为等电子体的氧化物是___ 。
(3)反应物中电负性最大的元素为_____ (填元素符号),写出其原子最外层的电子排布式____ 。
(4)冰晶石由两种微粒构成,冰晶石的晶胞结构如图甲所示,黑球位于大立方体的顶点和面心,白球位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是______ (填具体的微粒符号)。

(5)Al 单质的晶体中原子的堆积方式如图乙所示,其晶胞结构如图丙所示,原子之间相 互位置关系的平面图如图丁所示。若已知 Al 的原子半径为 d cm,NA代表阿伏加 德罗常数的 值,Al 的相对原子质量为 Mr,则一个晶胞中 Al 原子的数目为______ 个;Al 晶体的密度为________ (用字母表示)。
(1)冰晶石的晶体不导电,但熔融时能导电,则在冰晶石晶体中存在
a.离子键 b.极性键 c.配位键 d.范德华力
(2)CO2 分子的空间构型为
(3)反应物中电负性最大的元素为
(4)冰晶石由两种微粒构成,冰晶石的晶胞结构如图甲所示,黑球位于大立方体的顶点和面心,白球位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是

(5)Al 单质的晶体中原子的堆积方式如图乙所示,其晶胞结构如图丙所示,原子之间相 互位置关系的平面图如图丁所示。若已知 Al 的原子半径为 d cm,NA代表阿伏加 德罗常数的 值,Al 的相对原子质量为 Mr,则一个晶胞中 Al 原子的数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(1)Ni2+可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2-、丁二酮肟镍分子(见图)等。

①1mol[Ni(NH3)4]2+中含有_____ molσ键。
②[Ni(NH3)4]2+中H-N-H键角比NH3分子中H-N-H键角______ (填“大”或“小”)。
③丁二酮肟镍分子内含有的作用力有______ (填字母)。
a.配位键 b.离子键 c.氢键 d.范德华力
(2)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl2溶液时,则无明显现象。则第一种配合物的结构式可表示为______ ,第二种配合物的结构式可表示为______ 。若在第二种配合物的溶液中滴加AgNO3溶液,则产生的现象是______ 。
(3)关于[Ti(NH3)5Cl]Cl2的说法中错误的是______ 。
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol[Ti(NH3)5Cl]Cl2的水溶液中加入足量AgNO3溶液,产生3mol白色沉淀
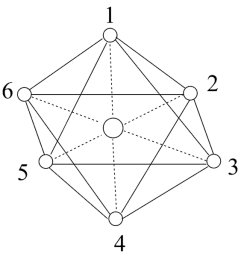
(4)已知[Co(NH3)6]3+的立体结构如图,其中1~6处的小圆圈表示NH3分子,且各相邻的NH3分子间的距离相等(图中虚线长度相等)。Co3+位于八面体的中心,若其中两个NH3被Cl-取代,所形成的[Co(NH3)4Cl2]+的结构的数目为______ 。
(1)Ni2+可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2-、丁二酮肟镍分子(见图)等。

①1mol[Ni(NH3)4]2+中含有
②[Ni(NH3)4]2+中H-N-H键角比NH3分子中H-N-H键角
③丁二酮肟镍分子内含有的作用力有
a.配位键 b.离子键 c.氢键 d.范德华力
(2)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl2溶液时,则无明显现象。则第一种配合物的结构式可表示为
(3)关于[Ti(NH3)5Cl]Cl2的说法中错误的是
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol[Ti(NH3)5Cl]Cl2的水溶液中加入足量AgNO3溶液,产生3mol白色沉淀
(4)已知[Co(NH3)6]3+的立体结构如图,其中1~6处的小圆圈表示NH3分子,且各相邻的NH3分子间的距离相等(图中虚线长度相等)。Co3+位于八面体的中心,若其中两个NH3被Cl-取代,所形成的[Co(NH3)4Cl2]+的结构的数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍行业发展蕴藏着巨大潜力。
(1)Ni元素位于周期表中_________ 区,基态Ni2+外围电子排布图是____________ 。
(2)Ni(CO)4常用作制备高纯镍粉,常温下为液态,易溶于CCl4、苯等有机溶剂。则:
①Ni(CO)4固态时属于________ 晶体(填晶体类型)
②已知CO与N2互为等电子体,则Ni(CO)4中σ键和π键的数目之比为____________ ,请事写出一种与CO互为等电子体的阴离子的化学式_________ 。
(3)NiSO4常用于电镀工业,丁二酮肟(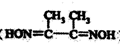 )是检验Ni2+的灵敏试剂,其中碳原子不存在
)是检验Ni2+的灵敏试剂,其中碳原子不存在_________ 杂化(填“sp”、“sp2”或“sp3”)。
(4)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的________ 空隙中,已知晶胞边长为a pm,阿伏加德罗常数为NA,NiO晶体的密度为________ g/cm3(只列出计算式)。

(5)NiO、FeO的晶体结构类型均与氯化钠的相同,熔点NiO>FeO,则离子半径r(Ni2+)________ r(Fe2+)(填“<”或“”>),请简述判断理由__________________________ 。
(1)Ni元素位于周期表中
(2)Ni(CO)4常用作制备高纯镍粉,常温下为液态,易溶于CCl4、苯等有机溶剂。则:
①Ni(CO)4固态时属于
②已知CO与N2互为等电子体,则Ni(CO)4中σ键和π键的数目之比为
(3)NiSO4常用于电镀工业,丁二酮肟(
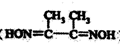 )是检验Ni2+的灵敏试剂,其中碳原子不存在
)是检验Ni2+的灵敏试剂,其中碳原子不存在(4)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的

(5)NiO、FeO的晶体结构类型均与氯化钠的相同,熔点NiO>FeO,则离子半径r(Ni2+)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】钴及其化合物在化工生产中有重要的用途。三氯化六氨合钴(Ⅲ)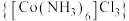 是黄色或橙黄色晶体,实验室以
是黄色或橙黄色晶体,实验室以 为原料经催化制备
为原料经催化制备 ,步骤如下:
,步骤如下:
I. 的制备
的制备
 可以通过钴和氯气反应制得,实验室制备纯净
可以通过钴和氯气反应制得,实验室制备纯净 可用如图实验装置(已知:
可用如图实验装置(已知: 易潮解)。
易潮解)。
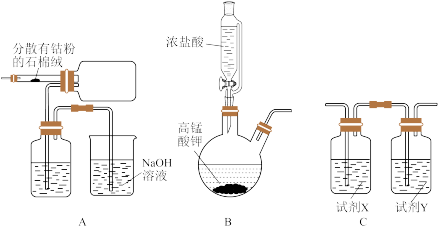
(1)B装置用于制备氯气,其反应的化学方程式为_______ 。A装置中洗气瓶内所装试剂的名称为_______ 。
(2)组装好仪器进行实验时,要先加入浓盐酸,使B装置中开始生成氯气,待A装置内充满黄绿色气体,再加热A装置中的钴粉,目的是_______ 。
II.三氯化六氨合钴(Ⅲ)的制备。其原理为:
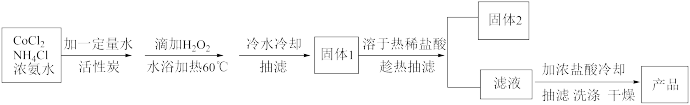
已知:三氯化六氨合钴不溶于乙醇,常温水中溶解度较小。
(3)水浴温度不超过60℃的原因是_______ 。
(4)下列说法不正确的是_______(填标号)。
III.晶体结构测定与钴含量分析。
(5)测定晶体结构最常见的仪器是_______ ,从而获取晶胞形状和大小、分子或原子在微观空间的有序排列。 中心离子采取
中心离子采取 杂化,其空间结构为
杂化,其空间结构为_______ 。
(6)利用 将KI氧化成
将KI氧化成 ,
, 被还原后的产物为
被还原后的产物为 。然后用
。然后用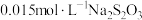 标准溶液滴定生成的
标准溶液滴定生成的 ,
, 所得产物为
所得产物为 。若称取样品的质量为0.295g,滴定
。若称取样品的质量为0.295g,滴定 时,达到终点消耗
时,达到终点消耗 标准溶液的平均体积为54.00mL。该样品中钴元素的质量分数为
标准溶液的平均体积为54.00mL。该样品中钴元素的质量分数为_______ %。
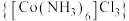 是黄色或橙黄色晶体,实验室以
是黄色或橙黄色晶体,实验室以 为原料经催化制备
为原料经催化制备 ,步骤如下:
,步骤如下:I.
 的制备
的制备 可以通过钴和氯气反应制得,实验室制备纯净
可以通过钴和氯气反应制得,实验室制备纯净 可用如图实验装置(已知:
可用如图实验装置(已知: 易潮解)。
易潮解)。
(1)B装置用于制备氯气,其反应的化学方程式为
(2)组装好仪器进行实验时,要先加入浓盐酸,使B装置中开始生成氯气,待A装置内充满黄绿色气体,再加热A装置中的钴粉,目的是
II.三氯化六氨合钴(Ⅲ)的制备。其原理为:

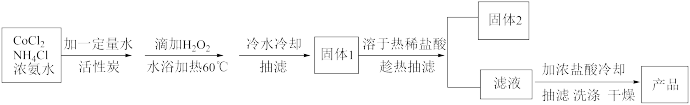
已知:三氯化六氨合钴不溶于乙醇,常温水中溶解度较小。
(3)水浴温度不超过60℃的原因是
(4)下列说法不正确的是_______(填标号)。
A. 除作为反应物外,还有调节溶液的pH、增强 除作为反应物外,还有调节溶液的pH、增强 的氧化性的作用 的氧化性的作用 |
| B.活性炭是脱色剂、固体2是活性炭 |
C.加入浓盐酸,析出产品的反应方程式为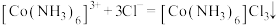 |
| D.可用乙醇水溶液洗涤产品 |
III.晶体结构测定与钴含量分析。
(5)测定晶体结构最常见的仪器是
 中心离子采取
中心离子采取 杂化,其空间结构为
杂化,其空间结构为(6)利用
 将KI氧化成
将KI氧化成 ,
, 被还原后的产物为
被还原后的产物为 。然后用
。然后用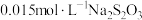 标准溶液滴定生成的
标准溶液滴定生成的 ,
, 所得产物为
所得产物为 。若称取样品的质量为0.295g,滴定
。若称取样品的质量为0.295g,滴定 时,达到终点消耗
时,达到终点消耗 标准溶液的平均体积为54.00mL。该样品中钴元素的质量分数为
标准溶液的平均体积为54.00mL。该样品中钴元素的质量分数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为_______ 。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成,第一电离能I1(Zn)_______ I1(Cu)(填“大于”或“小于”)。原因是_______ 。
(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为_______ ,C原子的杂化形式为_______ 。
(4)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______ 。六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为NA,Zn的密度为_______ g·cm-3(列出计算式)。

(1)Zn原子核外电子排布式为
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成,第一电离能I1(Zn)
(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
(4)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表列出了前20号元素中的某些元素性质的有关数据
试回答下列问题:
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是____________ (填写编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是______ (写分子式)。某元素R的原子半径为1.02×10-10m,该元素在周期表中位于______ ;若物质Na2R3是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式______ 。
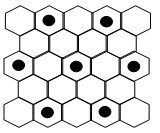
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,该物质的化学式为______ 。
 。
。
 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
原子半径( ) ) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,该物质的化学式为
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】铍由于重量轻、弹性模数高和热稳定性好,已成为引人注目的飞机和导弹结构材料。
(1)Be的基态原子核外电子排布式_______ 。
(2)铍的某些化合物的结构如图所示,图1为气态氯化铍,图2为固态氯化铍。
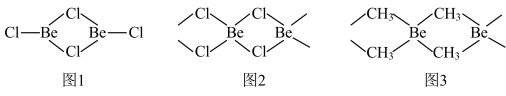
①气态氯化铍为_______ (填“极性”、“非极性”)分子。氯化铍由气态转化为固态,Be的杂化方式由_______ 转化为_______ 。
②若将固态氯化铍中的Cl原子替换为甲基(—CH3),可形成如图3化合物。1个甲基与2个Be原子形成共价键时所提供的电子数为_______ 。
③上述化合物涉及四种元素的电负性由大到小的顺序为_______ 。
(3)Be2+与 会反应生成配离子
会反应生成配离子 ,已知Be的配位数为4,则配合物中配位原子为
,已知Be的配位数为4,则配合物中配位原子为_______ 。
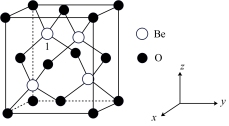
(4)氧化铍晶胞结构如如图所示,则1号Be原子的原子坐标。为_______ 。
(1)Be的基态原子核外电子排布式
(2)铍的某些化合物的结构如图所示,图1为气态氯化铍,图2为固态氯化铍。

①气态氯化铍为
②若将固态氯化铍中的Cl原子替换为甲基(—CH3),可形成如图3化合物。1个甲基与2个Be原子形成共价键时所提供的电子数为
③上述化合物涉及四种元素的电负性由大到小的顺序为
(3)Be2+与
 会反应生成配离子
会反应生成配离子 ,已知Be的配位数为4,则配合物中配位原子为
,已知Be的配位数为4,则配合物中配位原子为(4)氧化铍晶胞结构如如图所示,则1号Be原子的原子坐标。为

您最近一年使用:0次



