现有 、
、 、
、 三种元素的基态原子的电子排布式如下:①1s22s22p63s23p4,②1s22s22p63s23p3,③1s22s22p5。则下列有关比较中正确的是
三种元素的基态原子的电子排布式如下:①1s22s22p63s23p4,②1s22s22p63s23p3,③1s22s22p5。则下列有关比较中正确的是
 、
、 、
、 三种元素的基态原子的电子排布式如下:①1s22s22p63s23p4,②1s22s22p63s23p3,③1s22s22p5。则下列有关比较中正确的是
三种元素的基态原子的电子排布式如下:①1s22s22p63s23p4,②1s22s22p63s23p3,③1s22s22p5。则下列有关比较中正确的是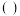
A.第一电离能: |
B.简单离子半径: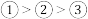 |
C.电负性: |
D.最高价氧化物对应水化物的酸性: |
更新时间:2019-05-13 15:33:16
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】工业上以含硫矿物(如黄铁矿)为原料来制备硫酸,其流程如下:
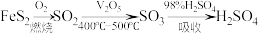
下列说法正确的是
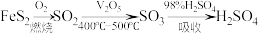
下列说法正确的是
| A.基态S原子核外有16种不同空间运动状态的电子 |
B.食品中添加适量的 可以起到漂白、防腐和抗氧化等作用 可以起到漂白、防腐和抗氧化等作用 |
C.浓硫酸不能干燥 ,但可干燥HI ,但可干燥HI |
D. 能降低反应的活化能,提高 能降低反应的活化能,提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某种催化剂阴离子的结构式如下所示,其组成元素X、Y、Z为原子半径逐渐增大的短周期元素,W是第四周期的某种元素,其化合物常用于检验酒驾,原子序数关系为:2X+2Y+Z=W,下列说法正确的是


A.该阴离子结构中有 键与 键与 键数目之比为9∶2 键数目之比为9∶2 |
| B.简单氢化物的稳定性:Y>Z,还原性:Y<Z |
| C.W在此离子中的化合价为+6价 |
D.W的基态原子价电子排布图为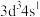 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法错误的是( )
| A.若把H2S分子写成H3S分子,违背了共价键的饱和性 |
| B.H3O+离子中存在配位键 |
| C.已知X、Y元素同周期,且电负性X>Y, 第一电离能X一定大于Y |
| D.在面心立方堆积的金属晶体中,属于1个晶胞的金属原子有4个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z为原子序数依次增大的主族元素,Y与Z同主族。W为第四周期元素,最外层电子数为1,价层电子数为11,四种元素组成的某蓝色晶体基本结构单元的结构简式如下图所示。下列说法不正确的是


| A.原子半径Z>Y>X |
| B.Y的第一电离能比同周期相邻元素小 |
| C.单质W和Z在加热条件下生成化合物WZ |
| D.Y的简单氢化物的热稳定性强于Z的简单氢化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、Q、E、M六种元素中,X的原子的基态价电子排布式为2s2,Y的基态原子核外有5种运动状态不同的电子,Z元素的两种同位素原子通常作为示踪原子研究生物化学反应和测定文物的年代,Q是元素周期表中电负性最大的元素,E的阳离子通常存在于硝石、明矾和草木灰中,M的原子序数比E大1。下列说法正确的是
| A.EYQ4中阴离子中心原子的杂化方式为sp3杂化 |
| B.X、Y元素的第一电离能大小关系:X<Y |
C.ZO 的空间构型为三角锥形 的空间构型为三角锥形 |
| D.MZ2含离子键和非极性共价键,阴阳离子之比为1∶2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.电负性越大的元素对键合电子的吸引力强,其第一电离能也越大 |
B. 与 与 两种离子的空间构型相同,但其中心原子的杂化方式不同 两种离子的空间构型相同,但其中心原子的杂化方式不同 |
| C.H2O2与C2H2均为既含σ键又含π键的非极性分子 |
| D.NH3的稳定性强于AsH3的原因为NH3存在分子间氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关说法正确的是
A.SiF4和SO 的中心原子的杂化轨道类型均为sp3杂化 的中心原子的杂化轨道类型均为sp3杂化 |
| B.电负性越大,元素的非金属性越强,第一电离能也越大 |
| C.乙醇分子和水分子间只存在范德华力 |
| D.在[Cu(NH3)4]2+中,Cu2+给出孤电子对,NH3提供空轨道 |
您最近一年使用:0次

 的空间结构为四面体形
的空间结构为四面体形
 分子中
分子中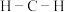 的键角小于光气
的键角小于光气 分子中
分子中 的键角
的键角





