三氯化硼(BCl3),主要用作半导体硅的掺杂源或有机合成催化剂,还用于高纯硼或有机硼的制取。某兴趣小组用氯气和硼为原料,采用下列装置(部分装置可重复使用)制备BCl3。
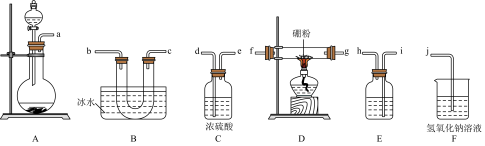
已知:①BCl3的沸点为12.5℃,熔点为-107.3℃;遇水剧烈反应生成硼酸和盐酸;②2B+6HCl 2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
请回答下列问题:
(1)A装置可用氯酸钾固体与浓盐酸反应制氯气,反应的化学方程式为___________ 。
(2)装置从左到右的接口连接顺序为a→___________________ →j。
(3)装里E中的试剂为___________ ,如果拆去E装置,可能的后果是____________ 。
(4)D装置中发生反应前先通入一段时间的氯气,排尽装置中的空气。若缺少此步骤,则造成的结果是_____ 。
(5)三氯化硼与水能剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式________ ,硼酸也可用电渗析法制备,“四室电渗析法”工作原理如图所示:

则阳极的电极反应式__________________ ,分析产品室可得到H3BO3的原因________________ 。

已知:①BCl3的沸点为12.5℃,熔点为-107.3℃;遇水剧烈反应生成硼酸和盐酸;②2B+6HCl
 2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。请回答下列问题:
(1)A装置可用氯酸钾固体与浓盐酸反应制氯气,反应的化学方程式为
(2)装置从左到右的接口连接顺序为a→
(3)装里E中的试剂为
(4)D装置中发生反应前先通入一段时间的氯气,排尽装置中的空气。若缺少此步骤,则造成的结果是
(5)三氯化硼与水能剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式

则阳极的电极反应式
更新时间:2019-05-11 16:55:20
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气,设计了如下实验装置。请按要求回答下列问题:
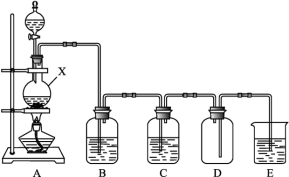
(1)仪器X的名称为_______ ,其中发生反应的化学方程式为_______
(2)欲除去 中的HCl,装置B中应选用的试剂为
中的HCl,装置B中应选用的试剂为_______ 。
(3)进入装置B的 中含有的杂质,除HCl外还有
中含有的杂质,除HCl外还有_______ ,欲除去该杂质,装置C中盛放的试剂名称为_______ 。
(4)装置D中的一处明显错误为_______ 。
(5)装置E中的试剂为_______
(6)假设收集到VL(标准状况下) ,与过量冷的石灰乳完全反应,所得漂白粉中有效成分
,与过量冷的石灰乳完全反应,所得漂白粉中有效成分 的质量为
的质量为_______ g(用含V的代数式表示)。

(1)仪器X的名称为
(2)欲除去
 中的HCl,装置B中应选用的试剂为
中的HCl,装置B中应选用的试剂为(3)进入装置B的
 中含有的杂质,除HCl外还有
中含有的杂质,除HCl外还有(4)装置D中的一处明显错误为
(5)装置E中的试剂为
(6)假设收集到VL(标准状况下)
 ,与过量冷的石灰乳完全反应,所得漂白粉中有效成分
,与过量冷的石灰乳完全反应,所得漂白粉中有效成分 的质量为
的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为红色的铜网,其右端出气管口放有脱脂棉。
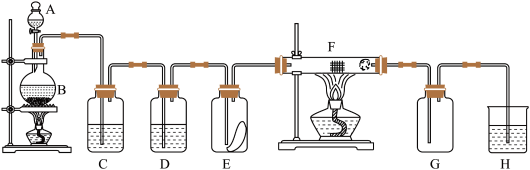
请回答下列问题:
(1)仪器A的名称是___________ 。
(2)写出实验室制氯气的化学方程式___________ 。
(3)装置C中盛装的溶液是___________ ,D中试剂的作用是___________ 。
(4)在空气中点燃纯净的氢气,然后把导管缓慢伸入盛满氯气的集气瓶中,请描述实验现象___________ 。
(5)E中的红色布条是否褪色?___________ (填“是”或“否”),F中的反应现象为___________ 。
(6)H中的试剂为___________ 溶液,用来吸收多余氯气。

请回答下列问题:
(1)仪器A的名称是
(2)写出实验室制氯气的化学方程式
(3)装置C中盛装的溶液是
(4)在空气中点燃纯净的氢气,然后把导管缓慢伸入盛满氯气的集气瓶中,请描述实验现象
(5)E中的红色布条是否褪色?
(6)H中的试剂为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】用如图所示装置可以完成一系列实验(图中夹持装置已略去)。
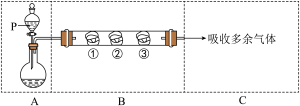
用装置A由浓硫酸和浓盐酸混合制取HCl气体,装置B中的三处棉花依次做了如下处理:①包有某固体物质,②蘸有KI溶液,③蘸有石蕊溶液。请回答下列问题:
(1)分液漏斗下面的玻璃仪器名称是___________ 。
(2)①处包有的某固体物质可能是(填符号)___________ ,发生反应的离子反应方程式:___________
a.MnO2 b.KMnO4 c.KCl d.Cu
反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式:___________ 。
(3)在实验过程中,在③处能观察到的现象是___________ 。

用装置A由浓硫酸和浓盐酸混合制取HCl气体,装置B中的三处棉花依次做了如下处理:①包有某固体物质,②蘸有KI溶液,③蘸有石蕊溶液。请回答下列问题:
(1)分液漏斗下面的玻璃仪器名称是
(2)①处包有的某固体物质可能是(填符号)
a.MnO2 b.KMnO4 c.KCl d.Cu
反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式:
(3)在实验过程中,在③处能观察到的现象是
您最近一年使用:0次
【推荐1】工业上生产金属钛的方法很多。以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如图,其中钛铁矿与浓硫酸发生反应的化学方程式为:FeTiO3+2H2SO4=TiOSO4+FeSO4+2H2O
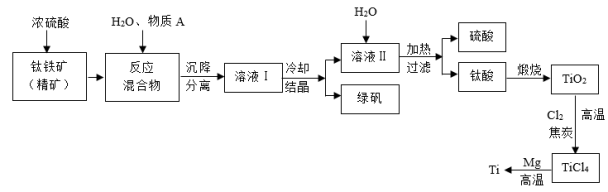
回答下列问题:
(1)钛铁矿和浓硫酸反应属于_______ (选填“氧化还原反应”或“非氧化还原反应”)。
(2)上述生产流程中加入物质A的目的是防止Fe2+被氧化,物质A是_______ ,上述制备TiO2的过程中,所得到的副产物和可回收利用的物质分别是_______ 、_______ 。
(3)反应TiCl4+2Mg=2MgCl2+Ti在Ar气氛中进行的理由是_______ 。
(4)由二氧化钛制取四氯化钛所涉及的反应有:
TiO2 (s)+ 2Cl2 (g) +2C(s) =TiCl4(g) + 2CO(g) ΔH1 = -72 kJ•mol-1
TiO2(s) + 2Cl2 (g) =TiCl4(g) + O2 (g) ΔH2 =+38.8kJ•mol-1
C(s)+CO2(g)=2CO(g) ΔH3 =+282.8kJ•mol-1
①反应C(s)+CO2(g)=2CO(g)在高温下能够自发进行的原因是_______ 。
②反应C(s)+O2(g)=CO2 (g)的ΔH=_______ 。
(5)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。①写出阳极所发生反应的电极反应式:_______ 。

②在制备金属钛前后,CaO的总量不变,其原因是(请结合化学用语解释)_______ 。

回答下列问题:
(1)钛铁矿和浓硫酸反应属于
(2)上述生产流程中加入物质A的目的是防止Fe2+被氧化,物质A是
(3)反应TiCl4+2Mg=2MgCl2+Ti在Ar气氛中进行的理由是
(4)由二氧化钛制取四氯化钛所涉及的反应有:
TiO2 (s)+ 2Cl2 (g) +2C(s) =TiCl4(g) + 2CO(g) ΔH1 = -72 kJ•mol-1
TiO2(s) + 2Cl2 (g) =TiCl4(g) + O2 (g) ΔH2 =+38.8kJ•mol-1
C(s)+CO2(g)=2CO(g) ΔH3 =+282.8kJ•mol-1
①反应C(s)+CO2(g)=2CO(g)在高温下能够自发进行的原因是
②反应C(s)+O2(g)=CO2 (g)的ΔH=
(5)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。①写出阳极所发生反应的电极反应式:

②在制备金属钛前后,CaO的总量不变,其原因是(请结合化学用语解释)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
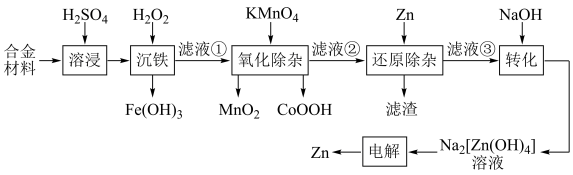
【推荐2】某废弃合金材料的主要成分为Zn,还含有Co、Fe、Mn、Cd及其氧化物。从该合金材料中生产高纯锌并分离各种金属化合物的工艺流程如下: 下,部分难溶物质的溶解平衡常数如下表:
下,部分难溶物质的溶解平衡常数如下表:
②当某离子浓度低于 时,认为溶液中不存在该离子。
时,认为溶液中不存在该离子。
回答下列问题:
(1)能提高“溶浸”效率的具体措施为___________ (任写一条);
(2)“滤液①”中含有的金属离子 、
、 、
、 、
、 ,且离子浓度均不高于
,且离子浓度均不高于 ;
;
①还原性:
___________  (填“
(填“ ”“
”“ ”或“
”或“ ”);
”);
②“滤液①”中pH的范围为___________ ;
(3)若“滤液②”的 ,则“氧化除杂”中发生反应的离子方程式为
,则“氧化除杂”中发生反应的离子方程式为___________ ;
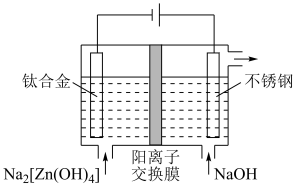
(4)“电解”工作原理如图。其中阴极的电极反应式为___________ ;若阴极区和阳极区溶液体积相等,电解过程中阳极区的
___________ (填“增加”或“减少”) ,阴极区
,阴极区___________ (填“增加”或“减少”)的
___________ ;
 下,部分难溶物质的溶解平衡常数如下表:
下,部分难溶物质的溶解平衡常数如下表:| 难溶电解质 |  |  |  |  |  | 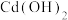 |
 | 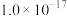 | 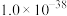 | 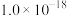 |  | 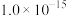 | 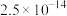 |
 时,认为溶液中不存在该离子。
时,认为溶液中不存在该离子。回答下列问题:
(1)能提高“溶浸”效率的具体措施为
(2)“滤液①”中含有的金属离子
 、
、 、
、 、
、 ,且离子浓度均不高于
,且离子浓度均不高于 ;
;①还原性:

 (填“
(填“ ”“
”“ ”或“
”或“ ”);
”);②“滤液①”中pH的范围为
(3)若“滤液②”的
 ,则“氧化除杂”中发生反应的离子方程式为
,则“氧化除杂”中发生反应的离子方程式为(4)“电解”工作原理如图。其中阴极的电极反应式为

 ,阴极区
,阴极区
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】铂是重要的催化剂和吸氢材料,广泛用于新能源和化工行业。一种以电解精炼铜的阳极泥(含Pt、Au、Ag及少量有机物)为原料生产海绵Pt及Au的工艺流程如下:

回答下列问题:
(1)电解精炼铜时阴极的电极反应式为___________ 。
(2)“焙烧”的主要目的是___________ ,“操作Ⅰ”为___________ 。
(3)已知“滤液Ⅰ”主要含HAuCl4、H2PtCl6,且二者均为强酸。HAuCl4中金元素化合价为___________ ,H2PtCl6的电离方程式为___________ 。
(4)“沉金”的化学反应方程式为___________ 。
(5)“沉铂”中,生成(NH4)2PtCl6的沉淀率随温度的变化曲线如图所示,结合平衡移动原理解释升高温度,(NH4)2PtCl6沉淀率升高的主要原因___________ 。

(6)“灼烧”时发生分解反应的化学方程式为___________ 。

回答下列问题:
(1)电解精炼铜时阴极的电极反应式为
(2)“焙烧”的主要目的是
(3)已知“滤液Ⅰ”主要含HAuCl4、H2PtCl6,且二者均为强酸。HAuCl4中金元素化合价为
(4)“沉金”的化学反应方程式为
(5)“沉铂”中,生成(NH4)2PtCl6的沉淀率随温度的变化曲线如图所示,结合平衡移动原理解释升高温度,(NH4)2PtCl6沉淀率升高的主要原因

(6)“灼烧”时发生分解反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】亚氯酸钠(NaClO2)是一种重要的消毒剂,可用ClO2为原料制取。某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。

已知:饱和NaClO2溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时 NaClO2分解成NaClO3和NaCl。Ba(ClO2)2可溶于水。利用如图所示装置进行实验。
(1)装置①的作用是________ ,装置④中反应生成NaClO2的离子方程式为______ 。
(2)从装置④反应后的溶液中获得NaClO2晶体的操作步骤为:①_______ ,55 ℃蒸发结晶;②趁热过滤;③用38~60 ℃的温水洗涤;④___________________ ,得到成品。如果撤去④中的冷水浴,可能导致产品中混有的杂质是______________ 。
(3)设计实验检验所得NaClO2晶体是否含有杂质Na2SO4:_______________________ 。
(4)为了测定NaClO2粗品的纯度,取10.0 g上述初产品溶于水配成1 L溶液,取出10 mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(NaClO2被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.20 mol·L-1的Na2S2O3标准液滴定,达到注定终点时的现象为:_____________________________________________ 。重复3次,消耗Na2S2O3溶液的体积依次为:19.50 mL、20.50 mL、22.00 mL,则NaClO2粗品的纯度为_____ 。(提示:2Na2S2O3+I2=Na2S4O6+2NaI)。

已知:饱和NaClO2溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时 NaClO2分解成NaClO3和NaCl。Ba(ClO2)2可溶于水。利用如图所示装置进行实验。
(1)装置①的作用是
(2)从装置④反应后的溶液中获得NaClO2晶体的操作步骤为:①
(3)设计实验检验所得NaClO2晶体是否含有杂质Na2SO4:
(4)为了测定NaClO2粗品的纯度,取10.0 g上述初产品溶于水配成1 L溶液,取出10 mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(NaClO2被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.20 mol·L-1的Na2S2O3标准液滴定,达到注定终点时的现象为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】镍是一种常用的催化剂。以红土镍矿(主要含有Fe2O3、FeO、NiO、SiO2等)为原料,制取纳米镍粉,同时获得净水剂黄钠铁矾 的工艺流程如下:
的工艺流程如下:

回答下列问题:
(1)黄钠铁矾 中,铁的化合价为
中,铁的化合价为___________ 价;黄钠铁矾能净水的原因是___________ 。
(2)过滤操作时要遵循“一贴、二低、三靠”的原则,其中“二低”指的是滤纸边缘略低于漏斗口、___________ 。
(3)“沉铁”过程加入Na2CO3的目的是___________ ,控制不同的条件可以得到不同的沉淀,所得沉淀与温度、pH的关系如图所示(图中阴影部分表示的是黄钠铁矾稳定存在区域)。若反应在120℃时进行,加入的Na2CO3偏多,则所得黄钠铁矾中混有的杂质是___________ (填化学式);检验沉铁反应是否完全的方法是___________ 。

(4)“转化”过程,向“过滤II”所得滤液(富含Ni2+)中加入N2H4,控制溶液中NaOH的浓度,可得到不同晶态物质( 、Ni或二者的混合物)。当生成
、Ni或二者的混合物)。当生成 和Ni的物质的量之比为1:2时,该反应的离子方程式为
和Ni的物质的量之比为1:2时,该反应的离子方程式为___________ ;在其他条件不变的情况下,随NaOH浓度增大,产物中Ni的含量增加,原因是___________ 。
(5)化学镀镍是金属表面镀镍的常用方法,以NiSO4为镀液,次亚磷酸钠(NaH2PO2)为还原剂,在90℃的酸性溶液中发生反应,NaH2PO2被氧化为亚磷酸(H3PO3)。写出化学镀镍反应的离子方程式:___________ 。
 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)黄钠铁矾
 中,铁的化合价为
中,铁的化合价为(2)过滤操作时要遵循“一贴、二低、三靠”的原则,其中“二低”指的是滤纸边缘略低于漏斗口、
(3)“沉铁”过程加入Na2CO3的目的是

(4)“转化”过程,向“过滤II”所得滤液(富含Ni2+)中加入N2H4,控制溶液中NaOH的浓度,可得到不同晶态物质(
 、Ni或二者的混合物)。当生成
、Ni或二者的混合物)。当生成 和Ni的物质的量之比为1:2时,该反应的离子方程式为
和Ni的物质的量之比为1:2时,该反应的离子方程式为(5)化学镀镍是金属表面镀镍的常用方法,以NiSO4为镀液,次亚磷酸钠(NaH2PO2)为还原剂,在90℃的酸性溶液中发生反应,NaH2PO2被氧化为亚磷酸(H3PO3)。写出化学镀镍反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)自然界中存在游离态的铁,通常称为____________ 。
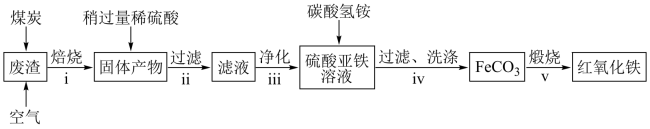
(2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如图(部分操作和条件略):
回答下列问题:
①在步骤i焙烧的目的是________ 。步骤ii的滤渣为_________ 。
②在步骤iii操作中,滴加氨水除Al3+。若常温时由1.0×10-32,此时理论上使Al3+恰好沉淀完全即溶液中c(Al3+)=1×10-5 mol·L-1,则溶液的pH为_______ 。
③在步骤iv中发生的反应中有一种气态产物,它是_________ (写化学式)。
④步骤v中,发生反应的化学方程式为_______________________ 。
(3)工业上,利用硫酸亚铁为原料,通过铁黄(FeOOH,一种不溶于水的黄色固体)制备高铁酸钾(K2FeO4),可降低生产成本且产品质量优。工艺流程如下:
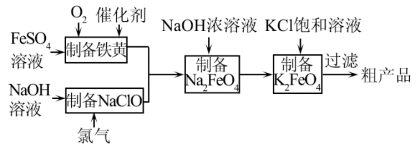
①由图知需先制得高铁酸钠溶液,然后加入饱和KCl溶液转化为高铁酸钾,说明相同温度下溶解度:高铁酸钾______ 高铁酸钠(填“>”或“<”)。
②写出由铁黄制备高铁酸钠的离子方程式_____________________________________ 。
③高铁电池是一种新型二次电池,电解液为强碱溶液,其电池反应为:
3Zn+2K2FeO4+8H2O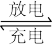 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
放电时电池的正极反应式为___________________________________ 。
(1)自然界中存在游离态的铁,通常称为
(2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如图(部分操作和条件略):

回答下列问题:
①在步骤i焙烧的目的是
②在步骤iii操作中,滴加氨水除Al3+。若常温时由1.0×10-32,此时理论上使Al3+恰好沉淀完全即溶液中c(Al3+)=1×10-5 mol·L-1,则溶液的pH为
③在步骤iv中发生的反应中有一种气态产物,它是
④步骤v中,发生反应的化学方程式为
(3)工业上,利用硫酸亚铁为原料,通过铁黄(FeOOH,一种不溶于水的黄色固体)制备高铁酸钾(K2FeO4),可降低生产成本且产品质量优。工艺流程如下:

①由图知需先制得高铁酸钠溶液,然后加入饱和KCl溶液转化为高铁酸钾,说明相同温度下溶解度:高铁酸钾
②写出由铁黄制备高铁酸钠的离子方程式
③高铁电池是一种新型二次电池,电解液为强碱溶液,其电池反应为:
3Zn+2K2FeO4+8H2O
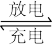 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH放电时电池的正极反应式为
您最近一年使用:0次



