化合物YX2、ZX2中,X、Y、Z的核电荷数小于18;X原子最外能层的p能级中有一个轨道充填了2个电子,Y原子的最外层中p能级的电子数等于前一能层电子总数,且X和Y具有相同的电子层数;Z与X在周期表中位于同一主族。回答下列问题:
(1)X的电子排布式为______________ ,Y的轨道表示式为_________________ ;
(2)YX2的电子式是______________ ,分子构型为_________ ,中心原子发生了____ 杂化。
(3)Y与Z形成的化合物的分子式是_______ ,该化合物中化学键是________ 键(填“极性”或“非极性”),该分子属于__________ 分子(填“极性”或“非极性”)。
(4)Y的氢化物中分子构型为正四面体的是_______ (填名称),键角为_______ ,中心原子的杂化形式为_______ 。
(1)X的电子排布式为
(2)YX2的电子式是
(3)Y与Z形成的化合物的分子式是
(4)Y的氢化物中分子构型为正四面体的是
更新时间:2019-06-11 15:45:36
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】短周期元素X、Y、Z、D与第VIII族元素E的信息如下表:
回答下列问题:
(1)X在元素周期表中的位置为___________ ;Z的氢化物电子式为___________ 。
(2)Y、Z的最高价氧化物对应的水化物酸性较强的是___________ (填化学式)。X、Y、D形成的简单离子的半径由大到小的顺序为___________ (用离子符号表示)。
(3)四种元素的原子序数如下,其中和D不处于同一主族的是___________ (填字母)。
a.5 b.21 c.49 d.81
(4)D的最高价氧化物对应的水化物与强碱反应的离子方程式为___________ 。
(5)E元素与Y元素可形成 和
和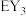 两种化合物,下列说法不正确的是
两种化合物,下列说法不正确的是___________ (填序号)。
①保存 溶液时,需向溶液中加入少量E单质
溶液时,需向溶液中加入少量E单质
② 、
、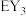 均只能通过化合反应生成
均只能通过化合反应生成
③铜片、碳棒和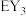 溶液可组成原电池,电子由铜片沿导线流向碳棒
溶液可组成原电池,电子由铜片沿导线流向碳棒
| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物既能溶于强酸又能溶于强碱 |
| E | 单质是生活中常见金属,其中一种氧化物具有磁性 |
(1)X在元素周期表中的位置为
(2)Y、Z的最高价氧化物对应的水化物酸性较强的是
(3)四种元素的原子序数如下,其中和D不处于同一主族的是
a.5 b.21 c.49 d.81
(4)D的最高价氧化物对应的水化物与强碱反应的离子方程式为
(5)E元素与Y元素可形成
 和
和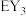 两种化合物,下列说法不正确的是
两种化合物,下列说法不正确的是①保存
 溶液时,需向溶液中加入少量E单质
溶液时,需向溶液中加入少量E单质②
 、
、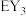 均只能通过化合反应生成
均只能通过化合反应生成③铜片、碳棒和
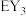 溶液可组成原电池,电子由铜片沿导线流向碳棒
溶液可组成原电池,电子由铜片沿导线流向碳棒
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E均为短周期的主族元素,其原子序数依次增大,A的原子电子层数等于其核外电子数,B与C可形成离子化合物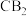 ,D原子的M层电子数是K层电子数的3倍。
,D原子的M层电子数是K层电子数的3倍。
(1)A的元素符号是_______ 。
(2)B的氢化物与E的氢化物相比,较不稳定的是_______ (填化学式)。
(3)C、E组成的化合物的电子式是_______ ,其中所含化学键的类型是_______ 。
(4)B、D、E按原子半径由小到大的顺序排列为_______ (填元素符号)。
(5)E的最高价氧化物对应的水化物是_______ ,它的稀溶液与C的最高价氧化物对应的水化物反应的离子方程式是_______ 。
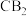 ,D原子的M层电子数是K层电子数的3倍。
,D原子的M层电子数是K层电子数的3倍。(1)A的元素符号是
(2)B的氢化物与E的氢化物相比,较不稳定的是
(3)C、E组成的化合物的电子式是
(4)B、D、E按原子半径由小到大的顺序排列为
(5)E的最高价氧化物对应的水化物是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有U、V、W、X四种前三周期元素,原子序数依次增大,其相关信息如下表:
请回答下列问题:
(1)U、V两种元素组成的一种化合物甲是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则甲分子的空间构型为________ 。
(2)写出W单质的结构式___________ ,其化学键为________ 性共价键:W最简单气态氢化物的电子式为___________ ,分子的空间构型是___________ ,其化学键为___________ 性共价键。
(3)X在周期表中的位置是_______ ,该主族元素的气态氢化物中,沸点最低的是__________ (填化学式)
(4)乙和丙分别是V和X的某种氢化物,这两种氢化物分子中含有有18个电子。乙和丙的化学式分别是________ 、________ 。
| 元素编号 | 相关信息 |
| U | 所处的周期数、族序数分别与其原子序数相等 |
| V | 外层电子数是最内层电子数的两倍 |
| W | 单质中有三对共用电子对 |
| X | 是地壳中含量最多的元素 |
请回答下列问题:
(1)U、V两种元素组成的一种化合物甲是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则甲分子的空间构型为
(2)写出W单质的结构式
(3)X在周期表中的位置是
(4)乙和丙分别是V和X的某种氢化物,这两种氢化物分子中含有有18个电子。乙和丙的化学式分别是
您最近半年使用:0次
【推荐1】近年来,我国航空航天事业成果显著,航空航天材料技术快速发展。
(1)“天宫二号”航天器使用了钛合金,质量轻,强度位于金属之首。钛在周期表中的位置为___ ,基态钛原子的价层电子排布式为___ 。
(2)“北斗三号”导航卫星使用的太阳能电池材料砷化镓是优良的化合物半导体,砷的电负性略___ 镓(填“>”“<”),基态镓原子电子占据最高能级的电子云轮廓图为___ 形。
(3)“C919”飞机机身使用的复合材料——碳纤维和环氧树脂。
①下列电子排布图能表示碳原子的最低能量状态的是___ 。碳在成键时,能将一个2s电子激发进入2p能级而参与成键,写出该激发态原子的核外电子排布式___ 。
A.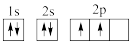 B.
B.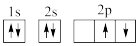
C.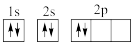 D.
D.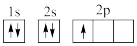
②氧原子的基态原子核外有___ 个未成对电子,有___ 种不同形状的电子云。
(1)“天宫二号”航天器使用了钛合金,质量轻,强度位于金属之首。钛在周期表中的位置为
(2)“北斗三号”导航卫星使用的太阳能电池材料砷化镓是优良的化合物半导体,砷的电负性略
(3)“C919”飞机机身使用的复合材料——碳纤维和环氧树脂。
①下列电子排布图能表示碳原子的最低能量状态的是
A.
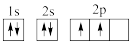 B.
B.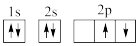
C.
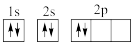 D.
D.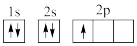
②氧原子的基态原子核外有
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)下面是某些元素的基态原子的电子排布,其中不符合构造原理的是_______ 。
a.[Ar]3d54s1 b.[Ar]3d104s1 c.[Ar]3d44s2 d. [Ar]3d2
(2)某基态原子的价电子轨道表示式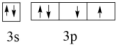 违背了
违背了_______ 原理或规则。
(3)只能有H2、HCl不可能有H3、H2Cl等,表明共价键具有_______ 性;σ键是由两个原子p轨道_______ 式重叠形成的,π键是由原子p轨道_______ 式重叠形成的。
(4)测定分子中含有何种化学键的仪器是_______ 。
(5)比较键角SO2和 的大小,并说明理由:
的大小,并说明理由:_______ 。
(6)接近水的沸点的水蒸气的相对分子质量测定值比按化学式H2O计算出来的相对分子质量大的原因是_______ 。
(7)通常氢键用“X-H…Y”表示,如水分子间的氢键表示为O-H…O。将氨气溶于水,则氨分子与水分子之间形成的氢键表示为_______ 。
(1)下面是某些元素的基态原子的电子排布,其中不符合构造原理的是
a.[Ar]3d54s1 b.[Ar]3d104s1 c.[Ar]3d44s2 d. [Ar]3d2
(2)某基态原子的价电子轨道表示式
 违背了
违背了(3)只能有H2、HCl不可能有H3、H2Cl等,表明共价键具有
(4)测定分子中含有何种化学键的仪器是
(5)比较键角SO2和
 的大小,并说明理由:
的大小,并说明理由:(6)接近水的沸点的水蒸气的相对分子质量测定值比按化学式H2O计算出来的相对分子质量大的原因是
(7)通常氢键用“X-H…Y”表示,如水分子间的氢键表示为O-H…O。将氨气溶于水,则氨分子与水分子之间形成的氢键表示为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分。表中所列字母分别代表一种化学元素。
试回答下列问题:
(1)请写出元素M的价电子排布图___________ 。
(2)D的氢化物极易溶于水的原因___________ 。
(3)由A、C、E形成的CA2E分子结构式为___________ ,含有___________ 个σ键,___________ 个π键。
(4)在基态N中,电子占据的最高能级符号为___________ ,该能级具有的原子轨道数为___________ 。原子核外共有___________ 种不同运动状态的电子,有___________ 种不同能级的电子。
(5)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。MO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是___________ (填“极性”或“非极性”)分子。
| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| G | H | I | J | K | L | ||||||||||||
| M | N | ||||||||||||||||
(1)请写出元素M的价电子排布图
(2)D的氢化物极易溶于水的原因
(3)由A、C、E形成的CA2E分子结构式为
(4)在基态N中,电子占据的最高能级符号为
(5)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。MO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E五种元素是周期表中前四周期元素,且原子序数依次增大。其中A、B、C为同周期的非金属元素,且B、C原子中均有两个未成对电子。D、E为同周期元素且分别位于s区和d区。五种元素所有的s能级电子均为全充满。E的d能级电子数等于A、B、C最高能层的p能级电子数之和。
回答下列问题:
(1)五种元素中,电负性最大的是____ (填元素符号)。
(2)E常有+2、+3两种价态,画出E2+的价电子排布图:____ 。
(3)与BC互为等电子体的分子、离子分别是____ (各举1例),BC的结构式为____ (若有配位键,须用“→”表示出来),实验测得该分子的极性极弱,试从结构方面进行解释:____ 。
(4)自然界中,含A的钠盐是一种天然矿藏,其化学式写作Na2A4O7·10H2O,实际上它的结构单元是由2个H3AO3和2个[A(OH)4]-缩合而成的双六元环,应该写成Na2[A4O5(OH)4]·8H2O,其结构式如图所示,它的阴离子可形成链状结构。
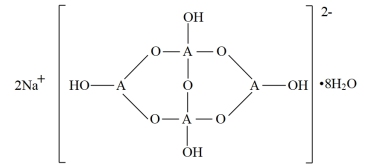
①A原子的杂化方式为____ 。
②Na2[A4O5(OH)4]·8H2O的阴离子由极性键和配位键构成,请在图中用“→”标出其中的配位键____ 。该阴离子通过____ 相互结合形成链状结构。
③已知H3AO3为一元弱酸,根据上述信息,用离子方程式解释分析H3AO3为一元酸的原因:____ 。
(5)E2+在水溶液中以[E(H2O)6]2+形式存在,向含E2+的溶液中加入氨水,可生成[E(NH3)6]2+,[E(NH3)6]2+更稳定,原因是____ 。
回答下列问题:
(1)五种元素中,电负性最大的是
(2)E常有+2、+3两种价态,画出E2+的价电子排布图:
(3)与BC互为等电子体的分子、离子分别是
(4)自然界中,含A的钠盐是一种天然矿藏,其化学式写作Na2A4O7·10H2O,实际上它的结构单元是由2个H3AO3和2个[A(OH)4]-缩合而成的双六元环,应该写成Na2[A4O5(OH)4]·8H2O,其结构式如图所示,它的阴离子可形成链状结构。

①A原子的杂化方式为
②Na2[A4O5(OH)4]·8H2O的阴离子由极性键和配位键构成,请在图中用“→”标出其中的配位键
③已知H3AO3为一元弱酸,根据上述信息,用离子方程式解释分析H3AO3为一元酸的原因:
(5)E2+在水溶液中以[E(H2O)6]2+形式存在,向含E2+的溶液中加入氨水,可生成[E(NH3)6]2+,[E(NH3)6]2+更稳定,原因是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】氮、氟、碘及其化合物应用广泛,回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最低的是______ ( 填序号)。
A.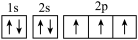 B.
B. 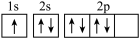 C.
C. 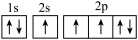 D.
D. 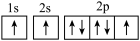
(2) N与F可形成化合物N2F2, 该化合物中所有原子均满足8电子稳定结构,元素的第一电离能大小是N_____ F (填“>”“=”或“<”),1mol N2F2含有的σ键的数目为_____ , 分子中氮原子的杂化轨道类型为_______ 。
(3) NaHF2可用于制无水氟化氢和供雕刻玻璃、木材防腐等用。常温常压下为白色固体,易溶于水,160℃分解。NaHF2中所含作用力的类型有_______ (填序号)。
a.离子键 b.共价键 c.氢键 d.配位键
(4)F与I同主族,已知高碘酸有两种形式,化学式分别为H5IO6(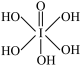 )和HIO4,二者酸性强弱顺序为H5IO6
)和HIO4,二者酸性强弱顺序为H5IO6______ HIO4(填“>”“<"或“=”)。
(5)二氟甲烷(CH2F2) 难溶于水,而三氟甲烷(CHF3) 可溶于水,其可能的原因是________
(6)KI 的晶胞结构如图所示,每个K+周围紧邻的I-个数为____ 个。 KI 晶体的密度为ρg·cm-3, K和I的离子半径分别为R(k+)cm和r(I-)cm,阿伏加德罗常数的值为NA,则KI晶胞的空间利用率为_________ 。

(1)下列氮原子的电子排布图表示的状态中,能量最低的是
A.
 B.
B.  C.
C.  D.
D. 
(2) N与F可形成化合物N2F2, 该化合物中所有原子均满足8电子稳定结构,元素的第一电离能大小是N
(3) NaHF2可用于制无水氟化氢和供雕刻玻璃、木材防腐等用。常温常压下为白色固体,易溶于水,160℃分解。NaHF2中所含作用力的类型有
a.离子键 b.共价键 c.氢键 d.配位键
(4)F与I同主族,已知高碘酸有两种形式,化学式分别为H5IO6(
 )和HIO4,二者酸性强弱顺序为H5IO6
)和HIO4,二者酸性强弱顺序为H5IO6(5)二氟甲烷(CH2F2) 难溶于水,而三氟甲烷(CHF3) 可溶于水,其可能的原因是
(6)KI 的晶胞结构如图所示,每个K+周围紧邻的I-个数为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】开发新型储氢材料是氢能利用的重要研究方向。
(1)化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。请回答:
①H3BNH3中是否存在配位键_______ (填“是”或“否”),B、C、N、O第一电离能由大到小的顺序为_______ ,CH4、H2O、CO2三分子按照键角由大到小的顺序排列为_______ 。
②与(HB=NH)3互为等电子体的分子为_______ (填分子式)。
③人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷。工业上可采用LiAlH4和BCl3在一定条件下制备乙硼烷B2H6,该反应的化学方程式为_______ 。
④在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式。图a为一种无限长链状结构的多硼酸根,其化学式为_______ ,图b为硼砂晶体中阴离子,其中硼原子采取的杂化方式为_______ 。

(2)一种铜合金具有储氢功能
①Cu2+的价层电子排布式为_______ 。
②铜及其它许多金属及其化合物都可以发生焰色反应,其原因是_______ 。
③铜的单质中按ABCABC⋯方式堆积,设铜原子半径为apm,则该晶体的密度为_______ g/cm3(阿伏加德罗常数值为NA)
(1)化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。请回答:
①H3BNH3中是否存在配位键
②与(HB=NH)3互为等电子体的分子为
③人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷。工业上可采用LiAlH4和BCl3在一定条件下制备乙硼烷B2H6,该反应的化学方程式为
④在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式。图a为一种无限长链状结构的多硼酸根,其化学式为

(2)一种铜合金具有储氢功能
①Cu2+的价层电子排布式为
②铜及其它许多金属及其化合物都可以发生焰色反应,其原因是
③铜的单质中按ABCABC⋯方式堆积,设铜原子半径为apm,则该晶体的密度为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】研究发现,在 低压合成甲醇反应(
低压合成甲醇反应(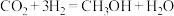 )中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)基态Co原子的价电子排布式为_______ 。基态Mn原子核外有_______ 个未成对电子。
(2)在 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_______ ,原因是_______ 。
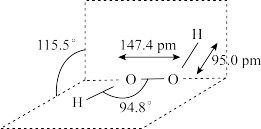
(3) 是一种无色液体,其结构如图所示。根据“相似相溶规则”,
是一种无色液体,其结构如图所示。根据“相似相溶规则”, 在水中的溶解度
在水中的溶解度_______ (填“大于”“小于”或“等于”)其在 中的溶解度。
中的溶解度。
 低压合成甲醇反应(
低压合成甲醇反应(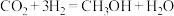 )中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:(1)基态Co原子的价电子排布式为
(2)在
 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为(3)
 是一种无色液体,其结构如图所示。根据“相似相溶规则”,
是一种无色液体,其结构如图所示。根据“相似相溶规则”, 在水中的溶解度
在水中的溶解度 中的溶解度。
中的溶解度。
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】表为周期表的一部分,其中的编号代表对应的元素,请用元素符号 回答下列问题
(1)上述元素中,属于ds区的是_______ (填元素符号)。
(2)不能 说明⑨的金属性比⑩强的是_______ 。
A.⑨与稀盐酸反应比⑩与同条件稀盐酸反应剧烈;
B.⑨单质的熔、沸点比⑩的低;
C.⑨的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强;
D.与非金属单质反应时,⑨原子失电子数目比⑩原子失电子数目少;
(3)④与元素①形成的最简单化合物X是_______ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______ 分子的空间构型为_______ 。
(4)元素⑫与 可形成
可形成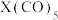 型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于_______ 晶体(填晶体类型)。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ | ⑪ | ⑫ | ⑬ | ⑭ |
(2)
A.⑨与稀盐酸反应比⑩与同条件稀盐酸反应剧烈;
B.⑨单质的熔、沸点比⑩的低;
C.⑨的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强;
D.与非金属单质反应时,⑨原子失电子数目比⑩原子失电子数目少;
(3)④与元素①形成的最简单化合物X是
(4)元素⑫与
 可形成
可形成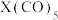 型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】一氧化二氮是一种强大的温室气体,也是人类最早应用于医疗的麻醉剂之一。它可由NH4NO3在加热条件下分解产生。
(1)等电子体理论认为N2O与CO2分子具有相似的结构(包括电子式),则其空间构型是
(2)一定温度下,将足量NH4NO3(s)加入含有催化剂的1L恒容密闭容器中,发生下面两个反应:
反应1:
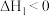
反应2: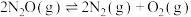 ;
;
测得平衡时容器中气体总压为33.0KPa,且P(O2)为2.4KPa。则平衡时,P(H2O)为
(3)分别向三个体积不变的密闭容器中充入如表所示相应气体,进行反应
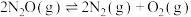 。容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率随温度变化的曲线如图所示:
。容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率随温度变化的曲线如图所示: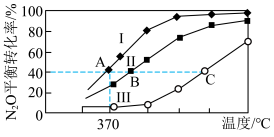
容器 | 物质的量/mol | |||
编号 | 体积/L | N2O | N2 | O2 |
Ⅰ |
| 0.2 | 0 | 0 |
Ⅱ |
| 0.2 | 0 | 0 |
Ⅲ |
| 0.2 | 0 | 0 |
① 、
、 、
、 由大到小的顺序为
由大到小的顺序为
②保持温度不变的情况下,达平衡后再向容器Ⅰ中注入Ar稀释,N2O的分压p(N2O)将
③370℃时该反应的平衡常数为
(4)在Co*的催化作用下,用CO(g)还原N2O(g)以除去污染,反应的化学方程式为:
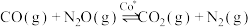 ,其反应历程和能量变化如图所示(逸出后物质认为状态未发生变化,在图中略去)。
,其反应历程和能量变化如图所示(逸出后物质认为状态未发生变化,在图中略去)。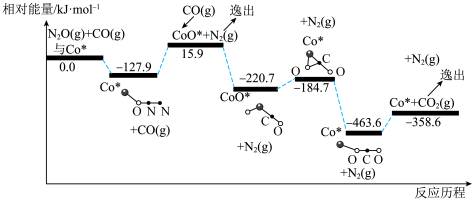
该反应分两步进行:
第一步:
 ;
;
第二步:
(5)若将CO(g)还原N2O(g)的反应设计成如图的原电池装置,则该电池正极的电极反应式为
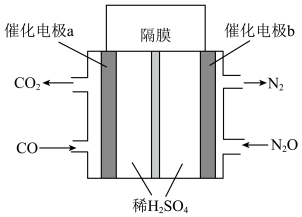
您最近半年使用:0次




