A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为________ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为__________ ,C的元素符号为____________ ;B的外围电子的轨道表示式为___________ 。
(3)D元素的正三价离子的3d轨道为半充满,D的元素符号为________________ ,其基态原子的电子排布式为________________________ 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为________ ,其基态原子的电子排布式为_________ 。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为
(3)D元素的正三价离子的3d轨道为半充满,D的元素符号为
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为
更新时间:2019-06-20 11:40:54
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式______________________________ 。
(2)B基态原子中能量最高的电子,其电子云在空间有________ 个方向,原子轨道呈________ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布为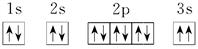 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了_____________________________________ 。
(4)G位于________ 族________ 区,价电子排布式为________ 。
(5)检验F元素的方法是________ ,请用原子结构的知识解释产生此现象的原因是_____________________________________________________________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是 I1=738 kJ/mol;I2=1 451 kJ/mol;I3=7 733 kJ/mol;I4=10 540 kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布为
 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了(4)G位于
(5)检验F元素的方法是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元它们的原子序数依次增大。请根据下列相关信息,回答问题:
(1)写出A的元素符号____ ,D的元素名称____ 。
(2)B基态原子中能量最高的电子,其电子云在空间有____ 个方向,原子轨道呈____ 形。
(3)某同学根据上述信息,推断C基态原子的核外轨道表示式为 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了____ 。
(4)E元素原子核外有____ 种运动状态不同的电子。
(5)G位于____ 族____ 区,价电子排布式为____ 。
(6)检验F元素的方法是____ ,请用原子结构的知识解释产生此现象的原因是____ 。
| A元素原子半径在元素周期表中最小,也是宇宙中最丰富的元素 |
| B元素原子的核外p能级总电子数比s能级总电子数少1个 |
| C元素原子的第一至第四电离能分别是I1=738kJ·mol-1;I2=l451kJ·mol-1;I3=7733kJ·mol-1;I4=10540kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4,原子半径同周期最小 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(4)E元素原子核外有
(5)G位于
(6)检验F元素的方法是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)A基态原子中能量最高的电子,其电子云在空间有___________ 个方向,原子轨道呈___________ 形。
(2)某同学根据上述信息,所画的B电子排布图如图

违背了___________ 原理。
(3)F位于___________ 族___________ 区,其基态原子有___________ 种运动状态。
(4)CD3 中心原子的杂化方式为___________ ,用价层电子对互斥理论推测其分子空间构型为___________ 。
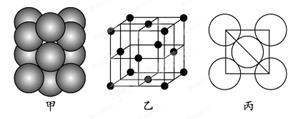
(5)若某金属单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为___________ ,该单质晶体中原子的堆积方式为四种基本堆积方式中的___________ 。若已知该金属的原子半径为d cm,NA代表阿伏加德罗常数,金属的相对原子质量为M,则该晶体的密度为___________ g·cm-3(用字母表示)。
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E是前四周期中电负性最小的元素 |
| F在周期表的第七列 |
(2)某同学根据上述信息,所画的B电子排布图如图

违背了
(3)F位于
(4)CD3 中心原子的杂化方式为
(5)若某金属单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式______________________________ 。
(2)B基态原子中能量最高的电子,其电子云在空间有________ 个方向,原子轨道呈________ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布为 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了_____________________________________ 。
(4)G位于________ 族________ 区,价电子排布式为________ 。
(5)检验F元素的方法是________ ,请用原子结构的知识解释产生此现象的原因是_____________________________________________________________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是 I1=738 kJ/mol;I2=1 451 kJ/mol;I3=7 733 kJ/mol;I4=10 540 kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布为
 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了(4)G位于
(5)检验F元素的方法是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】根据已学物质结构与性质的有关知识,回答下列问题:
(1)基态铁原子的价电子轨道排布图为_______________________ 。铁元素常见的离子有 和
和 ,稳定性
,稳定性 大于
大于 ,其原因是
,其原因是_______________________________________ 。
(2)C、H、N、O四种元素中电负性由大到小的顺序是____________________ (填元素符号下同),前四周期元素中基态原子核外未成对电子数最多的是_________________ 。
(3)一种铜的溴化物晶胞结构如图所示
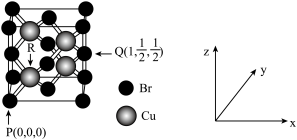
由图可知,该晶体的化学式为_____________ ,与每个Br紧邻Br有____________ 个。
(1)基态铁原子的价电子轨道排布图为
 和
和 ,稳定性
,稳定性 大于
大于 ,其原因是
,其原因是(2)C、H、N、O四种元素中电负性由大到小的顺序是
(3)一种铜的溴化物晶胞结构如图所示

由图可知,该晶体的化学式为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铁(26Fe)、镍(28Ni)的单质及其化合物在医药、材料等领域有着广泛的应用。回答下列问题:
(1)基态Fe原子核外电子排布式为___________ ,Ni位于元素周期表的___________ 区。
(2)乳酸亚铁口服液是缺铁人群补铁保健品,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度分析,Fe2+易被氧化成Fe3+的原因是___________ 。
(3)FeCl3常用作净水剂、刻蚀剂等。
①FeCl3的熔点(306℃)显著低于FeF3的熔点(1000℃)的原因是___________ 。
②FeCl3水溶液中Fe3+可水解生成双核阳离子[Fe2(H2O)8(OH)2]4+,结构如下图,分析其能够形成双核阳离子的原因:___________ 。___________ 。
(1)基态Fe原子核外电子排布式为
(2)乳酸亚铁口服液是缺铁人群补铁保健品,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度分析,Fe2+易被氧化成Fe3+的原因是
(3)FeCl3常用作净水剂、刻蚀剂等。
①FeCl3的熔点(306℃)显著低于FeF3的熔点(1000℃)的原因是
②FeCl3水溶液中Fe3+可水解生成双核阳离子[Fe2(H2O)8(OH)2]4+,结构如下图,分析其能够形成双核阳离子的原因:


您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E为短周期元素且它们的原子序数依次增大,A的核外电子总数与其所在周期序数相同;D原子的L层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L层中未成对电子数与D相同,但有空轨道;D与E同族。请回答下列问题:
(1)A与B、C、D、E元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为_______ ,其中心原子的杂化方式为_______ ;A分别与B、C、D形成的共价化合物中既含有极性键,又含有非极性键的是_______ (填化学式,任意写出三种)。
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的是_______ (写两种即可);酸根离子呈三角锥形的是_______ 。
(3) 分子的空间结构为
分子的空间结构为_______ ;根据原子轨道重叠方式的不同,该分子中共价键的类型为_______ 。
(4)B的一种氢化物的相对分子质量是26,其分子中 键与
键与 键的数目之比为
键的数目之比为_______ 。
(1)A与B、C、D、E元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的是
(3)
 分子的空间结构为
分子的空间结构为(4)B的一种氢化物的相对分子质量是26,其分子中
 键与
键与 键的数目之比为
键的数目之比为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列相关问题:
(1)用“>”或“<”填写下表:
(2)某半导体材料由X、Y两种元素组成,已知X的基态原子4p轨道上只有1个电子,Y的基态原子L层上有3个未成对电子,X位于周期表第_____ 周期____ 族;该半导体材料的化学式为_____ 。
(3)在短周期元素中基态原子的p轨道有1个未成对电子的元素可能是____ (填元素符号),其中核电荷数最大的元素核外电子排布式是________ 。
(4)雷式盐(Reinecke’s salt)结构式如下图所示:

配离子中Cr3+的配体为____ (填化学式),Cr3+与配体间形成的共价键又称为____ .
(1)用“>”或“<”填写下表:
| 电负性 | 第一电离能 | 半径 | 金属性 | 杂化轨道数 |
| Al | S | Na+ | Pb | SO2 |
(3)在短周期元素中基态原子的p轨道有1个未成对电子的元素可能是
(4)雷式盐(Reinecke’s salt)结构式如下图所示:

配离子中Cr3+的配体为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E为原子序数依次增大的五种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子;E为原子序数最小的ds区元素。回答下列问题:
(1)五种元素中电负性最大的是_____ (填元素符号),其中E原子的价电子排布式为________ 。
(2)单质A有两种同素异形体,其中沸点高的是_____ (填分子式),原因是________ 。
(3)C和D反应可生成组成比为1∶3的化合物F,F的立体构型为________ ,中心原子的杂化轨道类型为____ ;化合物D2A的立体构型为______ 。
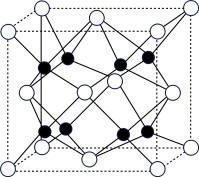
(4)A和B能够形成化合物G,其晶胞结构如图所示,晶胞参数a=0.566 nm,G的化学式为_______ ;晶胞中A原子的配位数为_______ ;已知阿伏加德罗常数的值用NA表示,晶体G的密度为________ g·cm-3(列出计算式)。
(1)五种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1∶3的化合物F,F的立体构型为
(4)A和B能够形成化合物G,其晶胞结构如图所示,晶胞参数a=0.566 nm,G的化学式为

您最近半年使用:0次
【推荐1】X、Y、Z、W是元素周期表前四周期中的常见元素,其原子序数依次增大。X元素的一种核素的质量数为12,中子数为6;Y元素是动植物生长不可缺少的、构成蛋白质的重要组成元素;Z的基态原子核外9个原子轨道上填充了电子且有2个未成对电子,与X不同族;W是一种常见元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。
(1)写出下列元素的名称 X_______ ,Y________ ,Z__________
(2)X—H键和Y—H键属于极性共价键,其中极性较强的是________ (X、Y用元素符号表示)键。X的第一电离能比Y的________ (填“大”或“小”)。
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液反应的化学方程式:________________ 。
(4)W的基态原子的价电子排布式为____________ ;
(5)Y元素的核外电子轨道表示式为___________ 。
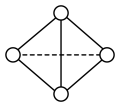
(6)已知一种Y4分子结构如图所示:_______ (填写吸收或放出)_______ kJ
(1)写出下列元素的名称 X
(2)X—H键和Y—H键属于极性共价键,其中极性较强的是
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液反应的化学方程式:
(4)W的基态原子的价电子排布式为
(5)Y元素的核外电子轨道表示式为
(6)已知一种Y4分子结构如图所示:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。
(1)画出A基态原子的核外电子排布图___________ 。
(2)C的基态原子的核外电子排布图 ,该同学所画的电子排布图违背
,该同学所画的电子排布图违背___________ 。
(3)D的基态原子中能量最高的电子,其电子云在空间有___________ 个方向,原子轨道呈___________ 形。
(4)写出C原子的电子排布式___________ ;写出E原子的电子简化排布式___________ 。
(5)请写出F元素价电子排布式___________ 。
(6)写出微粒的核外电子排布式:28Ni___________ ;26Fe3+___________ ;
| A元素原子的核外p电子数比s电子数少3 |
| B元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| C元素基态原子p轨道有3个未成对电子 |
| D原子核外所有p轨道全满或半满 |
| E在该周期中未成对电子数最多 |
| F能形成红色(或砖红色)和黑色的两种氧化物 |
(1)画出A基态原子的核外电子排布图
(2)C的基态原子的核外电子排布图
 ,该同学所画的电子排布图违背
,该同学所画的电子排布图违背(3)D的基态原子中能量最高的电子,其电子云在空间有
(4)写出C原子的电子排布式
(5)请写出F元素价电子排布式
(6)写出微粒的核外电子排布式:28Ni
您最近半年使用:0次
【推荐3】X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,其相关信息如下表:
请用化学用语填空:
(1)X元素位于元素周期表第___________ 周期___________ 族; R是___________ 区的元素。
(2)请写出Q元素基态原子的外围电子排布图:___________ 。
(3)X、Y、Z、M四种元素的原子半径由小到大的顺序是___________ (用元素符号表示)。
(4)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是___________ 。
(5)与M元素成“对角线规则”关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物的水化物反应的化学方程式:___________ ;已知T元素和Q元素的电负性分别为1.5和3.0,则它们形成的化合物是___________ (填“离子化合物”或“共价化合物”)。
| 元素 | 相关信息 |
| X | 原子核外有6种不同运动状态的电子 |
| Y | 基态原子中s电子总数与p电子总数相等 |
| Z | 原子半径在同周期元素中最大 |
| M | 逐级电离能(kJ·mol-1)依次为 578、1 817、2 745、11 575、14 830、18 376 |
| Q | 基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反 |
| R | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
(1)X元素位于元素周期表第
(2)请写出Q元素基态原子的外围电子排布图:
(3)X、Y、Z、M四种元素的原子半径由小到大的顺序是
(4)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是
(5)与M元素成“对角线规则”关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物的水化物反应的化学方程式:
您最近半年使用:0次



