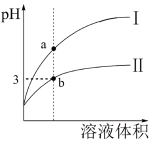
常温下向0.1mol·L-1CH3COOH溶液中加入少量的CH3COONa晶体时,会引起( )
| A.溶液中的c(H+)减小 | B.电离平衡左移,电离常数减小 |
| C.溶液的导电能力减弱 | D.溶液中的c(OH-)减小 |
更新时间:2019-07-24 10:16:21
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】室温下,关于1.0mL0.1mol/L氨水。下列判断正确的是
| A.溶液的pH等于13 |
| B.加入少量NH4Cl固体,c (OH-)不变 |
C.c(OH-)=c ( )+c(H+) )+c(H+) |
| D.与1.0mL0.1mol/L盐酸混合后,溶液呈中性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列物质溶于水中形成1 mol • L-1的溶液时,导电能力最强的是
| A.H2SO4 | B.HCl | C.CH3COOH | D.NH3 • H2O |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】将c(H+)=1×10-2mol/L的CH3COOH和HNO3溶液分别稀释100倍,稀释后两溶液的H+的物质的量浓度分别为a和b,则a和b的关系为
| A.a>b | B.a<b | C.a=b | D.不能确定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列有关水的叙述正确的是( )
| A.水是一种非电解质 |
| B.纯水中c(H+)随着温度的升高而降低 |
| C.由液态水结成冰的过程是一个熵增的过程 |
| D.25℃时浓度相同的氢氧化钠溶液与醋酸钠溶液,水的电离度前者小于后者 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】已知 的醋酸溶液中存在电离平衡:
的醋酸溶液中存在电离平衡: ,要使溶液中pH增大且平衡向正反应方向移动,可以采取的措施是
,要使溶液中pH增大且平衡向正反应方向移动,可以采取的措施是
 的醋酸溶液中存在电离平衡:
的醋酸溶液中存在电离平衡: ,要使溶液中pH增大且平衡向正反应方向移动,可以采取的措施是
,要使溶液中pH增大且平衡向正反应方向移动,可以采取的措施是| A.加少量烧碱固体 | B.升高温度 |
| C.加少量冰醋酸 | D.加少量 固体 固体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列图示与对应的叙述相符的是
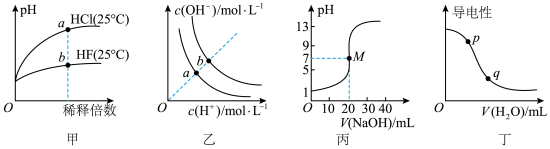

A.由图甲可知,a点 的数值比b点 的数值比b点 的数值大 的数值大 |
B.图乙表示不同温度下水溶液中 和 和 的浓度变化曲线,图中a点对应温度高于b点 的浓度变化曲线,图中a点对应温度高于b点 |
C.图丙表示 溶液滴定 溶液滴定 溶液的滴定曲线,M点水的电离程度最大 溶液的滴定曲线,M点水的电离程度最大 |
| D.图丁表示向醋酸稀溶液中加水时溶液的导电性变化,图中p点醋酸的电离程度大于q点 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】向0.1 mol·L-1 CH3COOH溶液中加入少量的CH3COONa晶体时,会引起
| A.溶液的pH增大 | B.溶液中的c(H+)增大 |
| C.溶液的导电能力减弱 | D.溶液中的c(CH3COO-)减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列操作中,能使电离平衡H2O⇌H++OH-,向逆反应反向移动的是( )
| A.向水中加入2.0mol/L碳酸钠溶液 | B.向水中加入2.0mol/L 氢氧化钠溶液 |
| C.向水中加入2.0mol/L 氯化钠溶液 | D.将水加热到100℃,使pH=6 |
您最近一年使用:0次

 ,下列叙述不正确的是
,下列叙述不正确的是 增大
增大 的
的 溶液加水稀释,溶液中导电粒子的数目增大
溶液加水稀释,溶液中导电粒子的数目增大