醋酸是一种常见的弱酸,为了证明醋酸是弱电解质,某同学开展了题为“醋酸是弱电解质的实验研究”的探究活动。
(1)本课题的研究对象是CH3COOH,研究目的是_____ ,研究方法是实验研究。
(2)该同学设计了如下方案:
A.先配制一定量的0.10mol/L CH3COOH溶液,然后测溶液的pH,若pH大于1,则可证明醋酸为弱电解质。
B.先配制0.01mol/L和0.10mol/L的CH3COOH,分别测他们的pH,若两者的pH相差小于1个单位,则可证明醋酸是弱电解质。
C.先测0.10mol/LCH3COOH的pH,然后将其加热至100℃(不考虑醋酸挥发),再测pH,如果pH变小,则可证明醋酸是弱电解质。
D.配制一定量的CH3COONa溶液,测其pH,若常温下pH大于7,则可证明醋酸是弱电解质。
你认为上述方案可行的是____ (多项选择)
(3)请回答以下两个问题:
①弱电解质的特点是____ (多项选择)
A.在水溶液中全部电离 B.在水溶液中部分电离
C.水溶液呈酸性 D.水溶液中存在电离平衡
②写出醋酸的电离方程式:____ 。
(1)本课题的研究对象是CH3COOH,研究目的是
(2)该同学设计了如下方案:
A.先配制一定量的0.10mol/L CH3COOH溶液,然后测溶液的pH,若pH大于1,则可证明醋酸为弱电解质。
B.先配制0.01mol/L和0.10mol/L的CH3COOH,分别测他们的pH,若两者的pH相差小于1个单位,则可证明醋酸是弱电解质。
C.先测0.10mol/LCH3COOH的pH,然后将其加热至100℃(不考虑醋酸挥发),再测pH,如果pH变小,则可证明醋酸是弱电解质。
D.配制一定量的CH3COONa溶液,测其pH,若常温下pH大于7,则可证明醋酸是弱电解质。
你认为上述方案可行的是
(3)请回答以下两个问题:
①弱电解质的特点是
A.在水溶液中全部电离 B.在水溶液中部分电离
C.水溶液呈酸性 D.水溶液中存在电离平衡
②写出醋酸的电离方程式:
更新时间:2019-10-28 09:13:48
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(A层)下面所列物质中,属于电解质的是________ (填序号,下同),属于强电解质的是________ ,属于弱电解质的是________ ,属于非电解质的是__________ ,溶于水后形成的水溶液能导电的是_______ ,只能在水溶液中导电的电解质是_______ 。①氯化钾 ②乙醇 ③醋酸 ④氨气 ⑤蔗糖⑥铁 ⑦硫酸氢钠 ⑧一水合氨 ⑨氯气
(B层)下面所列物质中,属于电解质的是________ (填序号,下同),属于强电解质的是________ ,属于非电解质的是________ ,能够导电的是__________ ,除⑥外溶于水后形成的水溶液能导电的是_______ ,只能在水溶液中导电的电解质是_______ 。
①NaCl晶体 ②液态SO2 ③液态醋酸 ④汞 ⑤固体BaSO4⑥稀硫酸 ⑦乙醇 ⑧熔融的KNO3 ⑨NH4Cl晶体 ⑩NaOH溶液
(B层)下面所列物质中,属于电解质的是
①NaCl晶体 ②液态SO2 ③液态醋酸 ④汞 ⑤固体BaSO4⑥稀硫酸 ⑦乙醇 ⑧熔融的KNO3 ⑨NH4Cl晶体 ⑩NaOH溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有铁片 NaNO3晶体 NH3·H2O ④Ba(OH)2溶液 ⑤酒精 ⑥SO2六种物质,根据其有关性质,完成下列填空。
(1)属于强电解质的是___ ,(用序号填写,下同)
(2)属于弱电解质的是___ ,
(3)属于非电解质的是___ ,
(4)能导电的是___ .
(5)关于pH=12的Ba(OH)2溶液:
a.Ba(OH)2的物质的量浓度为___ mol⋅L−1
b.取此溶液10mL,稀释到1L,溶液pH=___
c..取此溶液10mL,加入___ mLpH=3的盐酸溶液,使混合液呈中性。(体积变化忽略不计)
d.把此溶液加热至95℃,pH=___ (已知95℃,Kw=1×10-12)
(1)属于强电解质的是
(2)属于弱电解质的是
(3)属于非电解质的是
(4)能导电的是
(5)关于pH=12的Ba(OH)2溶液:
a.Ba(OH)2的物质的量浓度为
b.取此溶液10mL,稀释到1L,溶液pH=
c..取此溶液10mL,加入
d.把此溶液加热至95℃,pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】表中是不同温度下水的离子积数据:
试回答以下问题:
(1)若25<t1<t2,则a____ 1×10-14(填“小于”、“大于”或“等于”)。
(2)在t2℃下,pH=3的稀硫酸溶液中,水电离产生的H+浓度为c(H+)=____ 。
(3)t2℃下,将pH=11的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=____ 。
(4)t2℃下,取相同体积、相同pH的醋酸和盐酸,各稀释100倍后其pH大小关系为:pH(醋酸)___ pH(盐酸)(填“大于”、“小于”或“等于”。下同);稀释后溶液分别用等浓度的NaOH稀溶液中和至pH=7,则消耗的NaOH溶液的体积大小关系为:V(醋酸)____ V(盐酸)。
(5)t2℃时,HF的Ka=6.4×10-4,则此温度下0.1mol•L-1HF溶液的c(H+)=_____ mol•L-1。
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-12 |
(1)若25<t1<t2,则a
(2)在t2℃下,pH=3的稀硫酸溶液中,水电离产生的H+浓度为c(H+)=
(3)t2℃下,将pH=11的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=
(4)t2℃下,取相同体积、相同pH的醋酸和盐酸,各稀释100倍后其pH大小关系为:pH(醋酸)
(5)t2℃时,HF的Ka=6.4×10-4,则此温度下0.1mol•L-1HF溶液的c(H+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,则醋酸的电离平衡 向________ (填“正”或“逆”)反应方向移动;溶液中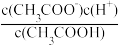 的值
的值________ (填“增大”、“减小”或“不变”)。
(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5mol·L-1;
b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈________ 性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈________ 性,NH4HCO3溶液中物质的量浓度最大的离子是________ (填化学式)。
(3)99 ℃时,KW=1.0×10-12mol2·L-2,该温度下测得0.1 mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为________________ 。
②该温度下,将0.01 mol·L-1H2A溶液稀释到20倍后,溶液的pH=__________ 。
③体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气____________ 。
④将0.1 mol·L-1H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为___________________________ 。
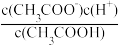 的值
的值(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5mol·L-1;
b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈
(3)99 ℃时,KW=1.0×10-12mol2·L-2,该温度下测得0.1 mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为
②该温度下,将0.01 mol·L-1H2A溶液稀释到20倍后,溶液的pH=
③体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气
| A.盐酸多 | B.H2A多 | C.一样多 | D.无法确定 |
④将0.1 mol·L-1H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定温度下,将冰醋酸加水稀释,溶液的导电能力随加水量变化的曲线如图所示。
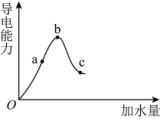
请回答下列问题:
(1)“0”点冰醋酸几乎不能导电的原因是___________ 。
(2)a、b、c三点对应的溶液中,c(H+)由小到大的顺序为___________ 。
(3)a、b、c三点对应的溶液中,c(CH3COOH)的电离程度最大的是___________ 。
(4)若使c点对应的溶液中c(CH3COO-)增大,下列措施,不可行的是___________(填字母,下同)。
(5)在稀释过程中,随着醋酸浓度的降低,下列各量增大的是___________。
(6)为证明醋酸为弱酸,请设计一个合理的实验:___________ 。

请回答下列问题:
(1)“0”点冰醋酸几乎不能导电的原因是
(2)a、b、c三点对应的溶液中,c(H+)由小到大的顺序为
(3)a、b、c三点对应的溶液中,c(CH3COOH)的电离程度最大的是
(4)若使c点对应的溶液中c(CH3COO-)增大,下列措施,不可行的是___________(填字母,下同)。
| A.加热 | B.加KOH固体 | C.加水 | D.加CH3COONa固体 |
| A.c(H+) | B.n(H+) | C.c(CH3COOH) | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在一定温度下,冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。
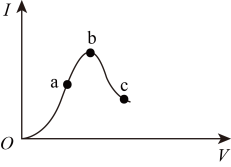
请回答下列问题:
(1)“O”点时醋酸不能导电的原因是_________________________________________ 。
(2)a、b、c三点对应的溶液中,c(H+)由小到大的顺序为______________________ 。
(3)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是______________ 。
(4)若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是____ (填标号、下同)。
A.加热 B.加入NaOH稀溶液C.加入KOH固体
D.加水 E.加入CH3COONa固体 F.加入锌粒
(5)在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是________ 。
A.c(H+) B.n(H+) C.CH3COOH分子数 D.

请回答下列问题:
(1)“O”点时醋酸不能导电的原因是
(2)a、b、c三点对应的溶液中,c(H+)由小到大的顺序为
(3)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是
(4)若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是
A.加热 B.加入NaOH稀溶液C.加入KOH固体
D.加水 E.加入CH3COONa固体 F.加入锌粒
(5)在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是
A.c(H+) B.n(H+) C.CH3COOH分子数 D.

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】①漂白粉 ②HClO ③CO2 ④固体BaSO4 ⑤ 石墨 ⑥小苏打⑦熔融MgCl2 ⑧纯醋酸 ⑨酒精
(1)上述属于非电解质的是____________ (用序号回答,下同)
(2)属于弱电解质的是____________ ;属于强电解质的且能导电的是___________
(1)上述属于非电解质的是
(2)属于弱电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有物质①硫酸铜晶体 ②碳酸钙固体 ③纯磷酸 ④硫化氢 ⑤三氧化硫 ⑥金属镁 ⑦石墨 ⑧固态苛性钾 ⑨氨水 ⑩熟石灰固体 ⑪液态HCl ⑫液态CH3COOH,按下列要求填空。
(1)属于强电解质的是_________________________ (填序号,下同);
(2)属于弱电解质的是________________________ ;
(3)属于非电解质的是________________________ ;
(4)既不是电解质,又不是非电解质的是________ ;
(5)能导电的是____________________________ 。
(1)属于强电解质的是
(2)属于弱电解质的是
(3)属于非电解质的是
(4)既不是电解质,又不是非电解质的是
(5)能导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】水溶液是中学化学的重点研究对象。
(1)水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中的c(H+)=10-9mol·L-1,则该电解质可能是_______ (填序号)。
A.CuSO4 B.HCl C.Na2S D.NaOH E.K2SO4
(2)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性。
①浓度为1.0×10-3 mol·L-1的氨水b L;
②c(OH-)=1.0×10-3 mol·L-1的氨水c L;
③c(OH-)=1.0×10-3 mol·L-1的氢氧化钡溶液d L
则a、b、c、d之间的大小关系是_______ 。
(1)水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中的c(H+)=10-9mol·L-1,则该电解质可能是
A.CuSO4 B.HCl C.Na2S D.NaOH E.K2SO4
(2)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性。
①浓度为1.0×10-3 mol·L-1的氨水b L;
②c(OH-)=1.0×10-3 mol·L-1的氨水c L;
③c(OH-)=1.0×10-3 mol·L-1的氢氧化钡溶液d L
则a、b、c、d之间的大小关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)若把H2O2看成是二元弱酸,请写出在水中的电离方程式:_______
(2)碘也可用作心脏起搏器电源—锂碘电池的材料。该电池反应为2Li(s)+I2(s)=2LiI(s)ΔH
已知:①4Li(s)+O2(g)=2Li2O(s) ΔH1 ②4LiI(s)+O2(g)=2I2(s)+2Li2O(s) ΔH2
则电池反应的ΔH=_______
(3)某温度时,在2 L容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。
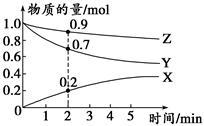
由此分析,该反应的化学方程式为_______ ;从反应开始至2 min时,Z的反应速率为_______ 。
(4)在某温度时,测得0.01 mol·L-1的NaOH溶液的pH=10。在此温度下,将1mL 0.1mol/L KOH溶液加水稀释至1L,则溶液的pH为_______ ,若加水稀释至1000L,则溶液的pH为_______ 。
(2)碘也可用作心脏起搏器电源—锂碘电池的材料。该电池反应为2Li(s)+I2(s)=2LiI(s)ΔH
已知:①4Li(s)+O2(g)=2Li2O(s) ΔH1 ②4LiI(s)+O2(g)=2I2(s)+2Li2O(s) ΔH2
则电池反应的ΔH=
(3)某温度时,在2 L容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。

由此分析,该反应的化学方程式为
(4)在某温度时,测得0.01 mol·L-1的NaOH溶液的pH=10。在此温度下,将1mL 0.1mol/L KOH溶液加水稀释至1L,则溶液的pH为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在菠菜等植物中含有丰富的草酸,草酸对生命活动有重要影响。草酸的学名叫乙二酸,是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料。常温下0.01mL的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示:
(1)草酸(H2C2O4)是一种二元弱酸。写出它在水中的电离方程式:_____ 。
(2)将0.1mol/L草酸溶液中[H2C2O4]、[HC2O ]、[C2O
]、[C2O ]按照由大到小的顺序排列:
]按照由大到小的顺序排列:_____ 。
(3)在H2C2O4溶液稀释过程中,下列物理量始终增大的是_____ 。
(4)KHC2O4溶液中c(H2C2O4)_____ c(C2O )(填>、<、=,下同),若0.1mol/LH2C2O4溶液中第二步电离产生的c(H+)=amol/L,则同浓度的KHC2O4溶液中HC2O
)(填>、<、=,下同),若0.1mol/LH2C2O4溶液中第二步电离产生的c(H+)=amol/L,则同浓度的KHC2O4溶液中HC2O 电离出来的c(H+)
电离出来的c(H+)_____ amol/L
(5)写出草酸钾(K2C2O4)溶液中的电荷守恒关系式_____ ,及物料守恒关系式_____ 。
| 物质 | H2C2O4 | KHC2O4 | K2C2O4 |
| pH | 2.1 | 3.1 | 8.1 |
(2)将0.1mol/L草酸溶液中[H2C2O4]、[HC2O
 ]、[C2O
]、[C2O ]按照由大到小的顺序排列:
]按照由大到小的顺序排列:(3)在H2C2O4溶液稀释过程中,下列物理量始终增大的是
A. | B.c(H+)•c(C2O ) ) |
C.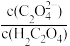 | D.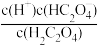 |
 )(填>、<、=,下同),若0.1mol/LH2C2O4溶液中第二步电离产生的c(H+)=amol/L,则同浓度的KHC2O4溶液中HC2O
)(填>、<、=,下同),若0.1mol/LH2C2O4溶液中第二步电离产生的c(H+)=amol/L,则同浓度的KHC2O4溶液中HC2O 电离出来的c(H+)
电离出来的c(H+)(5)写出草酸钾(K2C2O4)溶液中的电荷守恒关系式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】磷是重要的元素,能形成多种含氧酸和含氧酸盐。回答下列问题:
Ⅰ. 亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3 H+ + H2PO
H+ + H2PO 。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
(1)写出亚磷酸钠(Na2HPO3)中磷的化合价___________ 。
(2)当亚磷酸与少量NaOH溶液反应的离子方程式为___________ 。
(3)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式___________ 。
Ⅱ.已知:①次磷酸(H3PO2)是一种一元弱酸;
②常温下,电离平衡常数Ka(H3PO2)=5.9×10-2,Ka(CH3COOH)=1.8×10-5;
(4)下列说法正确的是___________。
(5)次磷酸钠NaH2PO2具有强还原性,是一种很好的化学镀剂。如NaH2PO2能将溶液中的Ni2+还原为Ni,用于化学镀镍。酸性条件下镀镍溶液中发生如下反应:____
___________Ni2++___________H2PO +___________(___________)═___________Ni+___________H2PO
+___________(___________)═___________Ni+___________H2PO +_______(___________)请完成并配平上列的离子方程式。
+_______(___________)请完成并配平上列的离子方程式。
Ⅲ.磷酸是三元弱酸(H3PO4)
(6)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为: 2Ca3(PO4)2+6SiO2 6CaSiO3+P4O10 10C+P4O10
6CaSiO3+P4O10 10C+P4O10  P4+10CO
P4+10CO
若反应生成31 g P4,则反应过程中转移的电子数为___________ (用NA表示阿伏加德罗常数的值)。
Ⅰ. 亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3
 H+ + H2PO
H+ + H2PO 。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。(1)写出亚磷酸钠(Na2HPO3)中磷的化合价
(2)当亚磷酸与少量NaOH溶液反应的离子方程式为
(3)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式
Ⅱ.已知:①次磷酸(H3PO2)是一种一元弱酸;
②常温下,电离平衡常数Ka(H3PO2)=5.9×10-2,Ka(CH3COOH)=1.8×10-5;
(4)下列说法正确的是___________。
A.次磷酸的电离方程式为:H3PO2⇌H++H2PO |
| B.NaH2PO2属于酸式盐 |
| C.浓度均为0.1mol•L-1的次磷酸(H3PO2)与盐酸相比前者导电能力强 |
| D.0.1mol•L-1NaH2PO2溶液的pH比0.1mol•L-1CH3COONa溶液的pH小 |
___________Ni2++___________H2PO
 +___________(___________)═___________Ni+___________H2PO
+___________(___________)═___________Ni+___________H2PO +_______(___________)请完成并配平上列的离子方程式。
+_______(___________)请完成并配平上列的离子方程式。Ⅲ.磷酸是三元弱酸(H3PO4)
(6)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为: 2Ca3(PO4)2+6SiO2
 6CaSiO3+P4O10 10C+P4O10
6CaSiO3+P4O10 10C+P4O10  P4+10CO
P4+10CO若反应生成31 g P4,则反应过程中转移的电子数为
您最近一年使用:0次



