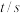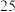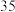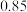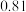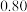(I)已知在448 ℃时,反应H2(g)+I2(g) 2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)
2HI(g)的平衡常数K1为49,则该温度下反应2HI(g) H2(g)+I2(g)的平衡常数K2为
H2(g)+I2(g)的平衡常数K2为______ ;反应 H2(g)+
H2(g)+ I2(g)
I2(g) HI(g)的平衡常数K3为
HI(g)的平衡常数K3为________ 。
(II)在一定体积的密闭容器中进行化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_____ 。
(2)该反应为_____ (填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_____ ℃。
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2mol·L−1,c(H2)=1.5mol·L−1,c(CO)=1mol·L−1,c(H2O)=3mol·L−1,则下一时刻,反应向_____ (填“正向”或“逆向”)进行。
 2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)
2HI(g)的平衡常数K1为49,则该温度下反应2HI(g) H2(g)+I2(g)的平衡常数K2为
H2(g)+I2(g)的平衡常数K2为 H2(g)+
H2(g)+ I2(g)
I2(g) HI(g)的平衡常数K3为
HI(g)的平衡常数K3为(II)在一定体积的密闭容器中进行化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2mol·L−1,c(H2)=1.5mol·L−1,c(CO)=1mol·L−1,c(H2O)=3mol·L−1,则下一时刻,反应向
2019高二上·全国·专题练习 查看更多[2]
更新时间:2019-10-18 23:26:03
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】在5 L的密闭容器中充入2 mol A气体和1 mol B气体,在一定条件下发生反应:2A(g)+B(g)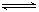 2C(g),10min后达平衡时,在相同温度下测得容器内混合气体的物质的量是反应前的5/6,试计算
2C(g),10min后达平衡时,在相同温度下测得容器内混合气体的物质的量是反应前的5/6,试计算
①A的转化率
②平衡常数K
③10min内生成物C的反应速率
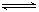 2C(g),10min后达平衡时,在相同温度下测得容器内混合气体的物质的量是反应前的5/6,试计算
2C(g),10min后达平衡时,在相同温度下测得容器内混合气体的物质的量是反应前的5/6,试计算①A的转化率
②平衡常数K
③10min内生成物C的反应速率
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】高炉炼铁中发生的基本反应之一如下:
FeO(固)+CO(气) Fe(固)+CO2(气)ΔH>0
Fe(固)+CO2(气)ΔH>0
(1)则该反应中平衡常数K=__________ 。
(2)已知1100℃时K=0.263。1100℃时测得高炉中c(CO2)=0.025mol·L-1,c(CO)=0.1mol·L-1在这种情况下,该反应是否处于平衡状态______ (选填是或否),此时化学反应速率是v正______ v逆(选填>,<,=)
FeO(固)+CO(气)
 Fe(固)+CO2(气)ΔH>0
Fe(固)+CO2(气)ΔH>0(1)则该反应中平衡常数K=
(2)已知1100℃时K=0.263。1100℃时测得高炉中c(CO2)=0.025mol·L-1,c(CO)=0.1mol·L-1在这种情况下,该反应是否处于平衡状态
您最近一年使用:0次
计算题
|
适中
(0.65)
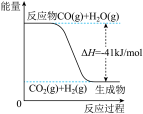
【推荐3】已知工业制氢气的反应为CO(g)+H2O(g)  CO2(g)+H2(g),反应过程中能量变化如下图所示。在500 ℃时的平衡常数K=9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
CO2(g)+H2(g),反应过程中能量变化如下图所示。在500 ℃时的平衡常数K=9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
(1)增加H2O(g)的浓度,CO的转化率将________ (填“增大”、“减小”或“不变”)。
(2)平衡常数的表达式K=________ 。400 ℃时平衡常数K______ 9(填“>”、“<” 或“=”)。
(3)已知2H2(g)+O2(g) 2H2O (g) ΔH=-484 kJ/mol。结合上图写出CO完全燃烧生成CO2的热化学方程式:
2H2O (g) ΔH=-484 kJ/mol。结合上图写出CO完全燃烧生成CO2的热化学方程式:____ 。
 CO2(g)+H2(g),反应过程中能量变化如下图所示。在500 ℃时的平衡常数K=9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
CO2(g)+H2(g),反应过程中能量变化如下图所示。在500 ℃时的平衡常数K=9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
(1)增加H2O(g)的浓度,CO的转化率将
(2)平衡常数的表达式K=
(3)已知2H2(g)+O2(g)
 2H2O (g) ΔH=-484 kJ/mol。结合上图写出CO完全燃烧生成CO2的热化学方程式:
2H2O (g) ΔH=-484 kJ/mol。结合上图写出CO完全燃烧生成CO2的热化学方程式:
您最近一年使用:0次
【推荐1】可逆反应 ⇌
⇌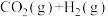 在密闭容器中建立了平衡。当温度为749 K时,
在密闭容器中建立了平衡。当温度为749 K时,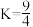 ,问:
,问:
(1)当CO和H2O的起始浓度为2mol/L时,CO的转化率为多少?_____
(2)当CO和H2O的起始浓度分别为2mol/L和6mol/L时,CO的转化率为多少_____
 ⇌
⇌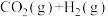 在密闭容器中建立了平衡。当温度为749 K时,
在密闭容器中建立了平衡。当温度为749 K时,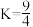 ,问:
,问:(1)当CO和H2O的起始浓度为2mol/L时,CO的转化率为多少?
(2)当CO和H2O的起始浓度分别为2mol/L和6mol/L时,CO的转化率为多少
您最近一年使用:0次
【推荐2】一定温度下,向 恒容容器中充入
恒容容器中充入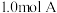 和
和 ,发生反应
,发生反应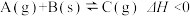 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
(1)前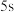 的平均反应速率
的平均反应速率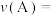
_______ ,达平衡时 的平衡体积分数为
的平衡体积分数为_______ 。
(2)由表中数据计算该温度下该反应的平衡常数为_______ ,随着反应温度升高,该反应的平衡常数_______ (选填“增大”、“减小”或“不变”)。
(3)保持温度不变,起始时向容器中充入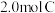 ,达平衡时,
,达平衡时, 的转化率为
的转化率为_______ 。
 恒容容器中充入
恒容容器中充入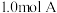 和
和 ,发生反应
,发生反应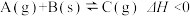 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
|
|
|
|
|
|
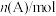 |
|
|
|
|
|
(1)前
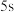 的平均反应速率
的平均反应速率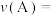
 的平衡体积分数为
的平衡体积分数为(2)由表中数据计算该温度下该反应的平衡常数为
(3)保持温度不变,起始时向容器中充入
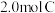 ,达平衡时,
,达平衡时, 的转化率为
的转化率为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。
反应Ⅰ:CO(g)+2H2(g) CH3OH(g),△H1
CH3OH(g),△H1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+ H2O(g),△H2
下表所列数据是反应I在不同温度下的化学平衡常数(K):
(1)在一定条件下将2 molCO和6molH2充入2L的密闭容器中发生反应I,5min后测得c(CO)=0.4 mol/L,计算此段时间的反应速 率(用H2表示)
率(用H2表示)___________ mol/(L·min)。
(2)由表中数据判断△H1_____ 0(填“>”、“<”或“=”)反应,CO2(g)+H2(g)⇌CO(g)+H2O(g)△H3=____ (用△H1和△H2表示)。
(3)若容器容积不变,下列措施可提高反应Ⅰ中CO转化率的是_________ (选字母)。
a.充入CO,使体系总压强增大
b.将CH3OH(g)从体系中分离
e.充入He,使体系总压强增大
d.使用高效催化剂
(4)写出反应Ⅱ的化学平衡常数表达式:K=_________ ;保持恒温恒容的条件下将反应Ⅱ的平衡体系各物质浓度均增加一倍,则化学平衡_________ (填“正向”、“逆向”或“不”)移动,平衡常数K____ (填“变大”、“变小”或“不变”)。
反应Ⅰ:CO(g)+2H2(g)
 CH3OH(g),△H1
CH3OH(g),△H1反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+ H2O(g),△H2
下表所列数据是反应I在不同温度下的化学平衡常数(K):
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.0 | 0.27 | 0.012 |
 率(用H2表示)
率(用H2表示)(2)由表中数据判断△H1
(3)若容器容积不变,下列措施可提高反应Ⅰ中CO转化率的是
a.充入CO,使体系总压强增大
b.将CH3OH(g)从体系中分离
e.充入He,使体系总压强增大
d.使用高效催化剂
(4)写出反应Ⅱ的化学平衡常数表达式:K=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4 (g) 2NO2 (g)△H,随温度升高,混合气体的颜色变深。回答下列问题:
2NO2 (g)△H,随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的△H___ 0(填“﹥”或“﹤”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为___________ mol·L-1·s-1,反应的平衡常数K为_______ mol·L-1。

(2)100℃时,在容积为1.00L的容器中,通入1mol NO2(g)和1mol N2O4(g),此时v正_______ v逆(填“>”或“<”或“=”)。
 2NO2 (g)△H,随温度升高,混合气体的颜色变深。回答下列问题:
2NO2 (g)△H,随温度升高,混合气体的颜色变深。回答下列问题:(1)反应的△H

(2)100℃时,在容积为1.00L的容器中,通入1mol NO2(g)和1mol N2O4(g),此时v正
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】 已知几种共价键的键能数据如下:
(1)通过计算,写出合成氨反应的热化学方程式____________________ 。
(2)某温度下,以1 mol N2和3mol H2作为初始反应物,在体积为2 L的恒容密闭容器中进行合成氨反应,达到平衡时测得反应放热68.1 kJ,试计算N2的转化率__________ 和该温度下的化学平衡常数________________ 。
| 共价键 | N≡N | H-H | N-H |
| 键能/(kJ·mol-1) | 946 | 436 | 390.8 |
(2)某温度下,以1 mol N2和3mol H2作为初始反应物,在体积为2 L的恒容密闭容器中进行合成氨反应,达到平衡时测得反应放热68.1 kJ,试计算N2的转化率
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(1)生产氢气,将水蒸气通过红热的炭即产生水煤气:C(s)+H2O(g) H2(g)+CO(g) ΔH=+131.3kJ•mol-1,写出该反应的平衡常数表达式
H2(g)+CO(g) ΔH=+131.3kJ•mol-1,写出该反应的平衡常数表达式______ 。
(2)已知在400℃时,N2(g)+3H2(g) 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。
①400℃时,2NH3(g) N2(g)+3H2(g)的K'=
N2(g)+3H2(g)的K'=______ (填数值)。
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正______ v(N2)逆(填“>”“<”“=”或“不能确定”)。
③若在恒温下将容器的容积缩小到原来的二分之一,则合成氨反应的平衡______ 移动(填“向左”、“向右”或“不”);反应的∆H______ (填“增大”、“减小”或“不变”)。
(3)水煤气转化反应CO(g)+H2O(g) CO2(g)+H2(g)在一定温度下达到化学平衡。现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如表两组数据:
CO2(g)+H2(g)在一定温度下达到化学平衡。现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如表两组数据:
①平衡常数K(650℃)______ K(900℃)(填“大于”,“小于”或“等于”)
②若将实验2中CO和H2O的物质的量加倍,则平衡时H2的物质的量浓度为______ 。
(1)生产氢气,将水蒸气通过红热的炭即产生水煤气:C(s)+H2O(g)
 H2(g)+CO(g) ΔH=+131.3kJ•mol-1,写出该反应的平衡常数表达式
H2(g)+CO(g) ΔH=+131.3kJ•mol-1,写出该反应的平衡常数表达式(2)已知在400℃时,N2(g)+3H2(g)
 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。①400℃时,2NH3(g)
 N2(g)+3H2(g)的K'=
N2(g)+3H2(g)的K'=②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正
③若在恒温下将容器的容积缩小到原来的二分之一,则合成氨反应的平衡
(3)水煤气转化反应CO(g)+H2O(g)
 CO2(g)+H2(g)在一定温度下达到化学平衡。现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如表两组数据:
CO2(g)+H2(g)在一定温度下达到化学平衡。现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如表两组数据:| 实验编号 | 温度/℃ | 起始量)/mol | 平衡量)/mol | 达到平衡所需时间)/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 5 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
①平衡常数K(650℃)
②若将实验2中CO和H2O的物质的量加倍,则平衡时H2的物质的量浓度为
您最近一年使用:0次