(1)写出下列物质在水溶液中的电离方程式:
CH3COOH____ HClO4_____
Fe(OH)3____ Ba(OH)2_____
NaHSO4____
(2)常温下2.3g乙醇和一定量的氧气混合,点燃恰好完全燃烧,生成液态水和CO2放出68.35kJ热量,则该反应的热化学方程式为:___ 。
(3)根据下列热化学方程式分析,C(s)的燃烧热△H等于___ 。
C(s)+H2O(l)=CO(g)+H2(g) △H1=+175.3kJ·mol-1
2CO(g) + O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g) + O2(g)=2H2O(l) △H3=-571.6kJ·mol-1
CH3COOH
Fe(OH)3
NaHSO4
(2)常温下2.3g乙醇和一定量的氧气混合,点燃恰好完全燃烧,生成液态水和CO2放出68.35kJ热量,则该反应的热化学方程式为:
(3)根据下列热化学方程式分析,C(s)的燃烧热△H等于
C(s)+H2O(l)=CO(g)+H2(g) △H1=+175.3kJ·mol-1
2CO(g) + O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g) + O2(g)=2H2O(l) △H3=-571.6kJ·mol-1
更新时间:2019-11-05 19:06:14
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】完成下列问题
(1)①CH4(g)+ H2O(g) CO(g)+3H2(g) △H1=+206.4kJ/mol
CO(g)+3H2(g) △H1=+206.4kJ/mol
②CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.0kJ/mol
CO2(g)+H2(g) △H2=-41.0kJ/mol
③CH4(g)+H2O(l) CO(g)+3H2(g) △H3
CO(g)+3H2(g) △H3
请回答:
反应①消耗8gCH4(g)吸收的热量_______ 。△H1_______ △H3(填“<”或“>”),书写甲烷与水蒸气反应生成二氧化碳和氢气的热化学方程式_______ 。
(2)CO2是一种廉价的碳资源,其综合利用具有重要意义,CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)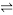 2CO(g)+2H2(g),已知上述反应中相关的化学键键能数据如下:
2CO(g)+2H2(g),已知上述反应中相关的化学键键能数据如下:
则该反应的ΔH=_______ 。
(3)治理NO通常是在氧化剂作用下,将NO氧化成溶解度高的NO2,然后用水或碱液吸收脱氮。下列物质可以用作氧化NO的是_______(填序号)。
(4)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用Rh做催化剂时该反应的过程示意图如下:

过程Ⅰ为_______ 过程(填“吸热”或“放热”)。已知过程Ⅰ的焓变为akJ/mol,过程Ⅱ的焓变为bkJ/mol,则该反应的热化学方程式为_______ 。
(1)①CH4(g)+ H2O(g)
 CO(g)+3H2(g) △H1=+206.4kJ/mol
CO(g)+3H2(g) △H1=+206.4kJ/mol②CO(g)+H2O(g)
 CO2(g)+H2(g) △H2=-41.0kJ/mol
CO2(g)+H2(g) △H2=-41.0kJ/mol③CH4(g)+H2O(l)
 CO(g)+3H2(g) △H3
CO(g)+3H2(g) △H3请回答:
反应①消耗8gCH4(g)吸收的热量
(2)CO2是一种廉价的碳资源,其综合利用具有重要意义,CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)
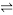 2CO(g)+2H2(g),已知上述反应中相关的化学键键能数据如下:
2CO(g)+2H2(g),已知上述反应中相关的化学键键能数据如下:| 化学键 | C-H | C=O | H-H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=
(3)治理NO通常是在氧化剂作用下,将NO氧化成溶解度高的NO2,然后用水或碱液吸收脱氮。下列物质可以用作氧化NO的是_______(填序号)。
| A.NaCl溶液 | B.NaOH溶液 | C.Na2CO3溶液 | D.KMnO4溶液 |

过程Ⅰ为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】25℃、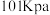 、
、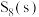 和
和 发生反应依次转化为
发生反应依次转化为 和
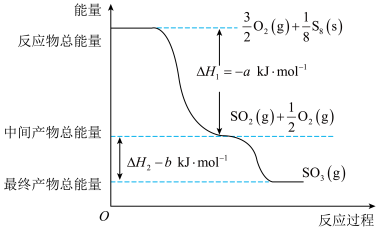
和 。反应过程和能量关系可用如图简单表示(图中的
。反应过程和能量关系可用如图简单表示(图中的 表示生成
表示生成 产物的数据),已知:
产物的数据),已知:
①
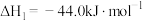 ;
;
②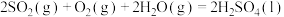
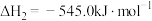 ;
;
(1)结合能量图,书写 与
与 反应生成
反应生成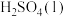 的热化学方程式是
的热化学方程式是___________ 。
(2)计算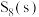 的燃烧热值为
的燃烧热值为___________ 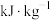 。
。
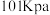 、
、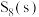 和
和 发生反应依次转化为
发生反应依次转化为 和
和 。反应过程和能量关系可用如图简单表示(图中的
。反应过程和能量关系可用如图简单表示(图中的 表示生成
表示生成 产物的数据),已知:
产物的数据),已知:
①

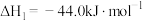 ;
;②
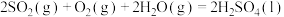
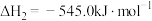 ;
;(1)结合能量图,书写
 与
与 反应生成
反应生成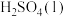 的热化学方程式是
的热化学方程式是(2)计算
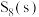 的燃烧热值为
的燃烧热值为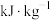 。
。
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25℃、101kPa时,8gCH4完全燃烧生成液态水时放出的热量是445.15kJ,则CH4燃烧的热化学方程式_____________ 。
(2)已知:
C(s)+O2(g) = CO2(g) △H=-437.3kJ·mol -1
H2(g)+1/2O2(g) = H2O(g) △H=-285.8kJ·mol-1
CO(g)+1/2O2(g) = CO2(g) △H=-283.0kJ·mol-1
则煤气化反应C(s)+H2O(g) = CO(g)+H2(g)的焓变△H=___ kJ·mol-1。
(1)在25℃、101kPa时,8gCH4完全燃烧生成液态水时放出的热量是445.15kJ,则CH4燃烧的热化学方程式
(2)已知:
C(s)+O2(g) = CO2(g) △H=-437.3kJ·mol -1
H2(g)+1/2O2(g) = H2O(g) △H=-285.8kJ·mol-1
CO(g)+1/2O2(g) = CO2(g) △H=-283.0kJ·mol-1
则煤气化反应C(s)+H2O(g) = CO(g)+H2(g)的焓变△H=
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】红磷和Cl2发生反应生成PCl3或PCl5。反应过程和能量关系如右图所示(图中的 表示生成1mol产物的数据)。
表示生成1mol产物的数据)。

回答下列问题:
(1)1molPCl3所具有的总能量比1molP和1.5molCl2所具有的总能量___________ (填“高”或“低”)___________ kJ。
(2)PCl3和Cl2化合成PCl5的热化学方程式是___________ 。
(3)P和Cl2反应生成1molPCl5的 =
=___________ 。
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是___________ 。
(5)红磷的同素异形体白磷在氧气中燃烧有如下转化关系。
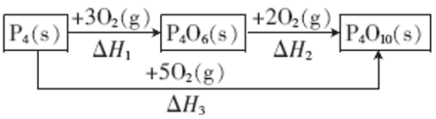
其中 =
=___________ (用含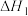 和
和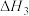 的代数式表示)。
的代数式表示)。
 表示生成1mol产物的数据)。
表示生成1mol产物的数据)。
回答下列问题:
(1)1molPCl3所具有的总能量比1molP和1.5molCl2所具有的总能量
(2)PCl3和Cl2化合成PCl5的热化学方程式是
(3)P和Cl2反应生成1molPCl5的
 =
=(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是
(5)红磷的同素异形体白磷在氧气中燃烧有如下转化关系。

其中
 =
=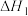 和
和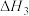 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题
(1)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世瞩目的成就。碳酰肼类化合物[Mn(L)3]( ClO4)2是种优良的含能材料,可作为火箭推进剂的组分,其相关反应的能量变化如图所示,已知△H2= -299kJ/mol,则△H1 (kJ/mol )为_____________
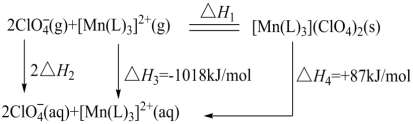
(2)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
(a)CH4(g)+CO2(g) 2CO(g)+2H2(g) ∆H1
2CO(g)+2H2(g) ∆H1
(b)CO2(g)+H2(g) CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2
(c)CH4(g) C(s)+2H2(g) ∆H3
C(s)+2H2(g) ∆H3
(d)2CO(g) CO2(g)+C(s) ∆H4
CO2(g)+C(s) ∆H4
(e)CO(g)+H2(g) H2O(g)+C(s) ∆H5
H2O(g)+C(s) ∆H5
根据盖斯定律,反应a的∆H1=_______ (写出一个代数式即可)。
(3)用H2还原SiCl4蒸汽可制取纯度很高的硅,当反应中有1mol电子转移时吸收59kJ热量,则该反应的热化学方程式为___________________________________ 。
(4)已知含11.2gKOH的稀溶液与1L0.1mol•L-1的H2SO4稀溶液反应放出11.46kJ的热量。请写出KOH的稀溶液与的H2SO4稀溶液发生中和反应,表示中和热的热化学方程式为___________________ 。
(5)1mol CH4(g)完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化如图所示。在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式:________________ 。

(1)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世瞩目的成就。碳酰肼类化合物[Mn(L)3]( ClO4)2是种优良的含能材料,可作为火箭推进剂的组分,其相关反应的能量变化如图所示,已知△H2= -299kJ/mol,则△H1 (kJ/mol )为
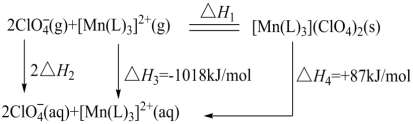
(2)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
(a)CH4(g)+CO2(g)
 2CO(g)+2H2(g) ∆H1
2CO(g)+2H2(g) ∆H1(b)CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2(c)CH4(g)
 C(s)+2H2(g) ∆H3
C(s)+2H2(g) ∆H3(d)2CO(g)
 CO2(g)+C(s) ∆H4
CO2(g)+C(s) ∆H4(e)CO(g)+H2(g)
 H2O(g)+C(s) ∆H5
H2O(g)+C(s) ∆H5根据盖斯定律,反应a的∆H1=
(3)用H2还原SiCl4蒸汽可制取纯度很高的硅,当反应中有1mol电子转移时吸收59kJ热量,则该反应的热化学方程式为
(4)已知含11.2gKOH的稀溶液与1L0.1mol•L-1的H2SO4稀溶液反应放出11.46kJ的热量。请写出KOH的稀溶液与的H2SO4稀溶液发生中和反应,表示中和热的热化学方程式为
(5)1mol CH4(g)完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化如图所示。在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式:

您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】结合CH3COOH或NH3·H2O电离方程式,根据平衡移动原理,分析电离平衡状态是如何建立的?电离平衡的特征有哪些?
CH3COOH
___
NH3·H2O
____
CH3COOH

NH3·H2O

您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】i.已知2mol氢气燃烧生成液态水时放出572kJ热量,反应方程式是2H2(g)+O2(g)=2H2O(l)。请回答下列问题:
①该反应的生成物能量总和___________ (填“大于”、“小于”或“等于”)反应物能量总和。
②若2mol氢气完全燃烧生成水蒸气,则放出的热量___________ (填“>”、“<”或“=”)572kJ。
③与化石燃料相比,利用氢能源有很多优点,请说出其中一点___________ 。
ii.写出下列物质的电离方程式:
NaHCO3___________ ,CH3COOH:___________ ,NH3•H2O:___________ ,H2CO3:___________ 。
①该反应的生成物能量总和
②若2mol氢气完全燃烧生成水蒸气,则放出的热量
③与化石燃料相比,利用氢能源有很多优点,请说出其中一点
ii.写出下列物质的电离方程式:
NaHCO3
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】判断正误:
1.强电解质稀溶液中不存在溶质分子,弱电解质稀溶液中存在溶质分子。(_______)
2.氨气溶于水,当NH3·H2O电离出的c(OH-)=c( )时,表明NH3·H2O电离处于平衡状态。(_______)
)时,表明NH3·H2O电离处于平衡状态。(_______)
3.室温下,由0.1mol·L-1一元碱BOH的pH=10,可知溶液中存在BOH=B++OH-。(_______)
4.电离平衡右移,电解质分子的浓度一定减小,离子浓度一定增大。(_______)
5.25℃时,0.1mol·L-1CH3COOH加水稀释,各离子浓度均减小。(_______)
6.电离平衡向右移动,弱电解质的电离度一定增大。(_______)
7.电离平衡向右移动,电解质的分子浓度一定减小。(_______)
8.Na2SO3溶液与NaHSO3溶液中所含微粒的种类一定相同。(_______)
1.强电解质稀溶液中不存在溶质分子,弱电解质稀溶液中存在溶质分子。(_______)
2.氨气溶于水,当NH3·H2O电离出的c(OH-)=c(
 )时,表明NH3·H2O电离处于平衡状态。(_______)
)时,表明NH3·H2O电离处于平衡状态。(_______)3.室温下,由0.1mol·L-1一元碱BOH的pH=10,可知溶液中存在BOH=B++OH-。(_______)
4.电离平衡右移,电解质分子的浓度一定减小,离子浓度一定增大。(_______)
5.25℃时,0.1mol·L-1CH3COOH加水稀释,各离子浓度均减小。(_______)
6.电离平衡向右移动,弱电解质的电离度一定增大。(_______)
7.电离平衡向右移动,电解质的分子浓度一定减小。(_______)
8.Na2SO3溶液与NaHSO3溶液中所含微粒的种类一定相同。(_______)
您最近半年使用:0次



