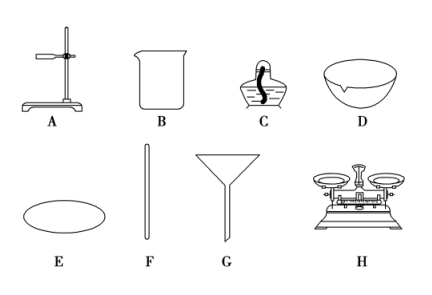
选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
(1)___ 分离氯化钙溶液与沙子的混合物。
(2)___ 从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)___ 分离固体碘单质和食盐的混合物。
(4)___ 分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
A.萃取 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
(1)
(2)
(3)
(4)
更新时间:2019-11-05 10:43:28
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】粗盐中含有泥沙等不溶性杂质和可溶于水的钙离子、镁离子、硫酸根离子等杂质离子。将粗盐溶解过滤后经以下步骤可得精盐:①加入稍过量的 溶液;②加入稍过量的NaOH溶液;③加入稍过量的
溶液;②加入稍过量的NaOH溶液;③加入稍过量的 溶液;④过滤;⑤滴入稀盐酸至无气泡产生;⑥蒸发。回答以下问题:
溶液;④过滤;⑤滴入稀盐酸至无气泡产生;⑥蒸发。回答以下问题:
(1)检验经步骤①后的溶液中还有无 离子的方法是
离子的方法是___________ 。
(2)步骤③加入稍过量 溶液的目的是
溶液的目的是___________ 。
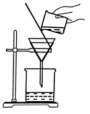
(3)步骤④需用如图装置,装置中有明显的两处错误是___________ 、___________ ,该操作中玻璃棒的作用是___________ 。
(4)步骤⑤滴入稀盐酸产生气泡,该反应的离子方程式为___________ 。
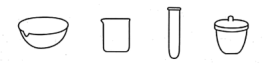
(5)步骤⑥中所用仪器除带铁圈的铁架台、酒精灯、玻璃棒外,还需选用下列仪器中的___________ (填名称)
 溶液;②加入稍过量的NaOH溶液;③加入稍过量的
溶液;②加入稍过量的NaOH溶液;③加入稍过量的 溶液;④过滤;⑤滴入稀盐酸至无气泡产生;⑥蒸发。回答以下问题:
溶液;④过滤;⑤滴入稀盐酸至无气泡产生;⑥蒸发。回答以下问题:(1)检验经步骤①后的溶液中还有无
 离子的方法是
离子的方法是(2)步骤③加入稍过量
 溶液的目的是
溶液的目的是(3)步骤④需用如图装置,装置中有明显的两处错误是

(4)步骤⑤滴入稀盐酸产生气泡,该反应的离子方程式为
(5)步骤⑥中所用仪器除带铁圈的铁架台、酒精灯、玻璃棒外,还需选用下列仪器中的

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
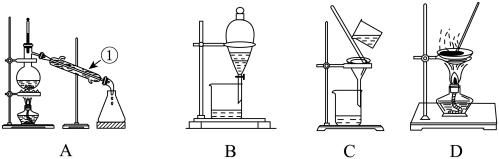
(1)从氯化钾溶液中得到氯化钾固体,选择装置___________ (填代表装置图的字母,下同);除去自来水中的 等杂质,选择装置
等杂质,选择装置___________ 。
(2)从碘水中分离出I2,得到固体碘,选择装置___________ 、___________ 。分离方法的名称为___________ 、___________ 。
(3)装置A中①的名称是___________ ,进水的方向是从___________ (填“上”或“下”)口进水。
(4)装置B在分液时为使液体顺利流下,先进行的操作是___________ ,后再打开下端活塞

(1)从氯化钾溶液中得到氯化钾固体,选择装置
 等杂质,选择装置
等杂质,选择装置(2)从碘水中分离出I2,得到固体碘,选择装置
(3)装置A中①的名称是
(4)装置B在分液时为使液体顺利流下,先进行的操作是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置________ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置_______ 。
(2)从油水混合物中分离出植物油,选择装置________ ,该分离方法的名称为________ 。
(3)装置A中①的名称是________ ,进水的方向是从_______ (填“上”或“下”)口进水。装置B在分液时上层液体从___________ (填仪器名称)的___________ (填“上”或“下”)口流出。

(1)从氯化钾溶液中得到氯化钾固体,选择装置
(2)从油水混合物中分离出植物油,选择装置
(3)装置A中①的名称是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】粗盐提纯实验的科学探究。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
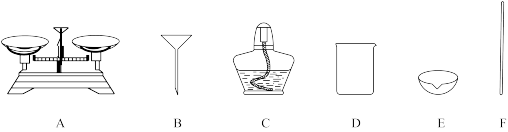
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为___________ (填序号)。
(2)仪器B的名称是___________ ,在实验中三个步骤中都须使用的一种仪器是___________ (填序号)。
(3)称量食盐应放在仪器A的___________ 盘,蒸发时防止液滴飞溅的操作是___________ 。
II.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。
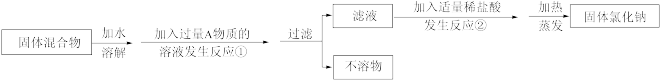
(4)写出A物质的化学式:___________ ,写出A物质的俗称:___________ 。
(5)写出反应②的化学方程式:___________ 。
(6)反应①中加入过量A物质的目的是___________ ;反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度___________ (填“有”或“没有”)影响。
(7)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果___________ (填“增大”、“不变”或“减少”)。
III.化学活动小组查阅资料发现,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质。他们要除去杂质得到精盐,设计了下列实验方案(序号①~⑧表示实验操作,用于沉淀的试剂稍过量 ):
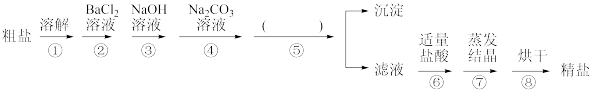
根据上述方案,回答下列问题:
(8)操作①中玻璃棒的作用是___________ 。
(9)第⑤步操作的名称是___________ 。
(10) “蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、石棉网、火柴、玻璃棒、___________ 、酒精灯。
(11)实验中加入“Na2CO3溶液”的目的是___________ 。
(12)利用提供的沉淀试剂,另写出一种添加试剂的操作顺序(填序号):___________ 。
IV.化学兴趣小组同学模拟“海水淡化工业”来制取蒸馏水。实验装置图如下:
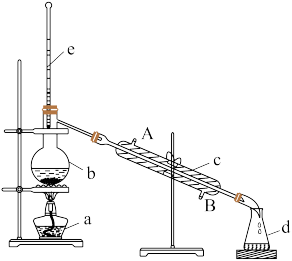
(13)仪器c的名称是___________ 。
(14)该分离混合物的原理是利用___________ 不同,通过加热的方式使其分离。
(15)冷水进水端是___________ 端( 填 A或B )
(16)为防暴沸需向___________ (填仪器名称)中加入___________ (填物品)。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。

(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为
(2)仪器B的名称是
(3)称量食盐应放在仪器A的
II.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。

(4)写出A物质的化学式:
(5)写出反应②的化学方程式:
(6)反应①中加入过量A物质的目的是
(7)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果
III.化学活动小组查阅资料发现,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质。他们要除去杂质得到精盐,设计了下列实验方案(序号①~⑧表示实验操作,用于沉淀的试剂稍

根据上述方案,回答下列问题:
(8)操作①中玻璃棒的作用是
(9)第⑤步操作的名称是
(10) “蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、石棉网、火柴、玻璃棒、
(11)实验中加入“Na2CO3溶液”的目的是
(12)利用提供的沉淀试剂,另写出一种添加试剂的操作顺序(填序号):
IV.化学兴趣小组同学模拟“海水淡化工业”来制取蒸馏水。实验装置图如下:

(13)仪器c的名称是
(14)该分离混合物的原理是利用
(15)冷水进水端是
(16)为防暴沸需向
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置。
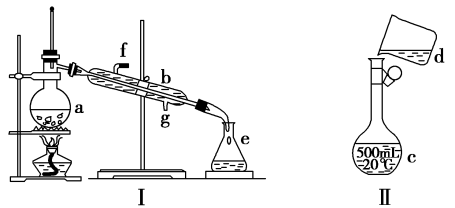
(1)写出下列仪器的名称:a._______ 、c._______ 。
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物冷凝水由(填“f”或“g”)_______ 口通入。
(3)现需配制0.13mol·L1NaOH溶液450mL,装置Ⅱ是某同学转移溶液的示意图。
①根据计算用托盘天平称取NaOH的质量为_______ g。为完成此溶液配制实验需要仪器c、托盘天平(带砝码)、药匙、烧杯、玻璃棒、量筒这六种仪器外,还缺少的必要仪器有 _______ (填名称)
②图Ⅱ中的错误是_______ 。
③配制时,按以下几个步骤进行:计算、称量、溶解、冷却、转移、定容、摇匀、装瓶。操作中还缺少一个重要步骤是_______ 。
④下面操作造成所配NaOH溶液浓度偏高的是_______ 。
A.暴露在空气中称量NaOH的时间太长
B.将砝码放在左盘上,NaOH放在右盘上进行称量(使用游码)
C.向容量瓶转移液体时,容量瓶内含有蒸馏水
D.溶解后未冷却至室温就转移至容量瓶
E.转移液体时玻璃棒的下端放在容量瓶刻度线以上处
F.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
G.定容时俯视刻度线

(1)写出下列仪器的名称:a.
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物冷凝水由(填“f”或“g”)
(3)现需配制0.13mol·L1NaOH溶液450mL,装置Ⅱ是某同学转移溶液的示意图。
①根据计算用托盘天平称取NaOH的质量为
②图Ⅱ中的错误是
③配制时,按以下几个步骤进行:计算、称量、溶解、冷却、转移、定容、摇匀、装瓶。操作中还缺少一个重要步骤是
④下面操作造成所配NaOH溶液浓度偏高的是
A.暴露在空气中称量NaOH的时间太长
B.将砝码放在左盘上,NaOH放在右盘上进行称量(使用游码)
C.向容量瓶转移液体时,容量瓶内含有蒸馏水
D.溶解后未冷却至室温就转移至容量瓶
E.转移液体时玻璃棒的下端放在容量瓶刻度线以上处
F.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
G.定容时俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图实验装置:
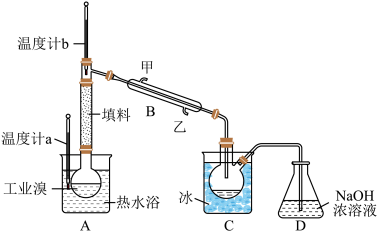
(1)图中仪器B的名称为______ ,冷却水的出口为___ (填写“甲”或“乙”编号)。整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是_________ 。
(2)实验装置气密性良好,要达到提纯溴的目的,操作的关键是___________ 。C中液体的颜色为____ 。为除去该产物中仍残留的少量Cl2,可向其中加入_____ 溶液。(填写化学式)

(1)图中仪器B的名称为
(2)实验装置气密性良好,要达到提纯溴的目的,操作的关键是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐1】某厂排出的废液主要含Zn(NO3)2和AgNO3,为了从中回收金属银和硝酸锌,某中学化学课外活动小组设计了以下的实验步骤
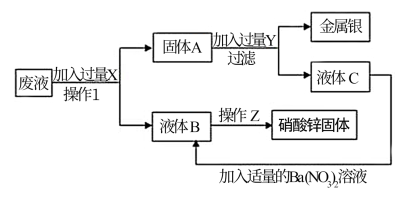
(1)操作I________ (名称)
(2)滤液B的主要成分是______________ 。(写化学式)
(3)请写出A到C的方程式_________________________________________________ 。

(1)操作I
(2)滤液B的主要成分是
(3)请写出A到C的方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】化学实验室要从含少量铜粉的银,锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:

(1)操作a的名称是___________ 。
(2)A、B、C三种金属的活动性顺序为___________ ,金属C是___________ 。
(3)已知A的硫酸盐中A元素显+2价,判断出A元素并用其元素符号写出步骤①反应的化学方程式:___________ 。

(1)操作a的名称是
(2)A、B、C三种金属的活动性顺序为
(3)已知A的硫酸盐中A元素显+2价,判断出A元素并用其元素符号写出步骤①反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)现有三种有机物 丙烷、
丙烷、 二甲醚
二甲醚 和
和 乙醇
乙醇 ,沸点数据如下
,沸点数据如下
(i)乙醇沸点高于二甲醚的原因是___________
(ii)二甲醚沸点高于丙烷的原因是___________
(2) 本草衍义
本草衍义 中对精制砒霜
中对精制砒霜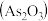 过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒盐上飞着覆器,遂凝结累然下垂如乳尖,长者为胜,平短者次之。”
过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒盐上飞着覆器,遂凝结累然下垂如乳尖,长者为胜,平短者次之。”
(i)文中涉及的操作方法是______
A.蒸馏 升华
升华  干馏
干馏 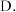 萃取
萃取 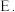 精馏
精馏 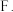 重结晶
重结晶
(ii)由以上工艺,砒霜最可能的晶体类型是______
A.原子晶体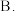 分子晶体
分子晶体  离子晶体
离子晶体  金属晶体
金属晶体  混合晶体
混合晶体
(iii)砒霜是剧毒物质,法庭医学分析上常用马氏试砷法来证明是否砒霜中毒:把试样与锌和硫酸混和,若试样中含有砒霜,则生成砷化氢气体,反应的化学方程式为___________ 。
(1)现有三种有机物
 丙烷、
丙烷、 二甲醚
二甲醚 和
和 乙醇
乙醇 ,沸点数据如下
,沸点数据如下| 沸点 | 78℃ | -23℃ | -42.09℃ |
| 物质 | CH3CH2OH | H3COCH3 | CH3CH2CH3 |
(ii)二甲醚沸点高于丙烷的原因是
(2)
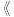 本草衍义
本草衍义 中对精制砒霜
中对精制砒霜 过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒盐上飞着覆器,遂凝结累然下垂如乳尖,长者为胜,平短者次之。”
过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒盐上飞着覆器,遂凝结累然下垂如乳尖,长者为胜,平短者次之。”(i)文中涉及的操作方法是
A.蒸馏
 升华
升华  干馏
干馏  萃取
萃取 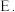 精馏
精馏 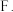 重结晶
重结晶(ii)由以上工艺,砒霜最可能的晶体类型是
A.原子晶体
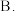 分子晶体
分子晶体  离子晶体
离子晶体 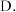 金属晶体
金属晶体  混合晶体
混合晶体(iii)砒霜是剧毒物质,法庭医学分析上常用马氏试砷法来证明是否砒霜中毒:把试样与锌和硫酸混和,若试样中含有砒霜,则生成砷化氢气体,反应的化学方程式为
您最近一年使用:0次
【推荐2】海带中含有碘元素,从海带中提取碘并验证其性质。提取过程如图所示:
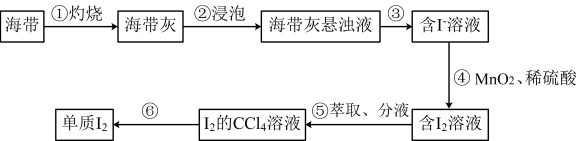
(1)验证“含 溶液”和“含
溶液”和“含 溶液”中含有的
溶液”中含有的 和
和 所需的试剂分别是
所需的试剂分别是______ 和_______ 。
(2)步骤④的反应中 被还原为
被还原为 ,反应的离子方程式为
,反应的离子方程式为__________ ; 、稀硫酸可用
、稀硫酸可用_______ 代替。
a. b.
b. c.
c. 、稀硫酸 d.
、稀硫酸 d.
(3)海带灰中含有的可溶性硫酸盐、碳酸盐等,在实验步骤___________ (填序号)中实现与碘分离。
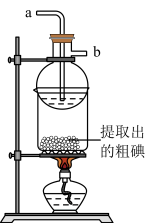
(4)某同学制得的粗碘中含有少量 ,对粗碘进行提纯的装置如图所示,采用的分离方法是
,对粗碘进行提纯的装置如图所示,采用的分离方法是________ ;a、b为冷凝水进出口,其中__________ (填“a”或“b”)接水龙头,最终能得到较多较高纯度的单质碘。

(1)验证“含
 溶液”和“含
溶液”和“含 溶液”中含有的
溶液”中含有的 和
和 所需的试剂分别是
所需的试剂分别是(2)步骤④的反应中
 被还原为
被还原为 ,反应的离子方程式为
,反应的离子方程式为 、稀硫酸可用
、稀硫酸可用a.
 b.
b. c.
c. 、稀硫酸 d.
、稀硫酸 d.
(3)海带灰中含有的可溶性硫酸盐、碳酸盐等,在实验步骤
(4)某同学制得的粗碘中含有少量
 ,对粗碘进行提纯的装置如图所示,采用的分离方法是
,对粗碘进行提纯的装置如图所示,采用的分离方法是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】正丁醛是一种化工原料。某实验小组利用如图装置合成正丁醛。
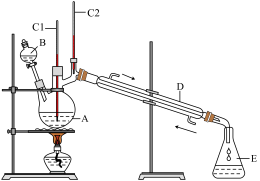
发生的反应如下:CH3CH2CH2CH2OH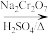 CH3CH2CH2CHO,反应物和产物的相关数据列表如下:
CH3CH2CH2CHO,反应物和产物的相关数据列表如下:
实验步骤如下:将6.0 g Na2Cr2O7放入100 mL烧杯中,加30 mL水溶解,与5 mL浓硫酸形成混合溶液,将所得溶液小心转移至B中。在A中加入4.0 g正丁醇和几粒沸石,加热。当有蒸气出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95 ℃,在E中收集90 ℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77 ℃馏分,产量2.0 g。回答下列问题:
(1)实验中,Na2Cr2O7溶液和浓硫酸添加的顺序为_______ 。
(2)加入沸石的作用是_____________ 。若加热后发现未加沸石,应采取的正确方法是__________ 。
(3)上述装置图中,D仪器的名称是________ ,E仪器的名称是________ 。
(4)分液漏斗使用前必须进行的操作是________ 。
(5)将正丁醛粗产品置于分液漏斗中分水时,正丁醛在_______ 层(填“上”或“下”)。
(6)反应温度应保持在90~95 ℃,其原因是___________ 。
(7)本实验中,正丁醛的产率为________ %(结果保留两位小数)。

发生的反应如下:CH3CH2CH2CH2OH
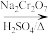 CH3CH2CH2CHO,反应物和产物的相关数据列表如下:
CH3CH2CH2CHO,反应物和产物的相关数据列表如下:| 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.810 9 | 微溶 |
| 正丁醛 | 75.7 | 0.801 7 | 微溶 |
(1)实验中,Na2Cr2O7溶液和浓硫酸添加的顺序为
(2)加入沸石的作用是
(3)上述装置图中,D仪器的名称是
(4)分液漏斗使用前必须进行的操作是
(5)将正丁醛粗产品置于分液漏斗中分水时,正丁醛在
(6)反应温度应保持在90~95 ℃,其原因是
(7)本实验中,正丁醛的产率为
您最近一年使用:0次