下列有关难溶电解质及其溶度积常数Ksp的说法正确的是
| A.常温下,向BaCO3饱和溶液中加入Na2CO3固体,BaCO3的Ksp 减小 |
| B.Ksp越大,难溶电解质的溶解能力越强 |
| C.过滤沉淀时,用稀盐酸洗涤AgCl沉淀比用水洗涤损耗的AgCl少 |
| D.工业上去除废水中的重金属离子,只能使用可溶性沉淀剂,如Na2S、(NH4)2 S等 |
更新时间:2019-11-20 15:00:55
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】根据下列操作及现象,所得结论正确的是
| 序号 | 操作及现象 | 结论 |
| A | 将 氨水稀释成 氨水稀释成 测得 测得 由11.1变成10.6 由11.1变成10.6 | 稀释后, 的电离程度减小 的电离程度减小 |
| B | 向 冷水和沸水中分别滴入5滴 冷水和沸水中分别滴入5滴 饱和溶液,前者为黄色,后者为红褐色 饱和溶液,前者为黄色,后者为红褐色 | 温度升高, 的水解程度增大 的水解程度增大 |
| C | 常温下,测得饱和 溶液的 溶液的 大于饱和 大于饱和 溶液 溶液 | 常温下水解程度: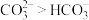 |
| D | 将固体 加入 加入 溶液中,一段时间后,检验固体成分为 溶液中,一段时间后,检验固体成分为 | 同温度下溶解度: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】T℃时,三种盐的沉淀溶解平衡曲线如图所示,已知pM为阳离子浓度的负对数,pR为阴离子浓度的负对数,下列说法正确的是


| A.Y点:c(Ca2+)>c(SO42-),Z点:c(CO32-)>c(Mn2+) |
| B.溶度积:Ksp(MnCO3)>Ksp(CaCO3)>Ksp(CaSO4) |
| C.X点对应的CaCO3溶液为不饱和溶液,可以继续溶解CaCO3 |
D.T℃时,CaSO4(s)+CO32-(aq) CaCO3(s)+SO42-(aq)的平衡常数K的数量级为103 CaCO3(s)+SO42-(aq)的平衡常数K的数量级为103 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验方案、现象和结论都正确的是
| 选项 | 探究方案 | 现象 | 结论 |
| A | 常温下,向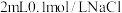 溶液中滴加2滴 溶液中滴加2滴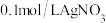 溶液,充分反应后,再滴加4滴0.1 溶液,充分反应后,再滴加4滴0.1 溶液 溶液 | 先产生白色沉淀,后沉淀颜色由白色逐渐转为黄色 | 证明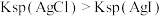 |
| B | 常温下,测定等体积的盐酸和醋酸溶液的 | 醋酸溶液的pH大于盐酸 | 证明醋酸是弱电解质 |
| C | 将 和 和 的混合气体通入密闭的注射器,压缩活塞 的混合气体通入密闭的注射器,压缩活塞 | 混合气体的颜色变浅 | 增大压强会使化学平衡向气体体积缩小的方向移动 |
| D | 向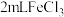 溶液中滴加 溶液中滴加 等浓度的 等浓度的 溶液,充分反应后,再滴加KSCN溶液,观察现象 溶液,充分反应后,再滴加KSCN溶液,观察现象 | 溶液最终变为血红色 |  溶液与 溶液与 溶液的反应为可逆反应 溶液的反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关叙述不正确的是( )
①在100 ℃、101 kPa条件下,液态水汽化热为40.69 kJ·mol-1,则H2O(g)===H2O(l) ΔH=+40.69 kJ·mol-1
②已知25 ℃时,MgCO3的Ksp=6.82×10-6,则在该温度下,含有固体MgCO3的溶液中,无论c(Mg2+)与c(CO )是否相等,总有c(Mg2+)·c(CO
)是否相等,总有c(Mg2+)·c(CO )=6.82×10-6
)=6.82×10-6
③已知:
则反应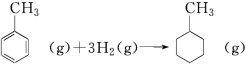 ΔH=-384 kJ·mol-1
ΔH=-384 kJ·mol-1
④常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,则NH3·H2O的电离被抑制,溶液pH减小
①在100 ℃、101 kPa条件下,液态水汽化热为40.69 kJ·mol-1,则H2O(g)===H2O(l) ΔH=+40.69 kJ·mol-1
②已知25 ℃时,MgCO3的Ksp=6.82×10-6,则在该温度下,含有固体MgCO3的溶液中,无论c(Mg2+)与c(CO
 )是否相等,总有c(Mg2+)·c(CO
)是否相等,总有c(Mg2+)·c(CO )=6.82×10-6
)=6.82×10-6③已知:
| 共价键 | C—C | C===C | C—H | H—H |
| 键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
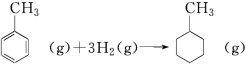 ΔH=-384 kJ·mol-1
ΔH=-384 kJ·mol-1④常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,则NH3·H2O的电离被抑制,溶液pH减小
| A.①② | B.③④ | C.②④ | D.①③ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,向10mL0.1mol·L-1MCl2溶液中滴加 0.1mol·L-1的Na2S溶液,滴加过程中溶液中-lgc(M2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法正确的是
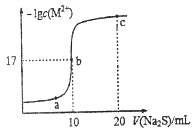
已知:Ksp(NS)=4.0×10-25

已知:Ksp(NS)=4.0×10-25
| A.该温度下Ksp(MS)=1.0×10-34 |
| B.Na2S溶液中:c(H+)+c(HS-)+c(H2S)=c(OH-) |
| C.a、b、c三点中,水的电离程度最大的为b点 |
| D.向NS的悬浊液中加入MCl2溶液,不可能实现NS沉淀转化为MS沉淀 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列陈述I与陈述II均正确, 且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | SO2具有氧化性 | 在葡萄酒酿制过程中添加适量SO2 |
| B | 人体需要补充铁单质 | 酱油中加入铁强化剂 |
| C | NaHCO3受热易分解生成CO2气体 | 用纯碱焙制糕点 |
| D | S2-能与Cu2+、Hg2+生成难溶的硫化物沉淀 | 用Na2S处理 含Cu2+、Hg2+的工业废水 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
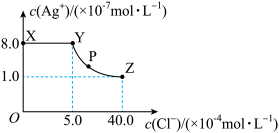
【推荐2】一定温度下,向足量的AgBr固体中加入100mL水,充分搅拌,慢慢加入NaCl固体,随着 增大,溶液中
增大,溶液中 的变化曲线如图所示。下列说法不正确的是
的变化曲线如图所示。下列说法不正确的是
 增大,溶液中
增大,溶液中 的变化曲线如图所示。下列说法不正确的是
的变化曲线如图所示。下列说法不正确的是
A.该温度下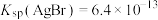 |
B.从Y点到Z点发生的离子反应为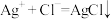 |
| C.AgBr与AgCl在一定条件下可以相互转化 |
D.P点溶液中 |
您最近半年使用:0次

 和
和 的水解程度
的水解程度 的
的 和
和 溶液的
溶液的 与
与 的
的 即大小
即大小 溶液中滴入过量
溶液中滴入过量 溶液,再滴加
溶液,再滴加 溶液
溶液 反应是否为可逆反应
反应是否为可逆反应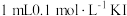 溶液中加入
溶液中加入
 溶液
溶液 的吸氧腐蚀产物是否有
的吸氧腐蚀产物是否有
 溶液
溶液

