多晶硅是制作光伏电池的关键材料。将SiCl4氢化为SiHCl3的热化学方程式为:3SiCl4+2H2(g)+Si(s) 4SiHCl3(g) △H2<0
4SiHCl3(g) △H2<0
(1)该反应是____________ 反应(填吸热、放热)
(2)在相同条件,相同时间t时,不同温度下该反应中SiCl4转化率如图所示。下列叙述正确的是________________ (填序号)。
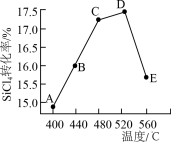
a.相同时间t内,A点的平均反应速率大于B点
b.相同时间t时,B点:v正>v逆
c.相同时间t时,v逆:C点大于A点
d.工业生产中采用了适宜温度:480~520°C
(3)为了增大化学反应速率,除加入催化剂、升高温度外还可以采用哪些方法和措施:___ 。(只写出一条)
 4SiHCl3(g) △H2<0
4SiHCl3(g) △H2<0(1)该反应是
(2)在相同条件,相同时间t时,不同温度下该反应中SiCl4转化率如图所示。下列叙述正确的是

a.相同时间t内,A点的平均反应速率大于B点
b.相同时间t时,B点:v正>v逆
c.相同时间t时,v逆:C点大于A点
d.工业生产中采用了适宜温度:480~520°C
(3)为了增大化学反应速率,除加入催化剂、升高温度外还可以采用哪些方法和措施:
更新时间:2019-12-01 23:02:29
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.反应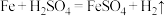 的能量变化趋势如图所示:
的能量变化趋势如图所示:
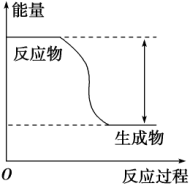
(1)该反应为_______ 反应 填“吸热”或“放热”
填“吸热”或“放热” 。
。
(2)若要使该反应的反应速率加快,下列措施可行的是_______  填序号
填序号 。
。
A.改铁片为铁粉 B.改稀硫酸为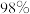 的浓硫酸 C.升高温度
的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_______  填“正”或“负”
填“正”或“负” 极。铜片上的现象为
极。铜片上的现象为_______ ,该极上发生的电极反应为_______ ,外电路中电子由_______ 极 填“正”或“负”,下同
填“正”或“负”,下同 向
向_______ 极移动。
Ⅱ.将铁粉、铜粉、 溶液和
溶液和 溶液混合于某容器中充分反应
溶液混合于某容器中充分反应 假定容器不参与反应
假定容器不参与反应 。试判断下列情况下,溶液中存在的金属离子和金属单质。
。试判断下列情况下,溶液中存在的金属离子和金属单质。
(4)若铁粉有剩余,则容器中不可能有的离子是_______ ;铜单质_______  填“一定”或“可能”
填“一定”或“可能” 存在。
存在。
(5)若氯化铜有剩余,则容器中还可能有的离子是_______ ;铜单质_______  填“一定”或“可能”
填“一定”或“可能” 存在。
存在。
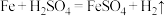 的能量变化趋势如图所示:
的能量变化趋势如图所示: 
(1)该反应为
 填“吸热”或“放热”
填“吸热”或“放热” 。
。(2)若要使该反应的反应速率加快,下列措施可行的是
 填序号
填序号 。
。A.改铁片为铁粉 B.改稀硫酸为
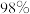 的浓硫酸 C.升高温度
的浓硫酸 C.升高温度(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
 填“正”或“负”
填“正”或“负” 极。铜片上的现象为
极。铜片上的现象为 填“正”或“负”,下同
填“正”或“负”,下同 向
向Ⅱ.将铁粉、铜粉、
 溶液和
溶液和 溶液混合于某容器中充分反应
溶液混合于某容器中充分反应 假定容器不参与反应
假定容器不参与反应 。试判断下列情况下,溶液中存在的金属离子和金属单质。
。试判断下列情况下,溶液中存在的金属离子和金属单质。(4)若铁粉有剩余,则容器中不可能有的离子是
 填“一定”或“可能”
填“一定”或“可能” 存在。
存在。(5)若氯化铜有剩余,则容器中还可能有的离子是
 填“一定”或“可能”
填“一定”或“可能” 存在。
存在。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.(1)下列变化中属于吸热反应 的是__ (填字母序号)。
①液态水汽化②将胆矾加热变为白色粉末③苛性钠固体溶于水;④氯酸钾分解制氧气⑤生石灰跟水反应生成熟石灰⑥干冰升华
A.①② B.②④ C.③ D.①⑥
Ⅱ.蕴藏在海底的大量“可燃冰”,其开发利用是当前解决能源危机的重要课题。CH4(g)+2H2O(g) CO2(g)+4H2(g)。若1molCH4气体
CO2(g)+4H2(g)。若1molCH4气体完全 反应时,吸收akJ热量。
(2)写出甲烷的结构式___ 。
(3)C=O的键能为___ kJ/mol(用含a、b、c、d的式子表示)。
(4)恒温条件下,在体积恒为0.5L的密闭容器中通入一定量甲烷和水蒸气,发生上述反应.测得甲烷物质的量随时间变化如表所示。0~10min内用水蒸气的浓度变化表示该反应的平均速率为v(H2O)=___ 。
(5)若想加快该反应的速率,可采取的措施有___ (任写一项即可)。
(6)恒温恒容情况下,下列叙述能说明此反应达到平衡状态的是___ 。
A.混合气体的平均相对分子质量保持不变
B.CO2和H2的体积分数比为1:4
C.混合气体的密度保持不变
D.生成1molCO2的同时,有4molH—H键断裂
①液态水汽化②将胆矾加热变为白色粉末③苛性钠固体溶于水;④氯酸钾分解制氧气⑤生石灰跟水反应生成熟石灰⑥干冰升华
A.①② B.②④ C.③ D.①⑥
Ⅱ.蕴藏在海底的大量“可燃冰”,其开发利用是当前解决能源危机的重要课题。CH4(g)+2H2O(g)
 CO2(g)+4H2(g)。若1molCH4气体
CO2(g)+4H2(g)。若1molCH4气体| 化学键 | C—H | H—H | H—O |
| 键能kJ/mol | b | c | d |
(3)C=O的键能为
(4)恒温条件下,在体积恒为0.5L的密闭容器中通入一定量甲烷和水蒸气,发生上述反应.测得甲烷物质的量随时间变化如表所示。0~10min内用水蒸气的浓度变化表示该反应的平均速率为v(H2O)=
| 时间/min | 0 | 10 | 20 | 40 | 50 | 60 |
| n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 | 0.10 |
(6)恒温恒容情况下,下列叙述能说明此反应达到平衡状态的是
A.混合气体的平均相对分子质量保持不变
B.CO2和H2的体积分数比为1:4
C.混合气体的密度保持不变
D.生成1molCO2的同时,有4molH—H键断裂
您最近一年使用:0次
【推荐3】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用_______ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面_______ (填字母)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水
(3)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是 和
和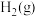 反应生成
反应生成 过程中能量变化示意图。请写出
过程中能量变化示意图。请写出 和
和 反应的热化学方程式:
反应的热化学方程式:_______ ;

(4)温度在150℃以上时, 便迅速分解为
便迅速分解为 和
和 ,发射火箭时用过氧化氢作强氧化剂就是利用这个原理,已知:
,发射火箭时用过氧化氢作强氧化剂就是利用这个原理,已知:
a.
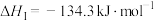
b.
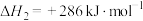
则反应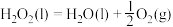 的
的
_______ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.浓硫酸和水
(3)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是
 和
和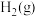 反应生成
反应生成 过程中能量变化示意图。请写出
过程中能量变化示意图。请写出 和
和 反应的热化学方程式:
反应的热化学方程式:
(4)温度在150℃以上时,
 便迅速分解为
便迅速分解为 和
和 ,发射火箭时用过氧化氢作强氧化剂就是利用这个原理,已知:
,发射火箭时用过氧化氢作强氧化剂就是利用这个原理,已知:a.

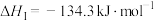
b.

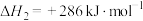
则反应
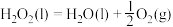 的
的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】对下列探究反应速率和化学平衡影响因素的四个实验,回答下列问题:

(1)利用实验(Ⅰ)探究锌与1mol/L硫酸和4mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(至少写出两项):___ ,___ 。
(2)实验(Ⅱ)已知:Cr2O (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+。D试管中实验现象为
(黄色)+2H+。D试管中实验现象为___ ,用平衡移动原理解释原因:___ 。
(3)实验(Ⅲ)中实验的目的是探究___ 。
(4)在室温下进行实验(Ⅳ)写出反应的离子方程式___ ,溶液褪色的时间:t(A)___ t(B)(填>、<或=)。

(1)利用实验(Ⅰ)探究锌与1mol/L硫酸和4mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(至少写出两项):
(2)实验(Ⅱ)已知:Cr2O
 (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+。D试管中实验现象为
(黄色)+2H+。D试管中实验现象为(3)实验(Ⅲ)中实验的目的是探究
(4)在室温下进行实验(Ⅳ)写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某温度时,在0.5L密闭容器中,某一反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析求得:
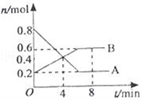
(1)该反应的化学方程式为________________ ;
(2)若降低温度,则v (正)_____ ,v (逆)_____ ;(填“加快”“减慢”或“不变”);
(3)第4min时,正、逆反应速率的大小关系为:v (正)______ v (逆);(填“>”“<”或“=”,下同)
(4)以下措施能加快反应速率的是_________ 。
A.恒温恒容充入He使压强增大 B.缩小体积,使压强增大
C.恒温恒压充入He D.平衡后加入催化剂

(1)该反应的化学方程式为
(2)若降低温度,则v (正)
(3)第4min时,正、逆反应速率的大小关系为:v (正)
(4)以下措施能加快反应速率的是
A.恒温恒容充入He使压强增大 B.缩小体积,使压强增大
C.恒温恒压充入He D.平衡后加入催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段反应速率最大?_______ min(填"0~1,“1~2",“2~3",“3~4”或“4~5”)。
②求3~4 min时间段以盐酸的浓度变化来表示的该反应速率:_______ mol/(L·min)(设溶液体积不变)
(2)另一学生为控制反应速率,防止反应过快难以准确测量氢气体积,为减慢反应速率,下列措施你认为可行的是_______(填字母)。
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
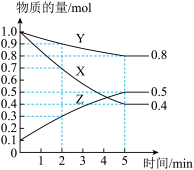
①该反应的化学方程式是_______ ;
②能说明该反应已经达到平衡状态的是_______ ;
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变
D.单位时间内生成1 mol Y的同时消耗2 mol Z
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积mL(标准状况) | l00 | 240 | 464 | 576 | 620 |
②求3~4 min时间段以盐酸的浓度变化来表示的该反应速率:
(2)另一学生为控制反应速率,防止反应过快难以准确测量氢气体积,为减慢反应速率,下列措施你认为可行的是_______(填字母)。
| A.加入蒸馏水 | B.加入同浓度的H2SO4溶液 |
| C.在冷水浴中进行 | D.锌粒改为等量的锌粉 |

①该反应的化学方程式是
②能说明该反应已经达到平衡状态的是
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变
D.单位时间内生成1 mol Y的同时消耗2 mol Z
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO发生如下反应2NO+2CO 2CO2+N2,将NO、CO转化为无毒气体。回答下列问题:
2CO2+N2,将NO、CO转化为无毒气体。回答下列问题:
(1)为了测定在该催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
前4s内的平均反应速率v(CO2)=____ 。0~1s和1~2s时间段内反应速率变化的主要原因是____ 。
(2)一定温度下,在固定容积的密闭容器中,通入1molCO和1molNO,在催化剂作用下发生反应。下列能作为反应达到平衡状态的依据的是____ (填序号)。
a.单位时间内消耗1molCO,同时生成1molNO
b.单位时间内断裂氮氧键的数目与断裂氮氮键的数目相等
c.NO的浓度与CO浓度相等
d.容器内总压强不再改变
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证不同条件对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表格中。
①实验I、II的目的是____ ,实验II选择的实验条件是温度____ 、c(NO)=____ ,c(NO)=____ 。
②对比实验I、III,得出的结论是____ 。
 2CO2+N2,将NO、CO转化为无毒气体。回答下列问题:
2CO2+N2,将NO、CO转化为无毒气体。回答下列问题:(1)为了测定在该催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2,.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(2)一定温度下,在固定容积的密闭容器中,通入1molCO和1molNO,在催化剂作用下发生反应。下列能作为反应达到平衡状态的依据的是
a.单位时间内消耗1molCO,同时生成1molNO
b.单位时间内断裂氮氧键的数目与断裂氮氮键的数目相等
c.NO的浓度与CO浓度相等
d.容器内总压强不再改变
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证不同条件对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表格中。
| 实验编号 | T/℃ | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 催化剂的比表面积/m2•g-1 |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 124 | |||
| III | 350 | 1.20×10-3 | 5.80×10-3 | 82 |
②对比实验I、III,得出的结论是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据我国目前汽车业发展速度,预计 年汽车保有量超过
年汽车保有量超过 亿辆,中国已成为全球最大的汽车市场。因此,如何有效处理汽车排放的尾气,是需要进行研究的一项重要课题。
亿辆,中国已成为全球最大的汽车市场。因此,如何有效处理汽车排放的尾气,是需要进行研究的一项重要课题。
(1)目前,汽车厂商常利用催化技术将尾气中的 和
和 转化成
转化成 和
和 ,化学方程式为:
,化学方程式为:_______________ ;
为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究:
【资料查阅】①不同的催化剂对同一反应的催化效率不同;
②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
(2)完成以下实验设计表(表中不要留空格)。
【图象分析与结论】利用气体传感器测定了三组实验中 浓度随时间变化的曲线图,如图:
浓度随时间变化的曲线图,如图:
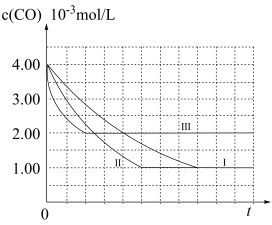
(3)计算第 组实验中,达平衡时
组实验中,达平衡时 的浓度为
的浓度为________ ;
(4)由曲线 、
、 可知,增大催化剂比表面积,汽车尾气转化速率
可知,增大催化剂比表面积,汽车尾气转化速率____________________ (填“增大”、“减小”、“无影响”)。
(5)下列措施中,能减少或控制汽车尾气污染有效且可行的是________ .
A.制定严格的汽车尾气排放标准,并严格执行
B.开发清洁能源汽车,如氢能汽车、太阳能汽车等
C.将污染源移到人口密集度低的郊区
 年汽车保有量超过
年汽车保有量超过 亿辆,中国已成为全球最大的汽车市场。因此,如何有效处理汽车排放的尾气,是需要进行研究的一项重要课题。
亿辆,中国已成为全球最大的汽车市场。因此,如何有效处理汽车排放的尾气,是需要进行研究的一项重要课题。(1)目前,汽车厂商常利用催化技术将尾气中的
 和
和 转化成
转化成 和
和 ,化学方程式为:
,化学方程式为:为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究:
【资料查阅】①不同的催化剂对同一反应的催化效率不同;
②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
(2)完成以下实验设计表(表中不要留空格)。
| 实验编号 | 实验目的 | T / ℃ |  初始浓度 初始浓度 |  初始浓度 初始浓度 | 同种催化剂的比表面积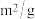 |
 | 为以下实验作参照 | 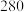 | 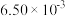 | 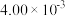 |  |
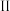 | ① | 280 | 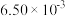 | 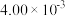 |  |
 | 探究温度对尾气转化速率的影响 |  | ② | 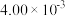 |  |
 浓度随时间变化的曲线图,如图:
浓度随时间变化的曲线图,如图:
(3)计算第
 组实验中,达平衡时
组实验中,达平衡时 的浓度为
的浓度为(4)由曲线
 、
、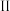 可知,增大催化剂比表面积,汽车尾气转化速率
可知,增大催化剂比表面积,汽车尾气转化速率(5)下列措施中,能减少或控制汽车尾气污染有效且可行的是
A.制定严格的汽车尾气排放标准,并严格执行
B.开发清洁能源汽车,如氢能汽车、太阳能汽车等
C.将污染源移到人口密集度低的郊区
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学反应速率与生产、生活密切相关。
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在 100mL 稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①反应速率最大的时间段是_____ (填“0~1” “1~2” “2~3” “3~4” “4~5”)min,原因是:_____ 。
②反应速率最小的时间段是_____ ,原因是:_____ 。
③2~3min 内该反应的反应速率 (HCl)=
(HCl)=_____ mol·L-1·min-1(设溶液体积不变)。
(2) B 学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列_____ (填字母)以减慢反应速率,同时不影响生成氢气的量。
A.蒸馏水 B.NaOH 溶液 C.Na2CO3溶液 D.CuSO4溶液 E.NaCl 溶液
(3)根据化学反应速率理论,联系化工生产实际,下列说法正确的是_____ (填字母)。
a.化学反应速率理论可指导怎样在一定时间内快出产品
b.催化剂的使用是提高产品产率的有效方法
c.正确利用化学反应速率可以提高化工生产的综合经济效益
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在 100mL 稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况) | 50 | 120 | 232 | 290 | 310 |
②反应速率最小的时间段是
③2~3min 内该反应的反应速率
 (HCl)=
(HCl)=(2) B 学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列
A.蒸馏水 B.NaOH 溶液 C.Na2CO3溶液 D.CuSO4溶液 E.NaCl 溶液
(3)根据化学反应速率理论,联系化工生产实际,下列说法正确的是
a.化学反应速率理论可指导怎样在一定时间内快出产品
b.催化剂的使用是提高产品产率的有效方法
c.正确利用化学反应速率可以提高化工生产的综合经济效益
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,X和Y两物质的浓度随时间变化情况如图。

(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):_________________________ 。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是________________ 。
素材1:某温度和压强下,2L容器中,发生反应2SO2+O2 2SO3,不同时间点测得密闭体系中三种物质的物质的量如下:
2SO3,不同时间点测得密闭体系中三种物质的物质的量如下:
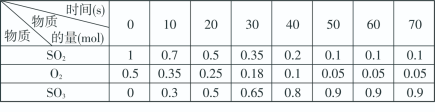
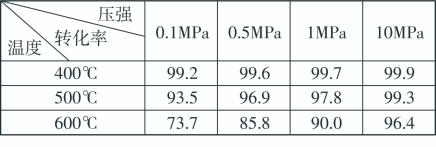
素材2:反应在不同条件下进行时SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的百分数,SO2的转化率越大,化学反应的限度越大)
根据以上的两个素材回答问题:
(3)根据素材1中计算20~30s期间,用二氧化硫表示的化学反应平均速率为________ 。
(4)根据素材2中分析得到,提高该化学反应限度的途径有_______________ 。
(5)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应具体条件是__________________ 。

(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是
素材1:某温度和压强下,2L容器中,发生反应2SO2+O2
 2SO3,不同时间点测得密闭体系中三种物质的物质的量如下:
2SO3,不同时间点测得密闭体系中三种物质的物质的量如下:
素材2:反应在不同条件下进行时SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的百分数,SO2的转化率越大,化学反应的限度越大)

根据以上的两个素材回答问题:
(3)根据素材1中计算20~30s期间,用二氧化硫表示的化学反应平均速率为
(4)根据素材2中分析得到,提高该化学反应限度的途径有
(5)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应具体条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国科研人员研究出了用活性炭对汽车尾气中NO处理的方法:C(s)+2NO(g) N2(g)+CO2(g) ΔH<0。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化关系如图所示:
N2(g)+CO2(g) ΔH<0。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化关系如图所示:
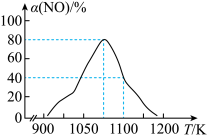
由图可知,温度低于1050K时,NO的转化率随温度升高而增大,原因是___________
 N2(g)+CO2(g) ΔH<0。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化关系如图所示:
N2(g)+CO2(g) ΔH<0。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化关系如图所示:
由图可知,温度低于1050K时,NO的转化率随温度升高而增大,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】羰基硫(COS)能引起催化剂中毒,使化学产品质量下降并引发大气污染,因此工业排放COS前必须对其进行脱硫处理,发生的反应如下:COS(g)+H2(g) H2S(g)+CO(g) 。.
H2S(g)+CO(g) 。.
(1)在480 K 时,将0.l0mol COS(g) 与0.40mol H2(g)充入2.5 L 的空钢瓶中,反应达到平衡后H2S 的物质的量分数为2%。
①COS的平衡转化率a1=_________ %。
②在500 K 时重复实验,测得平衡后H2S的物质的量分数为3%,则COS的转化率a2____________ (填“>”“<”或“=”,下同)a1,该反应的△H________ 0。
(2)若分别向钢瓶中再充入下列气体,能使COS转化率增大的是___________ (填字母)。
A.COS B.H2 C.H2S D.N2
 H2S(g)+CO(g) 。.
H2S(g)+CO(g) 。.(1)在480 K 时,将0.l0mol COS(g) 与0.40mol H2(g)充入2.5 L 的空钢瓶中,反应达到平衡后H2S 的物质的量分数为2%。
①COS的平衡转化率a1=
②在500 K 时重复实验,测得平衡后H2S的物质的量分数为3%,则COS的转化率a2
(2)若分别向钢瓶中再充入下列气体,能使COS转化率增大的是
A.COS B.H2 C.H2S D.N2
您最近一年使用:0次



